如右图所示,将铁棒和石墨棒插入盛有饱和NaCl溶液的U型管中。下列分析正确的是
| A.K1闭合,铁棒上发生的反应为2H++2e-→H2↑ |
| B.K1闭合,石墨棒周围溶液pH逐渐降低 |
| C.K2闭合,铁棒不会被腐蚀,属于外加电流的阴极保护法 |
| D.K2闭合,电路中通过0.4NA个电子时,两极共产生4.48L气体 |
目前,科学家正在研究开发一种高能电池——钠硫电池,它以熔融钠、硫为两极,以导电的β—Al2O3陶瓷作固体电解质,反应式如下:2Na+xS  Na2Sx,以下说法正确的是
Na2Sx,以下说法正确的是
| A.放电时,Na作正极,S极发生还原反应 |
| B.充电时,钠极与外电源的正极相连 |
C.放电时,阳极发生的反应为:S -2e=xS -2e=xS |
| D.若用此电池电解AgNO3溶液,当阳极产生标准状况下的气体1.12L时,消耗的金属钠为4.6g |
某学生欲用电解纯净CuSO4溶液的方法来测定铜的相对原子质量。其实验过程如图所示:

(1)步骤①所加的A的化学式为 ;已知:常温下Fe(OH)3的溶度积Ksp=8.0×10-38,Cu(OH)2的溶度积Ksp=3.0×10-20,通常认为残留在溶液中的离子浓度小于1×10-5 mol·L-1时就认为沉淀完全,设溶液中CuSO4的浓度为3.0 mol·L-1,则加入A调pH范围是_____ ___ (已知lg2=0.3)
(2)步骤②中所用的部分仪器如右图:则A应接在直流电源的 极(填“正”或“负” )。

(3)石墨电极上的电极反应式 。
(4)下列实验操作中必要的是(填字母) 。
| A.称量电解前电极的质量 |
| B.电解后,电极在烘干称重前,必须用蒸馏水冲洗 |
| C.刮下电解后电极上析出的铜,并清洗、称重 |
| D.电极在烘干称重的操作中必须按“烘干→称重→再烘干→再称重”进行 |
E.在有空气存在的情况下,烘干电极必须采用低温烘干的方法
(5)铜的相对原子质量为 (用带有n、V的计算式表示)。
(6)若②用甲醇—O2—熔融碳酸盐电池提供电能,写出该电池负极的电极反应式
下列用来表示物质变化的化学用语中,错误的是
| A.向FeCl3溶液中加入Mg(OH)2:3Mg(OH)2+2Fe3+=2Fe(OH)3+3Mg2+ |
| B.粗铜精炼时,与电源负极相连的是纯铜,电极反应式为:Cu2+ +2e- =Cu |
C.用Pt电极电解氯化铝溶液:2Cl-+2 H2O  Cl2↑+H2+2OH- Cl2↑+H2+2OH- |
| D.由Mg、Al、NaOH溶液组成原电池,其负极反应式为:Al-3e-+4OH-=AlO2-+2H2O |
(1)已知:① 2H2(g)+O2(g)=2H2O(l) △H1=" -a" kJ•mol-1
② 2CO(g)+O2(g)=2CO2(g) △H2 =" -b" kJ•mol-1
③ CO(g)+2H2(g) CH3OH(g) △H3 =" -c" kJ•mol-1
CH3OH(g) △H3 =" -c" kJ•mol-1
计算甲醇蒸气的标准燃烧热H=
(2)①As2S3和HNO3反应如下:As2S3+10H++10NO3-=2H3AsO4+3S+10NO2↑+2H2O,将该反应设计成原电池,则NO2应该在 (填“正极”或“负极”)附近逸出,该极的电极反应式为 。
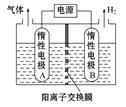
②利用LiOH和钴氧化物可制备锂离子电池正极材料。LiOH可由电解法制备,钴氧化物可通过处理钴渣获得。
利用如图装置电解制备LiOH,两电极区电解液分别为LiOH和LiCl溶液。B极区电解液为 溶液(填化学式),阳极电极反应式为 ,电解过程中Li+向 电极迁移(填“A”或“B”)。
③利用钴渣[含Co(OH)3、Fe(OH)3等]制备钴氧化物的工艺流程如下:
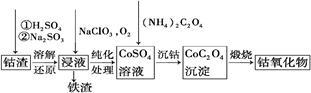
Co(OH)3溶解还原反应的离子方程式为 。
我国科学家最新研发的固体透氧膜提取金属钛工艺,其电解装置如右图所示:将TiO2熔于NaCl-NaF融盐体系,以石墨为阴极,覆盖氧渗透膜的多孔金属陶瓷涂层为阳极,固体透氧膜把阳极和熔融电解质隔开,只有O2-可以通过。下列说法不正确的是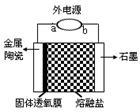
| A.a 极是电源的正极,O2-在熔融盐中从右往左迁移 |
| B.阳极电极反应式为2O2--4e- = O2↑ |
| C.阳极每产生4.48L的O2,理论上能生成0.2mol钛 |
| D.NaCl-NaF融盐的作用是降低熔化TiO2需要的温度 |
某硫酸厂用以下几种方法处理SO2尾气。

(1)活性炭还原法
反应原理:恒温恒容2C (s)+2SO2(g) S2(g)+2CO2(g) 。
S2(g)+2CO2(g) 。
反应进行到不同时间测得各物质的浓度如图:
①第一次出现平衡的时间是第 min;
②0~20min反应速率表示为V(SO2)= ;
③30 min时,改变某一条件平衡发生移动,则改变的条件最有可能是 ;40min时,平衡常数值为__________。
(2)亚硫酸钠吸牧法
①Na2SO3溶液吸收SO2的离子方程式为 ;
②常温下,当吸收至pH=6时,吸收液中相关离子浓度关系一定正确的是____(填序号)
a.c(Na+)+c(H+) >c(SO32-)+c(HSO3-)+ c(OH-)
b.c(Na+) = c(SO32-) + c(HSO3-)+ C(H2SO3)
c.c(Na+)> c(SO32-)> c(OH-)>c(H+)
d.水电离出c(OH一)=l×l0-8 mol/L,
(3)电化学处理法
如图所示,Pt(1)电极的反应式为 ;碱性条件下,用Pt(2)电极排出的S2O42-溶液吸收NO2,使其转化为N2,同时有SO32-生成。若阳极转移电子6mol,则理论上处理NO2气体 mol。

甲醇既可用于基本有机原料,又可作为燃料用于替代矿物燃料。
(1)以下是工业上合成甲醇的两个反应:
反应I: CO(g)+2H2(g) CH3OH(g) ΔH1
CH3OH(g) ΔH1
反应II:CO2(g)+3H2(g) CH3OH(g)+ H2O(g) ΔH2
CH3OH(g)+ H2O(g) ΔH2
① 上述反应符合“原子经济”原则的是 (填“I”或“II”)。
② 下表所列数据是反应I在不同温度下的化学平衡常数(K)。
| 温度 |
250℃ |
300℃ |
350℃ |
| K |
2.041 |
0.270 |
0.012 |
由表中数据判断反应I为______热反应(填“吸”或“放”)。
③ 某温度下,将2 mol CO和6 mol H2充入2L的密闭容器中,充分反应,达到平衡后,测得c(CO)= 0.2 mol/L,则CO的转化率为 ,此时的温度为 (从表中选择)。
(2) 已知在常温常压下:
① 2CH3OH(l)+3O2(g)=2CO2(g)+4H2O(g) ΔH1 kJ/mol
② 2CO(g)+ O2(g)= 2CO2(g) ΔH2 kJ/mol
③ H2O(g)= H2O(l) ΔH3 kJ/mol
则反应CH3OH(l)+ O2(g)= CO(g)+ 2H2O(l) ΔH= kJ/mol
(3)现以甲醇燃料电池,采用电解法来处理酸性含铬废水(主要含有Cr2O2‾7)时,实验室利用下图装置模拟该法:

① N电极的电极反应式为 。
② 请完成电解池中Cr2O2‾7转化为Cr3+的离子反应方程式:
Cr2O7 2‾+ Fe2+ + [ ] ═= Cr3++ Fe3++ H2O
(4) 处理废水时,最后Cr3+以Cr(OH)3形式除去,当c(Cr3+)=1×10‾5 mol•L﹣1时,Cr3+沉淀完全,此时溶液的pH= 。(已知, Ksp[Cr(OH)3]=6.4×10‾31,lg2=0.3)
下图是一个化学过程的示意图。

(1)图中甲池中OH-移向 极(填“CH3OH”或“O2”)。
(2)写出通入CH3OH的电极的电极反应式: 。
(3)向乙池两电极附近滴加适量紫色石蕊试液,附近变红的电极为 极(填“A”或"B”),并写出此电极的反应式:____ 。
(4)乙池中总反应的离子方程式:____ 。
(5)当乙池中B(Ag)极的质量增加5.4g时,乙池的pH是 (若此时乙池中溶液的体积为500mlL);此时丙池某电极析出1.60g某金属,则丙中的某盐溶液可能是 (填序号)。
| A.MgSO4 | B.CuSO4 | C.AgNO3 | D.AlCl3 |
氨气在生产、生活和科研中应用十分广泛
(1)传统工业上利用氨气合成尿素
①以CO2与NH3为原料合成尿素的主要反应如下:
2NH3(g)+CO2(g)=NH2CO2NH4(s) ΔH=-159.47 kJ·mol-1
NH2CO2NH4(s)=CO(NH2)2(s)+H2O(g) ΔH=+ 72.49 kJ·mol-1
反应2NH3(g)+CO2(g)=CO(NH2)2(s)+H2O(g) ΔH= kJ·mol-1。
②液氨可以发生电离:2NH3(l) NH2- + NH4+,COCl2和液氨发生“复分解”反应生成尿素,写出该反应的化学方程式 。
NH2- + NH4+,COCl2和液氨发生“复分解”反应生成尿素,写出该反应的化学方程式 。
(2)氨气易液化,便于储运,可利用NH3作储氢材料
已知:2NH3(g) N2(g) + 3H2(g) ΔH=+92.4 kJ·mol-1
N2(g) + 3H2(g) ΔH=+92.4 kJ·mol-1
① 氨气自发分解的反应条件是 (填“低温” 或 “高温”)。
②其他条件相同,该反应在不同催化剂作用下反应,相同时间后,氨气的转化率随反应温度的变化如右图所示。
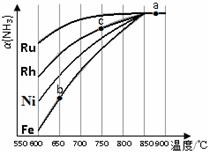
在600℃时催化效果最好的是 (填催化剂的化学式)。c点氨气的转化率高于b点,原因是 。
(3)垃圾渗滤液中含有大量的氨氮物质(用NH3表示)和氯化物,把垃圾渗滤液加入到如图所示的电解池(电极为惰性材料)进行电解除去NH3,净化污水。该净化过程分两步:第一步电解产生氧化剂,第二步氧化剂氧化氨氮物质生成N2。
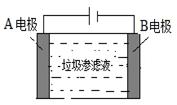
①写出电解时A极的电极反应式: 。
②写出第二步反应的化学方程式: 。
以氨气代替氢气研发氨燃料电池是当前科研的一个热点.
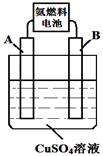
(1)氨燃料电池使用的电解质溶液是2 mol·L-1的KOH溶液,电池反应为:4NH3+3O2 =2N2+6H2O。该反应每消耗1.7g NH3转移的电子数目为 ;
(2)用氨燃料电池电解CuSO4溶液,如右图所示,A、B均为铂电极,通电一段时间后,在A电极上有红色固体析出,则B电极上发生的电极反应式为 ;此时向所得溶液中加入8gCuO固体后恰好可使溶液恢复到电解前的浓度,则电解过程中收集到的气体在标准状况下体积为 L.
(3)纳米级氧化亚铜(Cu2O)是一种重要光电材料。现用铜棒和石墨做电极,饱和食盐水做电解质制备纳米级氧化亚铜(Cu2O),电解反应为 。铜棒上发生的电极反应式为
。铜棒上发生的电极反应式为
甲烷作为一种新能源在化工领域应用广泛,请回答下列问题:
(1)高炉冶铁过程中,甲烷在催化反应室中产生水煤气(CO和H2)还原氧化铁,有关反应为:CH4(g)+CO2(g)===2CO(g)+2H2(g) ;ΔH=+260 kJ·mol-1
已知:2CO(g)+O2(g)===2CO2(g) ;ΔH=﹣566 kJ·mol-1
则CH4与O2反应生成CO和H2的热化学方程式为: _____________________.
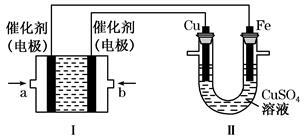
(2)如下图所示,装置Ⅰ为甲烷燃料电池(电解质溶液为KOH溶液),通过装置Ⅱ实现铁棒上镀铜。
①a处应通入_____(填“CH4”或“O2”),b处电极上发生的电极反应式是:
②电镀结束后,装置Ⅰ中溶液的pH值_____(填写“变大”“变小”或“不变”,下同),装置Ⅱ中Cu2+的物质的量浓度 .
③电镀结束后,装置Ⅰ溶液中的阴离子除了OH―以外还含有_____(忽略水解).
④在此过程中若完全反应,装置Ⅱ中阴极质量变化为12.8 g,则装置Ⅰ中理论上消耗甲烷_______L(标准状况下).
在1LK2SO4和CuSO4的混合溶液中,c(SO42-)="2.0" mol·L-1,用石墨作电极电解此溶液,当通电一段时间后,两极均收集到22.4L(标准状况)气体,则原溶液中K+的物质的量浓度为
| A.2.0 mol·L-1 |
| B.1.5 mol·L-1 |
| C.1.0 mol·L-1 |
| D.0.5 mol·L-1 |
将H2S通入FeCl3 溶液中,过滤后将反应液加入电解槽中电解(如下图所示)。电解后的溶液还可以循环利用。该方法可用于处理石油炼制过程中产生的H2S废气。下列有关说法正确的是
| A.过滤得到的沉淀可能是FeS和S |
| B.若有0.20mol的电子转移,一定能得到2.24L的氢气 |
| C.可以用Fe与外接电源的a极相连 |
| D.与a极相连的电极反应式为Fe2+-e-=Fe3+ |
(1)某课外兴趣小组用下图装置进行实验,试回答:

①若开始时开关K与a连接,则A的电极反应式为_________。
②若开始时开关K与b连接,这种方法经常用于金属的防护,这种防护措施叫做_______。
③开关K与b连接,铁和石墨棒互换位置即可制得白色的较纯净Fe(OH)2沉淀,则铁电极反应式为_______。
(2)如下图所示的装置,C、D、E、F都是惰性电极。将电源接通后,向乙中滴入酚酞试液,在F极附近显红色。试回答以下问题:

①电极A的名称是_______。
②甲装置中D电极的电极反应式:_______。
③在25℃时若用惰性电极电解饱和 NaCl溶液一段时间,当阳极产生5.6L(标准状况下)一种气体,电解后溶液体积为50L时,求所得溶液在25℃时的氢氧化钠物质的量浓度=_______。
④欲用丙装置给铜镀银,G应该是________(填“银”或“铜”),电镀液的主要成分是(填化学式)_______。