下列实验能达到预期目的的是( )
| A.滴定管洗净后,直接注入标准液进行滴定 |
| B.用石墨作电极,电解Mg(NO3)2和Cu(NO3)2的混合溶液,确定铜和镁的金属活动性强弱 |
| C.称取19.0g氯化亚锡(SnC12),用蒸馏水溶解,定容至100mL,配制1.0mol/L SnC12溶液 |
| D.测定NaC1和NaF溶液的pH,确定F、C1两元素非金属性的强弱 |
下图是电解CuCl2溶液的装置,其中c、d为石墨电极,则以下有关此电解池的判断正确的是( )

| A.a为负极、b为正极 |
| B.a为阳极、b为阴极 |
| C.电解过程中,d电极质量增加 |
| D.电解过程中,氯离子浓度不变 |
下列说法正确的是( )

| A.图a中,随着电解的进行,溶液中c(H+)增大 |
| B.图b中,Mg电极做电池负极 |
| C.图c中,发生的反应为Co+Cd2+=Cd+Co2+ |
| D.图d中,K分别与M、N连接,Fe电极均受到保护 |
在一个U形管里盛有氯化铜溶液,并插入两块锌片作电极,按下图连接。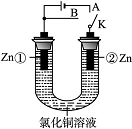
(1)如果把电键K接A,该装置应是________,Zn①为________极,Zn②的电极反应为________________。
(2)上述反应进行5 min后,转换电键K到B,则这一装置是________,Zn②为________极,Zn①的电极反应式是____________________。
(3)将Zn②换成铁片,电解质溶液换成ZnCl2饱和溶液,K接A,此时该装置为______池,阴极电极反应式为____________________________。
关于下列装置的说法正确的是

① ②
| A.①中盐桥内的K+移向CuSO4溶液 |
| B.①将电能转变为化学能 |
| C.若②用于铁棒镀铜,则N极为铁棒 |
| D.若②用于电解精炼铜,溶液中的Cu2+浓度保持不变 |
镉镍可充电电池在现代生活中有广泛应用,它的充、放电反应按下式进行:
Cd+2NiOOH+2H2O Cd(OH)2+2Ni(OH)2
Cd(OH)2+2Ni(OH)2
如果利用该电池精炼铜,则粗铜应连接的极是
| A.NiOOH | B.Ni(OH)2 | C.Cd | D.Cd(OH)2 |
有关下列装置的叙述不正确的是( )
① ②
② ③
③ ④
④
| A.图①铝片发生的电极反应式是:Al+4OH--3e-=AlO2-+2H2O |
| B.图②发生析氢腐蚀,离子反应方程式为:Fe+2H+=Fe2++H2↑ |
| C.图③溶液中发生了变化:4Fe(OH)2+O2+2H2O=4Fe(OH)3 |
| D.图④充电时,阳极反应是:PbSO4+2H2O-2e-=PbO2+SO42-+4H+ |
【化学——选修2:化学与技术】
由黄铜矿(主要成分是CuFeS2)炼制精铜的工艺流程示意图如下:

(1)在反射炉中,把铜精矿砂和石英砂混合加热到10000C左右,黄铜矿与空气反应生成Cu和Fe的低价硫化物,且部分Fe的硫化物转变为低价氧化物,该过程中两个主要反应的化学方程式分别是 , 反射炉内生成炉渣的主要成分是 ;
(2)冰铜(Cu2S和FeS互相熔合而成)含Cu量为20%~50%。转炉中,将冰铜加熔剂(石英砂)在1200°C左右吹入空气进行吹炼。冰铜中的Cu2S被氧化成Cu2O,生成的Cu2O与Cu2S反应,生成含Cu量约为98.5%的粗铜,该过程发生反应的化学方程式分别是 ; ;

(3)粗铜的电解精炼如图所示。在粗铜的电解过程中,粗铜板应是图中电极 (填图中的字母);在电极d上发生的电极反应式为 ;若粗铜中还含有Au、Ag、Fe,它们在电解槽中的存在形式和位置为 。
将含有0.400molCuSO4和0.200molFeCl3的水溶液1L,用惰性电极电解一段时间后,在一个电极上析出19.2gCu,此时在另一电极上放出的气体在标准状况下的体积为
| A.5.60L | B.6.72L | C.4.48L | D.7.84L |
下列四个装置图均与电化学有关,请根据图示回答相关问题:
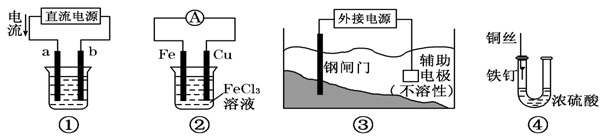
(1)这四个装置中,利用电解原理的是 (填装置序号);
(2)装置①若用来精炼铜,则a极的电极材料是 (填“粗铜”或“精铜”),电解质溶液为 ;
(3)装置②的总反应方程式是 ;
(4)装置③中钢闸门应与外接电源的 极相连(填“正”或“负”)
(5)装置④中的铁钉几乎没被腐蚀,其原因是 。
下列各组中,每种电解质溶液电解时只生成氢气和氧气的是
| A.NaOH、H2SO4、Ba(OH)2 | B.NaOH、CuSO4、H2SO4 |
| C.HCl、CuCl2、Ba(OH)2 | D.NaBr、H2SO4、Ba(OH)2 |
将0.1 mol AgNO3和0.2mol Cu(NO3)2固体溶于水配成100 mL溶液,用惰性电极电解一段时间后,在一极上析出0.15 mol O2,此时,另一极上析出的气体体积(标准状况)为( )
| A.1.12L | B.2.24 L | C.3.36 L | D.4.48L |
下列各组溶液电解一段时间后,再加入相关物质,溶液能恢复原来组成的是
| |
电解质溶液 |
阳极 |
阴极 |
加入的物质 |
| A |
NaCl溶液 |
碳 |
铁 |
盐酸 |
| B |
稀硫酸 |
铜 |
碳 |
水 |
| C |
硫酸铜溶液 |
铜 |
碳 |
硫酸铜 |
| D |
NaOH溶液 |
碳 |
铁 |
水 |
在25 ℃时,用石墨电极电解2.0 L 0.5mol·L-1 CuSO4溶液。5min后,在一个石墨电极上有6.4 g Cu生成。试回答下列问题。
(1)发生氧化反应的是__________极,电极反应式为____________。
(2)若电解后溶液的体积不变,则电解后溶液的pH为____________。
(3)若将溶液恢复到与电解前一样,则需加入________mol的_______。
下列说法正确的是( )
| A.常温下,反应4Fe(OH)2(s)+2H2O(l)+O2(g)═4Fe(OH)3(s)能自发进行,则△H<0 |
| B.铁片镀锌时,铁片与外电源的正极相连 |
| C.以熔融NaCl为电解质进行电解冶炼钠,熔融体中Na+向阳极移动 |
D.t℃时,恒容密闭容器中反应:NO2(g)+SO2(g) NO(g)+SO3(g),通入少量O2, NO(g)+SO3(g),通入少量O2,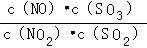 的值及SO2转化率不变 的值及SO2转化率不变 |