(原创)下列表达式正确的是
| A.CH3COOH溶液中CH3COOH的电离:CH3COOH =" H" + + CH3COO— |
B.用CuCl2溶液做导电实验,灯泡发光:CuCl2 Cu2++2Cl- Cu2++2Cl- |
C.NaHCO3溶液中HCO3一的水解:HCO3一+ H2O  H3O + + CO32一 H3O + + CO32一 |
| D.将FeCl3溶液滴入Na2CO3溶液中:2Fe3+ + 3 CO32‾+ 3 H2O = 2Fe(OH)3 ↓+ 3 CO2↑ |
下列关于铜电极的叙述中正确的是
| A.铜锌原电池中铜是负极 |
| B.用电解法精炼粗铜时粗铜作阳极 |
| C.在铁上电镀铜时用铜作阴极 |
| D.电解稀硫酸时用铜作阳极,阳极产生氧气 |
列四个图象的说法中正确的是
| A.图①表示将SO2气体通入溴水中溶液的pH随SO2气体变化关系 |
B.图②表示反应N2(g)+3H2(g) 2NH3(g),△H<0的平衡常数K随温度的变化 2NH3(g),△H<0的平衡常数K随温度的变化 |
| C.图③中阴、阳两极收集到的气体体积之比一定为1:1 |
| D.图④中的△H1<△H2 |
右图是一款笔记本电脑所用甲醇燃料电池的结构示意图。

甲醇在催化剂作用下提供质子(H+)和电子,电子经外电路、质子经内电路到达另一极与氧气反应,电池总反应为:2CH3OH+3O2 = 2CO2+4H2O 下列说法正确的是( )
| A.右电极为电池的正极,b处通入的物质是空气 |
| B.左电极为电池的负极,a处通入的物质是空气 |
| C.正极反应式为:CH3OH+H2O-6e-= CO2+6H+ |
| D.正极反应式为:O2+2H2O+4e-=4OH- |
下列关于电解池的叙述中不正确的是( )
| A.与电源正极相连的是电解池的阴极 |
| B.与电源负极相连的是电解池的阴极 |
| C.在电解池的阳极发生氧化反应 |
| D.电子从电源的负极沿导线流入电解池的阴极 |
如图两个电解槽中,A、B、C、D均为石墨电极。如果电解过程中共有0.02 mol电子通过,下列叙述中正确的是
A.甲烧杯中A极上最多可析出铜0.64 g
B.甲烧杯中B极上电极反应式4OH--4e-=2H2O+O2↑
C.乙烧杯中滴入酚酞试液,D极附近变红
D.乙烧杯中C极上电极反应式为4H++4e-===2H2↑
下列说法正确的是
| A.润洗酸式滴定管时应从滴定管上口加入3~5mL所要盛装的酸溶液,倾斜着转动滴定管,使液体润湿其内壁,再从上口倒出,重复2~3次 |
B.用惰性电极电解MgCl2溶液的离子方程式为:2Cl-+ 2H2O Cl2↑+ H2↑+ 2OH- Cl2↑+ H2↑+ 2OH- |
| C.为验证盐桥的作用,在两个烧杯中分别盛适量硫酸亚铁铵溶液和稀酸性高锰酸钾溶液,分别插入石墨棒用导线与电流计相连,然后用装有K2SO4饱和溶液的琼脂的U型管两端插入两个烧杯中,电流计偏转,一段时间后高锰酸钾溶液褪色 |
| D.嫦娥三号月球车玉兔号在进入第二个月夜休眠前,出现了机构控制异常情况,其病因或为月尘,即月球上直径小于10微米的浮尘,月尘分散在空气中形成的分散系属于胶体。 |
用碱性氢氧燃料电池为电源进行电解的实验装置示意图如下所示。下列说法中正确的是
| A.燃料电池工作时,负极反应为:H2-2e- = 2H+ |
| B.若要实现铁上镀铜,则a极是铁,b极是铜 |
| C.若a极是粗铜,b极是纯铜时,a极逐渐溶解,b极上有铜析出 |
| D.a、b两极均是石墨时,在相同条件下当电池中消耗H222.4L(标准状况)时,a极析出铜64g |
下列实验“操作和现象”与“结论”对应关系均正确的是( )
| |
操作和现象 |
结论 |
| A |
处理锅炉水垢中的CaSO4时,依次加入饱和Na2CO3溶液和盐酸,水垢溶解 |
Ksp:CaCO3<CaSO4 |
| B |
用石墨作电极电解MgSO4溶液,某电极附近有白色沉淀生成 |
该电极为阳极 |
| C |
向FeCl3和CuCl2混合溶液中加入少量铁粉,有红色固体析出 |
氧化性:Cu2+<Fe3+ |
| D |
向某溶液中先滴加硝酸酸化,再滴加BaCl2溶液,有白色沉淀生成 |
该溶液中一定含有Ag+ |
根据下图所示的装置,判断下列说法正确的是
| A.该装置中a极为负极 |
| B.该装置中b极的电极反应式是:2H++2e-= H2↑ |
| C.一段时间后,左边装置中溶液pH增大 |
| D.CuSO4溶液浓度保持不变 |
下列四个装置图均与电化学有关,请根据图示回答相关问题:
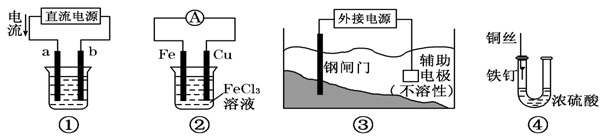
(1)这四个装置中,利用电解原理的是 (填装置序号);
(2)装置①若用来精炼铜,则a极的电极材料是 (填“粗铜”或“精铜”),电解质溶液为 ;
(3)装置②的总反应方程式是 ;
(4)装置③中钢闸门应与外接电源的 极相连(填“正”或“负”)
(5)装置④中的铁钉几乎没被腐蚀,其原因是 。
下列各组中,每种电解质溶液电解时只生成氢气和氧气的是
| A.NaOH、H2SO4、Ba(OH)2 | B.NaOH、CuSO4、H2SO4 |
| C.HCl、CuCl2、Ba(OH)2 | D.NaBr、H2SO4、Ba(OH)2 |
将0.1 mol AgNO3和0.2mol Cu(NO3)2固体溶于水配成100 mL溶液,用惰性电极电解一段时间后,在一极上析出0.15 mol O2,此时,另一极上析出的气体体积(标准状况)为( )
| A.1.12L | B.2.24 L | C.3.36 L | D.4.48L |
下列各组溶液电解一段时间后,再加入相关物质,溶液能恢复原来组成的是
| |
电解质溶液 |
阳极 |
阴极 |
加入的物质 |
| A |
NaCl溶液 |
碳 |
铁 |
盐酸 |
| B |
稀硫酸 |
铜 |
碳 |
水 |
| C |
硫酸铜溶液 |
铜 |
碳 |
硫酸铜 |
| D |
NaOH溶液 |
碳 |
铁 |
水 |