下图是一个化学过程的示意图。
(1)图中乙池是 装置。
(2)c(Pt)电极的名称是 。
(3)写出通入CH3OH的电极的电极反应式是 。
(4)乙池中反应的离子方程式为 。
(5)当乙池中B(Ag)极的质量增加5.40g时,甲池中理论上消耗O2 mL(标准状况下);此时丙池某电极析出1.6g某金属,则丙中的某盐溶液可能是 (填序号)
| A.MgSO4 | B.CuSO4 | C.NaCl | D.CuCl2 |
(1)已知N≡N、N—H、H—H的键能分别为946kJ·mol-1、390.8kJ·mol-1、436.0kJ·mol-1。试根据盖斯定律,写出合成氨反应的热化学方程式 。
(2)在通常状况下,足量氢氧化钠的稀溶液与含溶质为1mol的稀硫酸完全反应时放出akJ的热量,写出该反应中和热的热化学方程式____________。
(3)以镁和铝为电极,以NaOH作电解质溶液,构成原电池时,铝做 极,电极反应式为 ;与MnO2-Zn电池类似,K2FeO4-Zn也可以组成碱性电池,K2FeO4在电池中作为正极材料,其电极反应式为_______________,该电池总反应的离子方程式为_____________。
某实验小组的同学对电化学原理进行了一系列探究活动
(1)如图为某实验小组依据氧化还原反应:(用离子方程式表示) 设计的原电池装置,反应前,两电极质量相等,一段时间后,两电极质量相差18g,则导线中通过 mol电子。
(2)用胶头滴管吸出铁片附近溶液少许置于试管中,向其中滴加少量新制饱和氯水,写出发生反应的离子方程式 ,然后滴加几滴硫氰化钾溶液,溶液变红;继续滴加过量新制饱和氯水,红色褪去,假设之一是“溶液中的+3价铁被氧化为更高的价态”。如果+3价铁被氧化为FeO42-,试写出该反应的离子方程式 。
(3)如图其它条件不变,若将盐桥换成弯铜导线与石墨相连成n型,如图所示,石墨(1)为 极(填“正”、“负”、“阴”或 “阳”)。在甲装置中滴加几滴酚酞试液,振荡均匀,一段时间后,在甲装置中观察到 电极(填“铁”或“铜”)附近溶液先变红,该电极的反应式为 。
(1)已知反应Ⅰ:4NH3(g)+3O2(g)==2N2(g)+6H2O(g) △H=-1266.8kJ/mol
反应Ⅱ:N2(g) + O2(g)="=" 2NO(g) △=+180.5kJ/mol
它们的平衡常数依次为K1、K2
①写出氨高温催化氧化生成NO的热化学方程式 ,该反应的化学平衡常数的表达式K= (用含K1、K2的代数式表示)。
②反应Ⅰ可设计成燃料电池,若该电池以KOH溶液作电解质溶液,则负极的电极反应式为: 。该电池使用过程中,正极附近溶液的pH将 (填“升高”、“降低”或“不变”)。
(2)已知:N2(g) +3H2(g)  2NH3(g) △H=-92kJ/mol。
2NH3(g) △H=-92kJ/mol。
①为提高H2的转化率,宜采取的措施有 (填字母)
| A.及时移出氨 | B.升高温度 |
| C.使用催化剂 | D.循环利用和不断补充N2 |
②在一定温度、压强下,将N2和H2按体积比1:3在密闭容器中混合,当反应达平衡时,测得平衡混合气体中NH3的体积分数为25%,此时H2的转化率为 。
如图是常见原电池装置,电流表G发生偏转:
(1)若两个电极分别是Zn、Cu,电解质溶液是稀硫酸,正极的电极反应式为___________________________;如果把电解质溶液换成硫酸铜溶液,则正极的电极反应式为_____________________________。
(2)若总反应是2FeCl3+Fe=3FeCl2,则可以做负极材料的是________,
负极上发生的电极反应是________________________。
(3)若电解质溶液是稀硫酸,Mg、Al两种金属做电极,则Mg电极的电极反应式为_____________;
若电解质溶液换作稀氢氧化钠溶液,Mg、Al两金属做电极,则Mg是____(填“正极”或“负极”),总反应的离子方程式是_______________________________。
(13分)U、W、X、Y、Z都是短周期元素,且原子序数依次增大。W的气态氢化物甲和W的最高价氧化物对应的水化物可以化合生成盐,U与X可形成常温下呈液态的分子乙,甲、乙均为常见的10 电子分子;Y元素原子的K层电子数与M层电子数相同;Z元素的单质是太阳能转换为电能的常用材料。请回答问题:
(1)Z元素在周期表中的位置 。
(2)X、Y、Z三种元素的原子半径由小到大的顺序是 (用元素符号表示)。
(3)U与X形成的18电子化合物的电子式是 。
(4)(3)中描述的化合物含有的化学键有 。
a.离子键 b.极性共价键 c.非极性共价键
(5)已知:① N2(g)+3H2(g)=2NH3(g) ΔH=-92.4kJ/mol
②2H2(g)+O2(g)=2H2O(g) ΔH=-483.6kJ/mol
试写出氨气完全燃烧生成气态水和氮气的热化学方程式 。
(6)有人设想寻求合适的催化剂和电极材料,以U2、W2为电极反应物,以HCl—NH4Cl溶液为电解质溶液制造新型燃料电池,试写出该电池的正极电极反应式: ;溶液中H+移向 (填“正”或“负”)极。
如图:A、B、C三个烧杯中分别盛有相同物质的量浓度的稀硫酸。
(1)A中反应的离子方程式为 。
(2)B中Sn极的电极反应式为 。Sn极附近溶液的pH值 (填“变大”、“变小”、“不变”)
(3)C中被腐蚀的金属是 ,该电极电极反应式为 ,比较A、B、C中铁被腐蚀的速率,由快到慢的顺序为 。
(共8分)依据氧化还原反应:2Ag+(aq)+Cu(s)=Cu2+(aq)+2Ag(s),设计的原电池如图所示。
请回答下列问题:
(1)电极X的材料是____:电解质溶液Y的溶质是____:
(2)银电极为电池的____极,发生的电极反应为____;x电极上发生的电极反应为____;
(3)盐桥中装有含琼胶的KNO3饱和溶液,则盐桥中NO3-移向____。(填“左侧烧杯”或“右侧烧杯”)
工业生产中含硫废水的排放会污染环境,需要对含硫废水进行处理与利用。
(1)某制革厂含硫废水中主要含有物是Na2S。
①常温下,测得该废水溶液pH=12,用离子方程式解释溶液呈碱性的原因 。
②含硫废水的处理过程中可以采用纯氧将Na2S转化为Na2SO4,则反应中还原剂与氧化剂的物质的量之比为 。已知1000℃时,硫酸钠与氢气发生下列反应:Na2SO4(s) + 4H2(g)  Na2S(s) + 4H2O(g) ,已知该反应的平衡常数K1000℃<K1400℃,则该反应的△H______0(填“>”“=”或“<”)。
Na2S(s) + 4H2O(g) ,已知该反应的平衡常数K1000℃<K1400℃,则该反应的△H______0(填“>”“=”或“<”)。
(2)含硫燃料中间体废水中主要含有物为Na2SO3,回收废水中的硫化物,以减少资源的浪费,可采用以下方法:
①H2S气体与足量NaOH溶液反应的化学方程式
②铁屑与石墨能形成微型原电池,SO32—在酸性条件下放电生成H2S进入气相从而达到从废水中除去Na2SO3的目的,写出SO32—在酸性条件下放电生成H2S的电极反应式: 。
(共10分前2个空每空一个1分,其余每空2分)、
依据氧化还原反应2Ag+(aq)+Cu(s) ="===" Cu2+(aq)+2Ag(s)设计的原电池如图所示:
请回答下列问题:
(1)外电路中的电子是从_______ 电极流向________电极。
(2)银电极发生的电极反应为________________________;
X电极上发生的电极反应为____________________________;
(3)LiSOCl2电池可用于心脏起搏器。该电池的电极材料分别为锂和碳,电解液是LiAlCl4-SOCl2。电池的总反应可表示为4Li+2SOCl2==="4LiCl" +S +SO2↑。请回答下列问题:
写出电池的负极发生的电极反应为______________________________________;
电池正极发生的电极反应为_________________________________________;
按下图所示装置进行实验,并回答下列问题: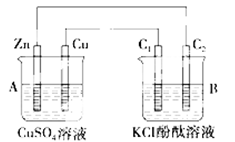
(1)锌极为________极,电极反应式为 ;
铜极为________极,电极反应式为 ;
(2)石墨棒C1为________极,电极反应式为 ;
石墨棒C2附近发生的实验现象为 。
(3)当C2极析出224 mL气体(标准状况)时,锌的质量 (填“增加”或“减少”) g ;
CuSO4溶液的质量 (填“增加”或“减少”) g。
某小组同学设想用如图装置电解硫酸钾溶液来制取氧气、氢气、硫酸和氢氧化钾。
(1)X极与电源的________(填“正”或“负”)极相连,氢气从________(填“A”、“B”、“C”或“D”)口导出。
(2)离子交换膜只允许一类离子通过,则M为________(填“阴离子”或“阳离子”,下同)。
(3)若将制得的氢气、氧气和氢氧化钾溶液组合为氢氧燃料电池(石墨为电极),则电池负极的反应式为____________________________________________________。
(4)若在标准状况下制得11.2 L氢气,则生成硫酸的质量是____,转移的电子数为______。
(12分)如图装置闭合电键时,电流计A的指针将发生偏转。试回答下列问题。
(1)A池是____________;Zn的电极名称是____________;B池是____________;
Pt的电极名称是____________(填电解池、原电池、阴、阳、正、负极等)
(2)写出下列有关反应:C极上电极反应:_________________
(3)B池中的总反应的化学方程式为________________________
依据氧化还原反应:2Ag+(aq)+Cu(s)===Cu2+(aq)+2Ag(s)设计的原电池,如图所示。请回答下列问题:
(1)电极X的材料是________;电解质溶液Y是________溶液。(填名称)
(2)银电极为电池的________极,发生的电极反应为____________________________;X电极上发生的电极反应为____________________________。
(3)外电路中的电子是从________极流向______极(填电极材料)。外电路中每通过0.1 mol电子,银电极的质量理论上增加 g。
(4)原电池工作时,盐桥(装有琼脂-KCl的U型管)里的Cl-移向 电极。