将两个铂电极插人KOH溶液中,向两极分别通人CH4和O2,构成甲烷燃料电池。已知。通人CH4的一极,其电极反应式是:CH4 + 10OH- - 8e-=CO32-+7 H2O;通入O2的另一极,其电极反应式是:2O2 + 4H2O +8e- = 8OH-。下列叙述不正确的是( )。
| A.通人CH4的电极为负极 |
| B.正极发生氧化反应 |
| C.燃料电池工作时,溶液中的OH-向负极移动 |
| D.该电池使用一段时间后应补充KOH |
我国拥有完全自主产权的氢氧燃料电池车在奥运会期间为运动员提供服务。某种氢氧燃料电池的电解液为KOH溶液。下列有关电池的叙述不正确的是( )
| A.正极反应式为:O2+2H2O+4e- ="=" 4OH- |
| B.用该电池电解CuCl2溶液,产生2.24LCl2(标况)时,有0.1mol电子转移 |
| C.该燃料电池的总反应方程式为:2H2+O2==2H2O |
| D.工作一段时间后,电解液中的KOH的物质的量不变 |
熔融盐燃料电池具有高的发电效率,因而受到重视。用Li2CO3和Na2CO3的熔融盐混合物作电解质,一极通CO气体,另一极通O2和CO2混合气体,可制得在650℃下工作的燃料电池。已知该电池总反应为:2CO+O2=2CO2。则下列说法中正确的是( )
| A.通CO的一极是电池的正极 |
| B.正极反应式为:2CO+2CO32--4e-=4CO2 |
| C.负极反应式为:O2+2CO2+4e-=2CO32- |
| D.该电池工作过程中需不断补充CO和O2,而CO2可循环利用 |
碱性电池具有容量大、放电电流大的特点,因而得到广泛应用。锌-锰碱性电池以氢氧化钾溶液为电解液,电池总反应式为:Zn(s)+2MnO2(s)+H2O(l)=Zn(OH)2(s)+Mn2O3(s)。则下列说法正确的是( )
| A.电池工作时,MnO2发生还原反应 |
| B.电池负极的电极反应式为:2MnO2+H2O+2e-→Mn2O3+2OH- |
| C.电池工作时,K+移向负极 |
| D.电池工作时,电路中每通过0.1mol电子,锌的质量理论上减少6.5g |
银锌电池(钮扣式电池)的两个电极分别是由氧化银与少量石墨组成的活性材料和锌汞合金构成,电解质为氢氧化钾溶液,电极反应为 Zn+2OH--2e-=ZnO+H2O;
Ag2O+H2O+2e- = 2Ag+2OH- ;总反应为:Ag2O+Zn=2Ag+ZnO,下列判断正确的是( )
| A.锌为正极,Ag2O为负极 | B.锌为负极,Ag2O为正极 |
| C.原电池工作时,正极区PH减小 | D.原电池工作时,负极区PH增大 |
固体氧化物燃料电池(SOFC)以固体氧化物作为电解质。其工作原理如右图所示:下列关于固体燃料电池的有关说法正确的是 ( )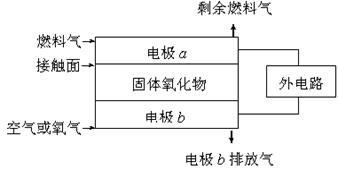
A.电极b为电池负极,电极反应式为O2+4e-=4O2-[
B.固体氧化物的作用是让电子在电池内通过
C.若H2作为燃料气,则接触面上发生的反应为H2+2OH--4e-=2H++H2O
D.若C2H4作为燃料气,则接触面上发生的反应为C2H4+6O2--12e-=2CO2+2H2O
一种基于酸性燃料电池原理设计的酒精检测仪,负极上的反应为:CH3CH2OH – 4e- + H2O = CH3COOH + 4H+。下列有关说法正确的是( )
| A.检测时,电解质溶液中的H+向负极移动 |
| B.若有0.4mol电子转移,则在标准状况下消耗4.48L氧气 |
| C.电池反应的化学方程式为:CH3CH2OH + O2 = CH3COOH + H2O |
| D.正极上发生的反应为:O2 + 4e- + 2H2O = 4OH- |
高功率Ni/MH(M表示储氢合金)电池已经用于混合动力汽车。总反应方程式如下:
Ni(OH)2+M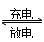 NiOOH+MH,下列叙述正确的是
NiOOH+MH,下列叙述正确的是
| A.放电时正极附近溶液的碱性增强 |
| B.放电时负极反应为:M+H2O+e-===MH+OH- |
| C.放电时阳极反应为:NiOOH+H2O+e-===Ni(OH)2+OH- |
| D.放电时每转移1 mol电子,正极有1 mol NiOOH被氧化 |
高铁电池是一种新型可充电电池,与普通高能电池相比,该电池能长时间保持稳定的放电电压。高铁电池的总反应为:
3Zn+2K2FeO4+8H2O 3Zn(OH)2+2Fe(OH)3+4KOH。下列叙述不正确的是 ( )
3Zn(OH)2+2Fe(OH)3+4KOH。下列叙述不正确的是 ( )
| A.放电时负极反应为: Zn-2e―+2OH―=Zn(OH)2 |
| B.充电时阳极反应为:Fe(OH)3-3e―+5OH―=FeO42-+4H2O |
| C.放电时每转移3mol电子,正极有1molK2FeO4被氧化 |
| D.放电时的正极在充电时须接电源正极 |
被称为“软电池”的纸质电池,采用一个薄层纸片作为传导体,在其一边镀锌,而在其另一边镀二氧化锰。在纸内的离子“流过”水和氧化锌组成的电解液。总反应的化学方程式为:
Zn+2MnO2+H2O===Zn(OH)2+Mn2O3,下列说法错误的是
| A.电池工作时,锌失去电子 |
| B.外电路中每通过0.2 mol电子,锌的质量理论上减小6.5 g |
| C.电池工作时,电子由正极通过外电路流向负极 |
| D.电池正极的电极反应式为:2MnO2+H2O+2e-===Mn2O3+2OH- |
一种新型燃料电池,它以多孔镍板为电极插入KOH溶液中,然后分别向两极上通乙烷(C2H6)和氧气,其电极反应式为:C2H6+18OH——14e-=2CO32—+12H2O,2H2O+O2+4e-=4OH—,有关此电池的推断不正确的是 ( )
| A.正极发生还原反应 | B.正极与负极上参加反应的气体的物质的量之比为2∶9 |
| C.通乙烷的电极为负极 | D.电池工作过程中,溶液的pH逐渐减小 |
一种新型燃料电池,它以多孔镍板为电极插入KOH溶液中,然后分别向两极上通乙烷和氧气,其电极反应式为:C2H6+18OH--14e-=2CO32-+12H2O,2H2O+O2+4e-=4OH-,有关此电池的推断正确的是( )
| A.电池工作过程中,溶液的pH值逐渐减小 |
| B.正极与负极上参加反应的气体的物质的量之比为2:7 |
| C.通乙烷的电极为正极 |
| D.正极发生氧化反应 |
有人设计出利用CH4和O2的反应,用铂电极在KOH溶液中构成原电池。电池的总反应类似于CH4在O2中燃烧,则下列说法正确的是( )
①在标准状况下,每消耗5.6L CH4可以向外电路提供2mole-
②通过甲烷电极的电极反应式为:CH4+10OH--8e-=CO32-+7H2O
③通过甲烷的电极为电池的正极,通过氧气的电极为负极
④电池放电后,溶液pH不断升高
| A.①② | B.①③ | C.①④ | D.③④ |
一种新型燃料电池,一极通入空气,另一极通入甲烷气体;电解质是掺杂氧化钇(Y2O3)的氧化锆(ZrO2)晶体,在熔融状态下能传导O2-.下列对该燃料电池说法正确的是( )
| A.在熔融电解质中,O2-由负极移向正极 |
| B.在外电路,电流从甲烷所通电极流向空气所通电极 |
| C.通入空气的一极是正极,电极反应为:O2-4e-=2O2- |
| D.通入甲烷的一极是负极,电极反应为: CH4-8e-+4O2-=CO2+2H2O |