下列说法正确的是 ( )
| A.某物质的溶解性为难溶,则该物质不溶于水 |
| B.不溶于水的物质的溶解度为0 |
| C.绝对不溶解的物质是不存在的 |
| D.某离子被沉淀完全是指该离子在溶液中的浓度为0 |
已知:Ksp(AgCl)=1.8×10-10;Ksp(Ag2S)=6.3×10-50。向盛0.1mol/L AgNO3溶液的试管中滴加0.1mol/L Na2S溶液至沉淀完全,再滴加足量NaCl溶液,产生的现象或生成的物质是
| A.黑色沉淀完全转化为白色沉淀 | B.既有氯化银也有硫化银 |
| C.只产生黑色硫化银沉淀 | D.只有氯化银白色沉淀 |
某无色透明溶液,可能含有下列离子:Mg2+、Al3+、Fe3+、Ba2+、H+、NH4+、SO42-、HCO3-、Cl-、CO32-。取该溶液进行如下实验:
①取溶液少许,滴入AgNO3溶液产生白色沉淀;
②另取溶液少许,滴入BaCl2溶液产生白色沉淀,加入足量稀硝酸沉淀不溶解;
③另取原溶液500mL,加入过氧化钠固体,产生的沉淀的物质的量与加入过氧化钠的物质的量的关系如下图所示。

根据实验现象和数据分析,回答下列问题:
(1)de段发生的反应的离子方程式是 ;
(2)溶液中肯定存在的离子是 (用离子符号表示);
(3)溶液中可能存在的离子是 (用离子符号表示);
(4)原溶液中金属阳离子的浓度分别为 ;
(5)请在答题卡对应图上画出加入过氧化钠从0~1.1mol时,产生气体的物质的量随加入过氧化钠物质的量变化的曲线(假设生成的气体全部逸出)。
某溶液可能含有Clˉ、SO42ˉ、CO32ˉ、NH4+、Fe3+、Al3+和K+。取该溶液200mL,加入过量浓NaOH溶液,加热,得到448mL气体(标准状况下测定),同时产生红褐色沉淀;过滤,洗涤,灼烧,得到3.2g固体;向上述滤液中加足量BaCl2溶液,得到9.32g不溶于盐酸的沉淀。由此可知原溶液中
| A.至少存在5种离子 |
| B.SO42ˉ、NH4+一定存在,Clˉ可能不存在 |
| C.Clˉ一定存在,且c(Clˉ)≥0.3mol/L |
| D.CO32ˉ、Al3+一定不存在,K+可能存在 |
I.下表是不同温度下水的离子积数据:
| 温度/℃ |
25 |
t 1 |
t 2 |
| 水的离子积 KW |
1×10-14 |
1×10-13 |
1×10-12 |
试回答以下问题:
(1)25℃下,某 Na2SO4溶液中 c(SO42-)=5×10-4 mol∙L-1,取该溶液 1mL 加水稀释至10mL,则稀释后溶液中 c(Na+):c(OH-)=____________。
(2)在 t 2℃下,将 a mol∙L-1CH3COOH 溶液与 b mol∙L-1NaOH 溶液等体积混合反应后,溶液恰好呈中性,则该温度下 CH3COOH 的电离常数 Ka=____________(用 a、b 表示)。
II.已知:25℃下,下列反应:①Ag+(aq)+2NH3(aq)  Ag(NH3)2+(aq) △H =" a" kJ∙mol-1 K = c
Ag(NH3)2+(aq) △H =" a" kJ∙mol-1 K = c
②2Ag+(aq)+2OH-(aq)  Ag2O(s)+H2O(l) △H =" b" kJ∙mol-1 K = d
Ag2O(s)+H2O(l) △H =" b" kJ∙mol-1 K = d
(3)写出 Ag2O溶于氨水(用 NH3表示)生成银氨溶液[Ag(NH3)2+]的热化学方程式:_____________;
计算 25℃下,该反应的平衡常数(用 c、d 表示)K =____________________。
III.某镁盐溶液中含有杂质离子Cr3+,所含主要离子及其浓度如下表所示(H+和OH-未列出):
| 离子 |
Mg2+ |
Cr3+ |
Cl- |
| 浓度(mol/L) |
0.5 |
0.01 |
a |
已知 25℃时,Ksp[Cr(OH)3]=10-32;Ksp[Mg (OH)2]=5×10-11;操作过程中溶液体积的变化忽略不计。
(4)表格中的 a____________1.03(填“<”、“>”或“=”)。
(5)除去杂质Cr3+离子,可加入MgO调节溶液 pH,理论上应调节 pH 的范围是_______________。
(6)溶液经除杂、过滤后,由滤液制取氯化镁晶体(MgCl2∙6H2O)的操作是___________________。
下列溶液均处于 25℃,有关叙述正确的是
| A.AgCl 在同浓度的CaCl2 和NaCl溶液中的溶解度相同 |
| B.0.1 mol∙L-1的Na2S溶液中,c(OH-)=c(H+)+c(HS-)+c(H2S) |
| C.含有 NH4+、Cl-、H+、OH-的溶液中,其离子浓度一定是:c(Cl-)>c(NH4+)>c(H+)>c(OH-) |
| D.pH=4.5的番茄汁中 c(H+) 是 pH=6.5 的牛奶中 c(H+)的 100 倍 |
向盛有0.1mol/LAgNO3溶液的试管中滴加 0.05mol/LNa2S溶液至沉淀完全,再向上层清液中滴加足量 NaCl,产生的现象及发生的反应是
| A.黑色沉淀完全转化为白色沉淀 | B.既有Ag2S也有 AgCl |
| C.不能由黑色沉淀转变为白色沉淀 | D.只有 AgCl白色沉淀 |
下图表示的是难溶氢氧化物在不同pH下的溶解度(S/mol·L-1),下列说法中正确的是( )

| A.pH=3时溶液中铁元素的主要存在形式是Fe3+ |
| B.若Ni(NO3)2溶液中含有少量的Co2+杂质,可通过调节溶液pH的方法来除去 |
| C.若分离溶液中的Fe3+和Cu2+,可调节溶液的pH在4左右 |
| D.若在含有Cu2+和Ni2+的溶液中加入烧碱,Ni(OH)2优先沉淀 |
某溶液中含有KCl、KBr、K2CrO4,浓度均为0.01mol/L,已知Ksp(AgCl)=1.77×10-10,Ksp(AgBr)=5.35×10-13,Ksp(Ag2CrO4)=1.12×10-12,向溶液中逐滴加入0.01mol/LAgNO3溶液时,最先产生沉淀的是( )
| A.AgCl | B.AgBr | C.Ag2CrO4 | D.同时沉淀 |
饱和石灰水中存在溶解平衡:Ca(OH)2(s)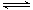 Ca2+(aq)+2OH-(aq),向其中加入少量生石灰,充分反应后恢复至原温度,则下列说法中不正确的是( )
Ca2+(aq)+2OH-(aq),向其中加入少量生石灰,充分反应后恢复至原温度,则下列说法中不正确的是( )
| A.溶液的pH不变 | B.溶液中Ca2+的浓度减小 |
| C.溶液中OH-的数目减小 | D.容器中固体的质量增加 |
常温下,Ksp(CaSO4)=9×10-6,常温下CaSO4在水溶液中的沉淀溶解平衡曲线见右图。下列说法不正确的是
| A.CaSO4溶解在水中,c(Ca2+)=c(SO42-) = 3×10-3mol/L |
| B.在d点溶液中加入一定量的CaCl2可能会有沉淀析出 |
| C.a点对应的Ksp等于c点对应的Ksp |
| D.b点将有沉淀生成,平衡后溶液中c(SO42-)等于3×10-3mol/L |
(1)今有①CH3COOH ②HCl ③H2SO4三种溶液,当它们温度相同、pH相同时,其物质的量浓度由大到小排列的顺序是 (用序号表示)。
(2)某温度下,纯水中的c(H+)=2.0×10-7mol/L,则此时溶液中c(OH-)为__________mol/L。
(3)在25℃下,向浓度均为0.1 mol·L-1的MgCl2和CuCl2混合溶液中逐滴加入氨水,请写出最先生成沉淀的离子方程式为 。
(已知25℃时Ksp[Mg(OH)2]=1.8×10-11,Ksp[Cu(OH)2]=2.2×10-20)。
(4)下列说法不正确的是 (填序号)。
| A.用稀盐酸洗涤AgCl沉淀比用水洗涤损耗AgCl小 |
| B.物质的溶解度随温度的升高而增加,故物质的溶解都是吸热的 |
| C.除去氯化钠溶液中的Mg2+,用NaOH溶液沉淀Mg2+比用Na2CO3溶液效果好,说明相同温度时Mg(OH)2的溶解度比MgCO3大 |
| D.沉淀反应中常加适当过量的沉淀剂,其目的是使相关离子沉淀完全 |
下列叙述正确的是
| A.稀醋酸中加入少量醋酸钠能增大醋酸的电离程度 |
| B.25℃时,等体积等浓度的硝酸与氨水混合后,溶液pH=7 |
| C.25℃时,0.1mol·L-1的硫化氢溶液比等浓度的硫化钠溶液的导电能力弱 |
| D.0.1 mol AgCl和0.1mol AgI混合后加入1L水中,所得溶液中c(Cl-)=c(I-) |
已知硫酸铅难溶于水,也难溶于硝酸,却可溶于醋酸铵溶液形成无色溶液,其化学方程式是PbSO4+2CH3COONH4=Pb(CH3COO)2+(NH4)2SO4。当在醋酸铅溶液中通入H2S时,有黑色沉淀PbS生成,表示这个反应的有关离子方程式正确的是( )
| A.Pb(CH3COO)2+H2S=PbS↓+2CH3COOH |
| B.Pb2++H2S=PbS↓+2H+ |
| C.Pb2++2CH3COO-+H2S=PbS↓+2CH3COOH |
| D.Pb2++2CH3COO-+2H++S2-=PbS↓+2CH3COOH |
下表是25°C时某些盐的浓度积常数和弱酸的电离平衡常数,下列说法正确的是
| A.相同浓度CH3COONa和NaClO的混合液中,各离子浓度的大小关系是c(Na+ )>c(C1O-)>c(CH3COO- )>c(OH-)>c(H+) |
| B.碳酸钠溶液中滴加少量氯水的离子方程式:2CO32-+Cl2+H2O=Cl-+ClO-+2HCO3- |
| C.向0.lmol•L-1CH3COOH 溶液中滴加NaOH 溶液至C(CH3COOH) : C(CH3COO-) =9:5,此时溶液pH = 5 |
| D.向浓度均为1×10 3 mol•L- 的KC1和K2Cr04混合液中滴加1×10 3 mol•L- 的AgN03溶液,CrO42-先形成沉淀 |