一定温度下,三种碳酸盐MCO3(M:Mg2+、Ca2+、Mn2+)的沉淀溶解平衡曲线如下图所示。已知: pM=-lgc(M),pc(CO32-)=-lgc(CO32-)。下列说法正确的是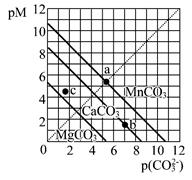
| A.MgCO3、CaCO3、MnCO3的Ksp依次增大 |
| B.a点可表示MnCO3的饱和溶液,且c(Mn2+)> c(CO32-) |
| C.b点可表示CaCO3的饱和溶液,且c(Ca2+)<c(CO32-) |
| D.c点可表示MgCO3的不饱和溶液,且c(Mg2+)<c(CO32-) |
已知Ksp(AgCl)=1.56×10-10,Ksp(AgBr)=7.7×10-13 ,Ksp(Ag2CrO4)=9×10-11。某溶液中含有Cl-、Br-和CrO42-,浓度均为0.010mol/L,向该溶液中逐滴加入0.010mol/L的AgNO3溶液时,三种阴离子产生沉淀的先后顺序为
| A.Cl-、Br-、CrO42- | B.CrO42-、Br-、Cl- |
| C.Br-、Cl-、CrO42- | D.Br-、CrO42-、Cl- |
在25℃时,AgCl的白色悬浊液中,依次加入等浓度的KI溶液和Na2S溶液。观察到的现象是先出现黄色沉淀,最终出现黑色沉淀。已知有关物质的溶度积Ksp (25℃)如下:
| |
AgCl |
AgI |
Ag2S |
| Ksp(单位省略) |
1.8×10-10 |
1.5×10-16 |
6.3×10-50 |
下列叙述错误的是
A.沉淀转化的实质就是沉淀溶解平衡的移动
B.溶解度小的沉淀容易转化为溶解度更小的沉淀
C.AgCl固体在等物质的量浓度的NaCl、CaCl2溶液中的溶解程度相同
D.25℃时,在饱和AgCl、AgI、Ag2S溶液中,所含Ag+的浓度不同
下面是某课外小组从初选后的方铅矿【主要成分PbS,含少量黄铜矿(CuFeS2)中提取硫磺、铜、铅的工艺流程: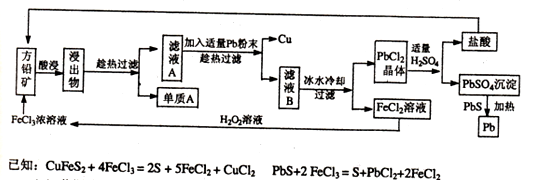
(1)黄铜矿(CuFeS2 )中Fe元素的化合价为 ,提高方铅矿酸浸效率的措施有 (写出两种方法即可)。
(2)过滤过程中用到的玻璃仪器有烧杯、玻璃棒、 ;单质A是 ;在此工艺操作中可循环利用的物质有铅和
(3)在酸性的FeC12溶液中加入H202溶液,其反应的离子方程式为 。
(4)PbS04与PbS加热条件下反应的化学方程式为. .将沉淀PbSO4与足量的碳酸钠溶液混合,沉淀可转化为PbCO3,写出该反应的平衡常数表达式:K= 。(己知Ksp(PbSO4)="1.6x" 10-5,Ksp(PbC03)=3.3x10-14)
(5)铅蓄电池的电极材料分别是Pb和PbO2,电解质溶液为硫酸。铅蓄电池充放电的总反应方程式为:PbO2+Pb+2H2SO4 2PbS04+2H20,充电时,铅蓄电池阳极的电极反应式为 。
2PbS04+2H20,充电时,铅蓄电池阳极的电极反应式为 。
常温下,Ksp(CaSO4)=9×10-6,常温下CaSO4在水中的沉淀溶解平衡曲线见图。下列说法正确的是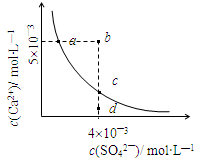
| A.常温下CaSO4饱和溶液中,c(Ca2+)、c(SO42—)对应于曲线上任意一点 |
| B.b点将有沉淀生成,平衡后溶液中c(SO42—)等于3×10-3 mol·L—1 |
| C.d点溶液通过蒸发可以变到c点 |
| D.a点对应的Ksp等于c点对应的Ksp |
相关物质的溶度积常数见下表(25℃):
| 物质 |
Mg(OH)2 |
CH3COOAg |
AgCl |
Ag2CrO4 |
| Ksp(单位略) |
1.1×10-11 |
2.3×10-3 |
1.8×10-10 |
1.9×10-12 |
下列有关说法中不正确的是
A.浓度均为0.2 mol·L-1的AgNO3溶液和CH3COONa溶液等体积混合一定产生CH3COOAg沉淀
B.将0.001 mol·L-1的AgN03溶液滴入0.001 mol·L-1的KCl和0.001 mol·L-1的K2CrO4混合溶液中。先产生Ag2CrO4沉淀
C.0.ll mol·L-1的MgCL2溶液中加入氨水产生Mg(OH)2沉淀时溶液的pH为9
D.在其他条件不变的情况下,向饱和AgCl水溶液中加入NaCl溶液,Ksp(AgCl)不变
铁的化合物在生产生活中的应用广泛。
(1)高铁酸钾(K2FeO4)具有强氧化性,是一种新型高效水处理剂,它在水处理过程中(铁元素被还原为+3 价)的两个作用是____________、_____________。
(2)氧化铁是重要工业颜料,用废铁屑制备它的流程如下图。请回答下列问题: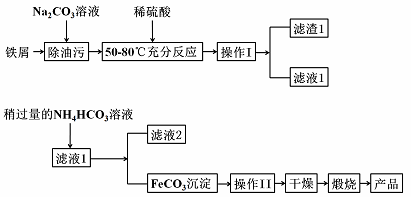
①操作Ⅰ、Ⅱ的名称分别是____________、______________;
②操作I所得滤液中若加入碱性较强的(NH4)2CO3溶液,还会产生 Fe(OH)2,可能的原因是: ,该反应的平衡常数K= (填数值)。【已知:Ksp(FeCO3) = 3.2×10-11,Ksp(Fe(OH)2) = 8.0×10-16】
,该反应的平衡常数K= (填数值)。【已知:Ksp(FeCO3) = 3.2×10-11,Ksp(Fe(OH)2) = 8.0×10-16】
③写出在空气中煅烧FeCO3获得氧化铁产品的化学方程式_____________________;
④煅烧如果不充分,产品中将有Fe2+存在,检验产品中有无Fe2+的实验操作是_______。
(3)含 Cr2O72-的酸性废水可加入FeSO4 将其转化为无毒的Cr3+,反应的离子方程式为 。
对于难溶盐MX,其饱和溶液中M+和X-的物质的量浓度之间的关系类似于c(H+)·c(OH-)=Kw,存在等式c(M+)·c(X-)=Ksp。现将足量的AgCl分别放入下列物质中,AgCl的溶解度由大到小的排列顺序是
①30 mL0.03 mol·L-1 AgNO3溶液 ②30 mL 0.02mol·L-1CaCl2溶液
③30 mL 0.03mol·L-1HI溶液 ④30 mL蒸馏水
| A.①>②>③>④ | B.③>④>①>② |
| C.②>①④>>③ | D.④>③>②>① |
下列说法正确的是
| A.制备硫酸亚铁晶体时,最后在蒸发皿中蒸发浓缩溶液时,只需小火加热至溶液被全部蒸干 |
| B.向1 mL浓度均为0.05 mol·L-1的NaCl、NaI混合溶液中滴加2滴0.01 mol·L-1的AgNO3溶液,振荡,沉淀呈黄色。结论:Ksp(AgCl)<Ksp(AgI) |
| C.0.1mol·L-1的NaOH溶液分别中和pH、体积均相等的醋酸和盐酸,所消耗NaOH溶液的体积:前者小于后者 |
| D.水的电离过程是吸热过程,升高温度,水的离子积增大、pH减小 |
下列有关电解质溶液中粒子浓度关系正确的是
| A.pH相同的①CH3COONa、②NaHCO3、③NaClO三种溶液的c(Na+):①>②>③ |
| B.含有AgCl和AgI固体的悬浊液:c(Ag+)>c(Cl-)=c(I-) |
| C.CO2的水溶液:c(H+)>c(HCO3-)=2c(CO32-) |
| D.含等物质的量的NaHC2O4和Na2C2O4的溶液:3c(Na+)=2[c(HC2O4-)+c(C2O42-)+c(H2C2O4)] |
下列说法中,正确的是
| A.AgI、AgCl与水混合后形成的分散系中:c(Ag+)=c(I-)>c(C1-) |
| B.25℃时,在pH相等的NH4C1溶液和盐酸中,水的电离程度也相等 |
| C.25℃时,将pH=11的NaOH溶液与pH=3的某弱酸HA的溶液等体积混合,混合后的溶液呈碱性 |
| D.25℃时,在pH=2的H2C2O4(一种二元弱酸)溶液与pH=12的NaOH溶液以任意比例混合后形成的溶液中,一定存在:c(Na+)+c(H+)=c(OH-)+c(HC2O4-)+2c(C2O42-) |
高锰酸钾是强氧化剂,它的用途遍布各个行业。
(1)工业上由软锰矿(主要成分为MnO2)生产髙锰酸钾分为两个步骤:
①步骤一将软锰矿与过量的固体KOH和空气在高温下反应,生成锰酸钾(K2MnO4),该反应的化学方程式是 。
②步骤二以石墨为阳极,铁为阴极,电解锰酸钾(K2MnO4)溶液,在 (填“阴极区”或“阳极区”)得到高锰酸钾。阴极反应的电极反应式是 。
(2)某研究小组用工业生产高锰酸钾产生的废渣——锰泥(含K2MnO4、MnO2及Pb、Ca等元素)和乳钢废酸液制取工业级碳酸锰(MnCO3),其流程如下:
③轧钢废酸中Fe2+的作用是 。
④操作I、操作Ⅱ、操作Ⅲ的名称是 。
⑤溶液C中除含有Ca2+、Mn2+、H+外,还含有的阳离子是 。
⑥若固体C中不含CaCO3,则溶液C中 < (已知:Ksp(MnCO3)=1×10-11,Ksp(CaCO3)=5×10-9)。
< (已知:Ksp(MnCO3)=1×10-11,Ksp(CaCO3)=5×10-9)。
(本题共12分)Na2S2O3、Na2S、Na2SO3等含硫化合物在工业上有广泛的用途。
完成下列填空:
28.若将Na2S2O3中的硫元素看作为+2价,下列反应中与Na2S2O3+H2SO4(稀) → Na2SO4+S↓+SO2↑+H2O属于同一类型的是_______(填序号)。
a.2H2S+SO2→ 3S↓+2H2O
b.3NaClO 2NaCl+NaClO3
2NaCl+NaClO3
c.S+2H2SO4(浓)  3SO2↑+2H2O
3SO2↑+2H2O
d.4P+3NaOH+3H2O → 3NaH2PO2+PH3↑
29.棉织物用氯气漂白后,加入Na2S2O3除去余氯时,发生如下反应:
____S2O32―+____Cl2+________ → ___SO42―+___Cl―+___H+
完成并配平该反应方程式;若反应中生成0.2 mol SO42―,则转移电子___________mol。
30.下图是Na2SO3溶液中各离子浓度的相对大小关系示意图。其中,②是_______,④是______(填微粒符号)。
31.已知Na2S溶液显碱性,其主要原因是_________________(用离子方程式解释)。往装有Na2S溶液的烧杯中加入足量的ZnCl2溶液,产生白色的ZnS沉淀;再向烧杯中滴加CuCl2溶液,沉淀转变为黑色。请用溶解平衡原理解释上述现象______________________________________。
从铝土矿(主要成分是Al2O3,含SiO2、Fe2O3、MgO等杂质)中提取两种工艺的流程如下: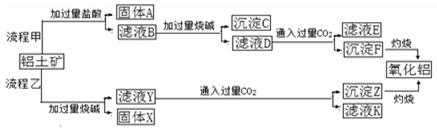
请回答下列问题:
(1)流程甲加入盐酸后生成Al3+的方程式为____________________________.
(2)流程乙加入烧碱后生成SiO32—的离子方程式为______________________.
(3)验证滤液B含Fe3+,可取少量滤液并加入________(填试剂名称)。
(4)滤液E、K中溶质的主要成份是_________(填化学式),写出该溶液的一种用途__________
(5)已知298K时,Mg(OH)2的溶度积常数KSP=5.6×10—12,取适量的滤液B,加入一定量的烧碱达到沉淀溶液平衡,测得PH=13.00,则此温度下残留在溶液中的c(Mg2+)=__________________.