海南省高三5月模拟化学试卷
化学与环境密切相关,下列有关说法正确的是
| A.雾霾是一种自然现象,对人体健康影响不大 |
| B.PM2.5是指大气中直径小于或等于2.5μm的颗粒物 |
| C.大气中SO2含量的增加会导致温室效应加剧 |
| D.酸雨是pH小于7的雨水 |
若NA表示阿伏加德罗常数,下列有关叙述正确的是
| A.标准状况下,44.8L苯中分子数为2NA |
| B.1mol水中含氢离子数为NA |
| C.5.6g铁与足量稀硫酸完全反应失去电子数为0.3NA |
| D.16 g CH4与18 g NH4+所含电子数均为10NA |
下列用品的主要成分及用途对应不正确的是
| |
A |
B |
C |
D |
| 用品 |
 |
 |
 |
 |
| 成分 |
(NH4)2SO4 |
Na2CO3 |
 |
Fe2O3 |
| 用途 |
化肥 |
制玻璃 |
盛放食品 |
涂料 |
下列表示对应化学反应的离子方程式正确的是
| A.用白醋除铁锈:Fe2O3+6H+==3H2O+2Fe3+ |
B.向NH4HCO3溶液中加入过量的Ba(OH)2溶液并加热:Ba2++ 2OH-+NH+ HCO NH3↑+2H2O+BaCO3↓ NH3↑+2H2O+BaCO3↓ |
| C.AlCl3溶液中滴加浓氨水至过量:Al3++4NH3˙H2O ="=" AlO2-+4 NH4++2H2O |
| D.MnO2与浓盐酸反应制取Cl2:MnO2+4H++4Cl-== Mn2++2Cl2↑+2H2O |
硒(Se)与硫在元素周期表中位于同一主族。下列说法不正确的是
| A.原子半径:Se > S | B.沸点:H2S > H2Se |
| C.稳定性:H2S > H2Se | D.酸性:H2SO4 > H2SeO4 |
在25℃时,AgCl的白色悬浊液中,依次加入等浓度的KI溶液和Na2S溶液。观察到的现象是先出现黄色沉淀,最终出现黑色沉淀。已知有关物质的溶度积Ksp (25℃)如下:
| |
AgCl |
AgI |
Ag2S |
| Ksp(单位省略) |
1.8×10-10 |
1.5×10-16 |
6.3×10-50 |
下列叙述错误的是
A.沉淀转化的实质就是沉淀溶解平衡的移动
B.溶解度小的沉淀容易转化为溶解度更小的沉淀
C.AgCl固体在等物质的量浓度的NaCl、CaCl2溶液中的溶解程度相同
D.25℃时,在饱和AgCl、AgI、Ag2S溶液中,所含Ag+的浓度不同
下列鉴别方法可行的是
| A.用氨水鉴别Al3+、Mg2+和Ag+ |
B.用盐酸酸化的BaCl2溶液鉴别Cl-、SO 和CO 和CO |
| C.用溴水鉴别CH4和C2H4 |
| D.用KMnO4酸性溶液鉴别CH3CH2OH和CH3CHO |
下图曲线a和b是盐酸与氢氧化钠溶液的相互滴定的滴定曲线,下列叙述正确的是
| A.NaOH溶液的浓度为0.1 mol·L-1 |
| B.P点时恰好完全反应,溶液呈中性 |
| C.曲线a是盐酸滴定氢氧化钠溶液的测定曲线 |
| D.本实验的指示剂不能用甲基橙,只能用酚酞 |
下列关于有机化合物的说法正确的是
| A.苯在常温下可与溴水发生取代反应 |
| B.糖类、油脂和蛋白质都能发生水解反应 |
| C.乙醇和乙酸都能与金属钠反应 |
| D.葡萄糖能发生氧化反应和银镜反应 |
用图中装置进行实验,实验一段时间后,现象与预测不一致的是
| |
①中物质 |
②中物质 |
实验预测 |
| A |
浓氨水 |
酚酞试液 |
②中溶液变为红色 |
| B |
浓硝酸 |
淀粉KI溶液 |
②中溶液变为蓝色 |
| C |
浓盐酸 |
浓氨水 |
大烧杯中有白烟 |
| D |
饱和的亚硫酸溶液 |
稀溴水 |
②中无明显变化 |
硫酸亚锡(SnSO4)是一种重要的能溶于水的硫酸盐,广泛应用于镀锡工业。SnSO4的实验室制备设计路线如下:
下列有关说法正确的是
| A.SnCl2酸化是为了防止溶解时发生水解 |
| B.反应I中发生的离子反应为:CO32-+2H+=CO2↑+ H2O |
| C.漂洗时,将固体置于烧杯中,加蒸馏水洗涤过滤2~3次 |
| D.操作1为过滤,操作2为结晶 |
某二次电池充、放电的化学方程式为:2K2S2+KI3 K2S4+3KI。与其它设备连接的电路如图示。当闭合开关K时,X附近溶液先变红。则下列说法正确的是
K2S4+3KI。与其它设备连接的电路如图示。当闭合开关K时,X附近溶液先变红。则下列说法正确的是
| A.K+从右到左通过离子交换膜 |
| B.A的电极反应式为:3I--2e-= I3- |
| C.当有0.1 mol K+通过离子交换膜,X电极上产生气体1.12 L(标准状况下) |
| D.电池充电时,B电极要与外电源的正极相连,电极上发生还原反应 |
X、Y、Z、M和N均为短周期元素,X、Y、Z原子序数依次增大且最外层电子数之和为15,X与Z可形成XZ、XZ2型分子, Y与M气态化合物标准状况下密度约0.76g/L。N的原子半径为短周期元素中最大。回答下列问题:
(1)M、Z和N的元素符号分别为 、 、 。
(2)X、Y、Z、M四种元素的原子半径由大到小的顺序为 。
(3)由上述元素组成、既含有共价键又含有离子键的化合物,其中含有极性共价键或含有非极性共价键,各举一例用电子式表示为 、 。
(4)X和Y组成的离子XY-对环境有害,可在NaClO的碱性溶液中转化为碳酸盐和氮气,相应的离子方程式为 。
铁及其化合物在国民经济的发展中起着重要作用。
(1)已知:4Fe(s)+3O2(g)=2Fe2O3(s) △H=-1641.0 kJ·mol-1
C(石墨)+1/2O2(g)=CO(g) △H=-110.5 kJ·mol-1
则Fe2O3(s)+3C(石墨)=2Fe(s)+3CO(g)的 △H= kJ·mol-1。
(2)将NaCl溶液滴在一块光亮清洁的铁板表面上,一段时间后发现液滴覆盖的圆周中心区(a)已被腐蚀而变暗,在液滴外沿形成棕色(b),如图所示。液滴中心是 区(填“正极”或“负极”),其电极反应式为 。为减缓钢铁的腐蚀,可与锌块相连,该方法称为 。
(3)铁钛合金是一种不锈钢材料,某同学在探究该合金的性质时,往含有TiO2+、Fe3+溶液中加入铁屑至溶液显紫色,该过程中发生的反应有:
①2TiO2+(无色)+Fe+4H+=2Ti3+(紫色)+Fe2++2H2O
②Ti3+(紫色)+Fe3++H2O=TiO2+(无色)+Fe2++2H+
③ 。
下图I中表示在2L的密闭容器中、T1温度下,某可逆反应各物质浓度与时间关系;图II表示当其它条件不变时,C物质的体积分数(C%)与温度(T)和压强(p)的关系。回答下列问题:
(1)该可逆反应的化学方程式为 。
(2)上述反应的压强p1 p2,反应的焓变△H 0(填“大于”、“小于”或“等于”)
(3)若温度T1时,5min后反应达到平衡,则
①平衡时体系总的物质的量为 。
②反应的平衡常数K= 。(列式计算)
③反应在0~5min区间的平均反应速率v(B)= 。
化合物C是某合成路线的中间体,可通过下列方法合成:
回答下列问题:
(1)在催化剂作用下,A与氢气反应的化学方程式为 ,反应类型为 。
(2)B的结构简式为 ,所得B的粗产品通常用 的方法提纯。
(3)在C的制备中,浓硫酸的作用是 。
三个化学小组的同学测定某Na2CO3固体样品(仅含NaOH杂质)的纯度,他们提出了各自的气体分析法。
(1)第一小组用图I所示装置,仪器A的名称 。把m1 g的混合物与足量稀硫酸反应后,测定产生的CO2气体的体积。实验开始时需检查该装置气密性,具体的操作方法是 。
(2)第二小组用图II装置测定CO2的质量。该装置存在明显缺陷是: 。
(3)第三小组在第二小组装置的基础上,解决了第二小组装置的问题。所用到的仪器如图III,装置的连接顺序是a— (填写接口字母,图中仪器可重复使用)。实验中取了样品m1 g,称量干燥管质量为m2 g,与足量稀硫酸反应后称量干燥管质量为m3 g,则Na2CO3的纯度表达式为 。
选考[选修5——有机化学基础]
羟基扁桃酸是药物合成的重要中间体,它可由苯酚和乙醛酸在一定的条件下反应制得。
下列有关说法正确的是学
| A.该反应是取代反应 |
| B.苯酚和羟基扁桃酸遇上FeCl3溶液都会显色 |
| C.乙醛酸与H2加成的产物能在催化剂作用下形成高分子化合物 |
| D.1 mol羟基扁桃酸能与3 mol NaOH反应 |
从A出发,发生图示中的系列反应,其中B分子核磁共振氢谱有三组峰,峰面积比为1:2:2,F的苯环上一氯代物只有一种,Z和G均不能与金属钠反应,且互为同分异构体。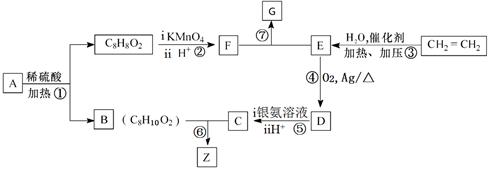
回答下列问题:
(1)F的化学名称为 。
(2)反应④的化学方程式为 ,在①~⑦的反应中,属于取代反应的有 。
(3)B的结构简式为 ,其所含官能团名称为 。
(4)E和F反应生成G的化学方程式为 。
(5)与B互为同分异构体,属于酚类且苯环上只有对位两取代的化合物有 种,写出可能的结构简式 , , , ,。
选考[选修3——物质结构与性质]
下列叙述正确的是
| A.SO32-中硫原子的杂化方式为sp3 |
| B.H2O分子中氧原子的杂化方式为sp2 |
| C.BF3分子呈三角锥体空间型 |
| D.C2H2分子中含有3个σ键和2个π键 |
锂—磷酸氧铜电池正极的活性物质是Cu4O(PO4)2,可通过下列反应制备:
2Na3PO4+4CuSO4+2NH3·H2O=Cu4O(PO4)2↓+3Na2SO4+(NH4)2SO4+H2O
(1)基态Cu2+的核外电子排布式为 。
(2)根据价层电子对互斥模型(VSEPR),PO43-离子内中心原子价层成键电子对和孤电子对之和为 ,离子的空间构型是 。
(3)液氨分子间存在自耦电离:2NH3 NH2-+NH4+,NH2-中氮原子轨道的杂化类型是 ,H+易与NH3形成NH4+,配位键的解释是 。
NH2-+NH4+,NH2-中氮原子轨道的杂化类型是 ,H+易与NH3形成NH4+,配位键的解释是 。
(4) 胆矾CuSO4·5H2O的结构示意图如下,其含有的微粒间作用力有 。(填序号)
胆矾CuSO4·5H2O的结构示意图如下,其含有的微粒间作用力有 。(填序号)
a.离子键
b.极性键
c.金属键
d.配位键
e.氢键
f.非极性键
(5)在硫酸铜溶液中加入过量KCN,生成配合物[Cu(CN)4]2-,Cu2+的配位数为 ,1mol CN-中含有的π键的数目为 。
[选修2——化学与技术]
下列关于工业生产的说法正确的是
| A.在侯氏制碱工业中,向饱和氯化钠溶液中先通二氧化碳,后通氨气 |
| B.在硫酸工业、合成氨工业、硝酸工业中,皆采用循环操作提高原料利用率 |
| C.在氯碱工业,电解槽一般用铁网作电极 |
| D.合成氨工业用天然气造气的方法中,与水蒸汽高温反应优于热分解法 |

 粤公网安备 44130202000953号
粤公网安备 44130202000953号