在一个绝热的体积一定的密闭容器中发生可逆反应:N2(g) + 3H2(g) 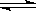 2NH3(g) , △H<0,下列各项中不能说明该反应已经达到平衡状态的是
2NH3(g) , △H<0,下列各项中不能说明该反应已经达到平衡状态的是
| A.体系的压强不再改变 |
| B.体系的温度不再改变 |
| C.断裂1mol N≡N键的同时,也断裂6molN—H键 |
| D.反应消耗的N2、H2与产生的NH3的速率υ(N2) : υ(H2) : υ(NH3) ==1∶3 ∶2 |
一定条件下反应2AB(g)  A2(g)+B2(g)达到平衡状态的标志是
A2(g)+B2(g)达到平衡状态的标志是
A.单位时间内生成n molA2,同时消耗2n molAB
B.容器内三种气体AB、A2、B2共存
C.容器中各组分的体积分数不随时间变化
D.AB的消耗速率等于A2的消耗速率
可逆反应2NO2 2NO+O2在恒容的密闭容器中反应,达到平衡状态的标志是
2NO+O2在恒容的密闭容器中反应,达到平衡状态的标志是
①单位时间内生成n molO2的同时生成2n molNO2
②用NO2、NO、O2的物质的量浓度变化表示的反应速率的比为2 : 2 : 1
③混合气体的颜色不再改变
④混合气体的密度不再改变
⑤混合气体的平均相对分子质量不再改变
| A.①③⑤ | B.①④⑤ | C.①③④⑤ | D.①②③④⑤ |
高温下,某反应达平衡,平衡常数K=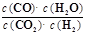 ,恒容时,温度升高,H2浓度减小。下列说法正确的是
,恒容时,温度升高,H2浓度减小。下列说法正确的是
| A.该反应的焓变为正值 |
| B.恒温恒容下,增大压强,H2浓度一定减小 |
| C.升高温度,逆反应速率减小 |
D.该反应化学方程式为CO + H2O CO2+ H2 CO2+ H2 |
在密闭容器中进行如下反应:X2(g)+Y2(g)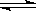 2Z(g),已知X2、Y2、Z的起始浓度分别为0.1mol/L、0.3mol/L、0.2mol/L,在一定条件下,当反应达到平衡时,各物质的浓度有可能是
2Z(g),已知X2、Y2、Z的起始浓度分别为0.1mol/L、0.3mol/L、0.2mol/L,在一定条件下,当反应达到平衡时,各物质的浓度有可能是
| A.Z为0.3mol/L | B.Y2为0.4mol/L |
| C.X2为0.2mol/L | D.Z为0.4mol/L |
体积一定的绝热密闭容器中加入等物质的量的X、Y,进行如下可逆反应:
X(g)+Y(g) Z(g)+W(s)ΔH>0下列叙述正确的是
Z(g)+W(s)ΔH>0下列叙述正确的是
| A.若继续充入X,平衡向正反应方向移动,Y的转化率增大 |
| B.若继续充入Z,平衡逆向移动,Z的体积分数减小 |
| C.若移走部分W,平衡正向移动 |
| D.平衡后移走X,上述反应的ΔH减小 |
在一定的条件下,将10molH2和1molN2充入一密闭容器中,在适当条件下使其发生反应:N2+3H2 2NH3,达到平衡后。则H2的转化率可能是
2NH3,达到平衡后。则H2的转化率可能是
| A.35% | B.30% | C.25% | D.75% |
一定条件下,在一恒容密闭容器中,能表示反应 X(g) + 2Y(g)  2Z(g) 一定达到化学平衡状态的是
2Z(g) 一定达到化学平衡状态的是
① 容器中气体的密度不再发生变化
② X、Y、Z的浓度不再发生变化
③ 容器中的压强不再发生变化
④ 单位时间内生成n mol Z,同时生成2n mol Y
| A.①② | B.②③ | C.③④ | D.①④ |
某温度下的某容积不变的密闭容器中,建立下列化学平衡:C(s)+H2O(g)  CO(g)+H2(g)不能确定上述可逆反应在一定条件下已达到化学平衡状态的是
CO(g)+H2(g)不能确定上述可逆反应在一定条件下已达到化学平衡状态的是
| A.体系的压强不再发生变化 |
| B.v正(CO)=v逆(H2O) |
| C.生成n mol CO的同时生成n mol H2 |
| D.1 mol H—H键断裂的同时断裂2 mol H—O键 |
某温度时,一定压强下的密闭容器中发生反应:aX(g)+bY(g) cZ(g)+dW(g),达平衡后,保持温度不变压强增大至原来的2倍,当再达到平衡时,W的浓度为原平衡状态的1.8倍,下列叙述正确是
cZ(g)+dW(g),达平衡后,保持温度不变压强增大至原来的2倍,当再达到平衡时,W的浓度为原平衡状态的1.8倍,下列叙述正确是
| A.平衡正移 | B.(a+b)>(c+d) |
| C.Z的体积分数变小 | D.X的转化率变大 |
硫化氢的转化是资源利用和环境保护的重要研究课题。由硫化氢获得硫单质有多种方法。
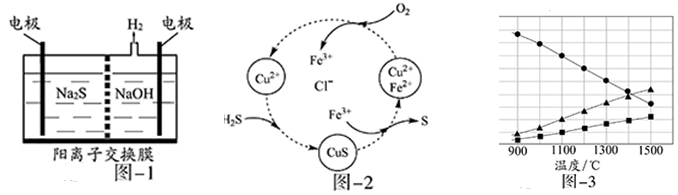
(1)将烧碱吸收H2S后的溶液加入到如图—1所示的电解池的阳极区进行电解。电解过程中阳极区发生如下反应:S2-—2e- S (n—1)S+ S2-
S (n—1)S+ S2- Sn2-
Sn2-
①写出电解时阴极的电极反应式:
②电解后阳极区的溶液用稀硫酸酸化得到硫单质,其离子方程式可写成
(2)将H2S和空气的混合气体通入FeCl3、FeCl2、CuCl2的混合溶液中反应回收S,其物质转化如图—2所示。
①在图示的转化中,化合价不变的元素是
②反应中当有1molH2S转化为硫单质时,保持溶液中Fe3+的物质的量不变,需要消耗O2的物质的量为
③在温度一定和不补加溶液的条件下,缓慢通入混合气体,并充分搅拌。欲使生成的硫单质中不含CuS,可采取的措施有
(3)H2S在高温下分解生成硫蒸气和H2。若反应在不同温度下达到平衡时,混合气体中各组分的体积分数如图—3所示,H2S在高温下分解反应的化学方程式为
甲醇是一种可再生能源,在日常生活中有着广泛的应用.工业上用CO生产燃料甲醇,如:CO(g)+2H2(g)⇌CH3OH(g).图1表示反应中能量的变化;图2表示一定温度下,在体积为2L的密闭容器中加入4mol H2和一定量的CO后,CO和CH3OH(g)的浓度随时间变化.
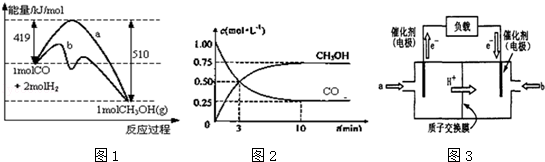
请回答下列问题:
(1)图1表示使用和未使用催化剂时反应过程和能量的对应关系.下列有关催化剂的说法不正确是
| A.降低分子的能量 |
| B.增加了活化分子数 |
| C.提高了活化分子百分数 |
| D.增加了单位体积内的活化分子数 |
(2)从反应开始到建立平衡,该过程中释放 kJ热量.
(3)在T2℃下,将2molCO和6molH2充入2L的密闭容器中,达到平衡状态时,测得C(CO)=0.2mol•L﹣1,则CO的转化率为 .
(4)如图3为常用笔记本电脑所用甲醇质子交换膜燃料电池的结构示意图如.电池总反应为2CH3OH+3O2⇌2CO2+4H2O.在电脑的使用过程中,电池的温度往往因为各种原因会升高.温度升高_____________(填:“有利于”或“不利于”)电池将化学能转化为电能.该装置中_____(填:“a”或“B”)为电池的负极,该电极反应式为 .
已知反应2SO2(g)+O2(g) 2SO3(g);ΔH<0,向某体积恒定的密闭容器中按体积比2∶1充入SO2和O2,在一定条件下发生反应。右图是某物理量(Y)随时间(t)变化的示意图(图中T表示温度),Y可以是( )
2SO3(g);ΔH<0,向某体积恒定的密闭容器中按体积比2∶1充入SO2和O2,在一定条件下发生反应。右图是某物理量(Y)随时间(t)变化的示意图(图中T表示温度),Y可以是( )

| A.O2的体积分数 | B.混合气体的密度 |
| C.密闭容器内的压强 | D.SO2的转化率 |
下述实验操作与预期实验目的或所得实验结论不一致的是( )
| 编号 |
实 验 操 作 |
实验目的或结论 |
| A |
将SO2气体通入紫色石蕊试液中,观察溶液是否褪色 |
证明SO2有漂白性 |
| B |
向试管中加入等体积的0.005mol/L的FeCl3溶液和0.01mol/L的KSCN溶液,再滴加几滴饱和FeCl3溶液,观察颜色变化 |
探究增大反应物浓度时平衡移动的方向 |
| C |
将装有NO2和N2O4气体的联通球,一个置于冰水中,一个置于热水中,观察颜色变化 |
探究温度对化学平衡的影响 |
| D |
将CO2通入Na2SiO3水溶液观察是否有沉淀产生 |
探究碳和硅两元素非金属性强弱 |