(12 分)实验室制乙烯通常采用95%的乙醇与浓硫酸(体积比为1:3)混合加热到170℃制得,请根据实验回答下列问题。
(1)其制备原理可用化学方程式表示为: ,浓硫酸的作用是 。
反应装置中除了加入乙醇和浓硫酸外,还需要加入 (填物质名称)
(2)请从以下装置中选择该反应的反应装置( )
(3)反应过程中乙醇常被炭化,溶液中有黑色物质出现,随着反应进行炭化现象越来越严重,同时制得的乙烯气体中通常会含有CO2、SO2等气体,为确认混合气体中含有乙烯和二氧化硫,可让混合气体依次通过下图实验装置。(可供选择的试剂:品红溶液、氢氧化钠溶液、溴水、酸性高锰酸钾溶液、浓硫酸,试剂可重复使用。)
A.①②中盛放的试剂分别为① ;② ;(填试剂名称)
B.能说明二氧化硫气体存在的现象是 。
C.能确认含有乙烯的现 象是 。
象是 。
Ⅰ.下图是实验室制备乙酸乙酯的装置图,填写下列空白。
(1)试管A中加入沸石的作用是:__________。导管B的作用是导气和___________。
(2)试管C中的饱和碳酸钠溶液作用是:溶解乙醇、中和乙酸、____________。装置中通蒸汽的导管要插在溶液的液面以上,不能插在溶液中,目的是:________________。
(3)要将乙酸乙酯从试管C的混合物中分离出来,必须用到的仪器是_________。
Ⅱ.下图是实验室石油分馏的装置图,填写下列空白。
(4)A仪器的名称是____________,B仪器的名称是____________,B仪器内的水流方向是_______________(选答“上进下出”或“下进上出”)。
某化学小组利用浓盐酸和二氧化锰在加热条件下制取氯气,并利用氯气进行有关的探究实验 ,制取氯气的装置如图I和Ⅱ。
,制取氯气的装置如图I和Ⅱ。
(1)制取氯气的反应的离子方程式 ;
(2)装置Ⅱ中小试管的作用为 ;
(3)装置I与装置Ⅱ比较,装置I的主要优点为: 。
(4)将生成的氯气通入水中,可制得氯水,氯水见光易分解生成 气体。
(5)氯气能使湿润的红色布条褪色。对于使红色布条褪色的物质,同学们的看法不一致,认为氯水中存在的几种粒子都有可能,请利用中学实验室常见试剂,设计实验,得出正确结论。
| 提出问题 |
收集资料 |
提出假设 |
验证假设 |
得出结论 |
| 氯水中何种物质能使湿润的红色布条褪色? |
①Cl2有强氧化性 ②Cl2与冷水反应生成盐酸和HClO ③HClO有强氧化性 |
① 。 ②盐酸使布条褪色。 ③ 。 ④H2O使布条褪色 |
验证假设①:把红色干布条放入充Cl2的集气瓶,布条不褪色; 验证假设②: 。 验证假设④:把红色布条放在水里,布条不褪色。 |
使红色布条褪色的物质是 。 |
下图是实验室用来验证乙烯与氢气反应产物的装置,请回答下列问题:湖北
(1)方框内装置用来制取乙烯,现有下列仪器及用品:①碎瓷片②石棉网和铁架台③圆底烧瓶④温度计(量程100℃)⑤温度计(量程200℃)⑥酒精灯⑦单孔塞⑧双孔塞⑨导管。
其中不需用的仪器及用品有 (填序号)湖北
(2)写出制乙烯化学方程式:
(3)碱石灰的作用是:
(4)溴水的作用是:
(5)出现什么现象可说明生成了乙烷?
海藻中含有丰富的碘元素(以I-形式存在)。实验室中提取碘的流程如下:
(1)实验操作③的名称是 ,所用主要仪器名称为 。
(2)提取碘的过程中,可供选择的有机试剂是 (填序号)。
| A.酒精(沸点78℃) | B.四氯化碳(沸点77℃) |
| C.甘油(沸点290℃) | D.苯(沸点80℃) |
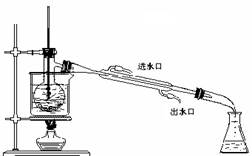
(3)为使从含碘有机溶液中提取碘并回收溶剂顺利进行,采用水浴加热蒸馏(如上图所示)。请指出图中实验装置中错误之处
① _ ___,② ___
(4)实验中使用水浴的原因是 ,最后晶体碘聚集在 (填仪器名称)中。
(5)②处反应化学方程式
(15分)实验室用浓硫酸和乙醇制乙烯时,常会看到烧瓶中液体变黑,并在制得的乙烯中混有CO2、SO2等杂质
(1)写出实验室制取乙烯的化学方程式__________________________________
(2)写出生成上述无机副产物的化学方程式_________________________________________________________。
(3)请从下图中选用所需要的仪器(可重复选用)组成一套能进行上述反应,并检出所得混合气体中含有乙烯、SO2、CO2、H2O(g)的装置(连接用的玻璃管、橡胶管等略去)。
供选用的试剂:浓硫酸、无水乙醇、无水硫酸铜、酸性KMnO4溶液、FeCl3溶液、溴水、品红溶液、澄清石灰水、NaOH溶液、浓盐酸。按仪器连接顺序从上到下将下补充完整。
| 序号 |
选用的仪器(填字母) |
加入的试剂 |
作用 |
| ① |
B |
浓硫酸、无水乙醇 |
反应器 |
| ② |
|
|
|
| ③ |
C |
品红溶液 |
|
| ④ |
C |
|
吸收SO2 |
| ⑤ |
C |
品红溶液 |
|
| ⑥ |
C |
|
检出乙烯 |
| ⑦ |
C |
|
检出CO2 |
(4)能说明混合气体中既有乙烯又有CO2的实验现象是:
___________________________________________________________________。
亚硝酰氯(ClNO)是有机合成中的重要试剂,可由NO与Cl2在通常条件下反应得到。亚硝酰氯有关性质如下:
| 分子式 |
别名 |
熔点 |
沸点 |
溶解性 |
性状 |
| ClNO |
氯化亚硝酰 |
-64.5℃ |
-5.5℃ |
溶于浓硫酸 |
红褐色液体或有毒气体,具有刺激恶臭,遇水反应生成氮的氧化物与氯化氢 |
某研究性学习小组根据亚硝酰氯性质拟在通风橱中制取亚硝酰氯,设计了如图所示实验装置。实验开始前K2处于打开状态,K1、K3均已关闭。、
试回答下列问题:
(1)①若D中装有纯净的NO气体,则B中应选用的试剂为 。实验时利用B除去某些杂质气体并通过观察B中的气泡来判断反应速率,B还具有的作用是 ;②若D中装有纯净的氯气,则C中应选用的试剂为 。
(2)装置F的作用是 ;装置G的作用是 。
(3)若无装置G,则F中ClNO可能发生反应的化学方程式为 。
(4)某同学认为氢氧化钠溶液只能吸收氯气和ClNO,但不能吸收NO,所以装置H不能有效除去有毒气体。为解决这一问题,可将尾气与某种气体同时通入氢氧化钠溶液中,这种气体的化学式是 。
(15分)利用有机反应R-H+Cl2 R-Cl(液)+HCl(气)制取副产品盐酸的设想己成为现实。请根据所给模拟装置图回答下列问题:
R-Cl(液)+HCl(气)制取副产品盐酸的设想己成为现实。请根据所给模拟装置图回答下列问题:
(1)装置B中盛放的溶液是
其作用是 。
(2)写出C装置的三种功能:
① ;
② ;
③ ;
(3)玻璃管D中所放石棉碎块的作用是
玻璃管E中所放碘化钾的作用是
(4)F中导管末端做成“膨大”形的作用是
(5)①点燃A处酒精灯,②点燃D处酒精灯,③通入CH4,这三种操作的先后顺序是
__________ ___(依次填代号)
(10分)实验室用乙醇与浓硫酸共热制取乙烯,常因温度过高生成少量SO2,有人设计了如下图所示实验,以验证上述混合气体中是否含有乙烯和SO2。
(1)装置中X仪器的名称是: ;碎瓷片的作用是: 。
(2)写出生成乙烯的反应方程式: 。
(3)A、B、C、D装置中可盛放的试剂是(从下列所给试剂中选出,填序号):
①品红溶液,②NaOH溶液,③溴水,④KMnO4酸性溶液。
A. ;B. ;C. ;D. 。
(4)能说明SO2气体存在的现象是 。
(5)确证含有乙烯的现象是 。
中学实验室可用同一种装置制备不同的气体,若只有右图装置制备气体
(1)请在下表空格中填上所需药品
| 所制气体 |
药品 |
|
| 分液漏斗内 |
烧瓶中 |
|
| O2 |
|
MnO2 |
| H2 |
稀H2SO4 |
|
| Cl2 |
浓HCl |
MnO2 |
| SO2 |
浓H2SO4 |
Na2SO3 |
| CO2 |
稀H2SO4 |
石灰石 |
(2)写出表中药品制备O2的化学方程式
。
(3)表中给全药品的项目中,不能用于制备相应气体的有(可不填满)
①气体 ,理由 。
②气体 ,理由 。
③气体 ,理由 。
下图所示装置为铜跟浓硫酸反应制取二氧化硫的实验装置:请回答下列问题:
(1)在装置A中放入有关药品后,打开活塞K,将分液漏斗中的液体加入烧瓶中,关闭分液漏斗的活塞,点燃酒精灯,烧瓶中反应的化学方程式为__________。
(2)装置D中试管口放置的棉花中应浸有一种液体,这种液体是________,其作用是_________________。
(3)装置B的作用是贮存多余的二氧化硫和防止其污 染环境,则B中应盛放的液体是(填写字母代号)________;
a.水 b.浓溴水; c.KMnO4酸性溶液 d.NaHSO3饱和溶液
(4)收集二氧化硫完毕,应进行的操作为:________________________________。
(5)若用该套的A、B、C装置制备H2S,则B中应加入的最合理的液体是____________。
(1)写出实验室制乙烯的化学方程式
(2)该实验需加入碎瓷片目的是
(3)下列实验操作正确的是
A、配制乙醇与浓硫酸的混合液时,将1体积乙醇沿烧杯器壁缓缓注入3体积的浓硫酸中,并用玻璃棒不断搅拌
B、加热混合液时,应小心加热使温度缓缓上升至所需温度
C、温度计水银球的位置应伸入液面之下,而不是液面之上
D、收集乙烯气体时应用排水法收集,不能用排空气法收集
(4)在实验室里制取乙烯,常因温度过高而使乙醇和浓硫酸反应生成少量的二氧化硫,有人设计下列实验图以确认上述混合气体中有C2H4和SO2。回答下列问题: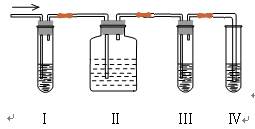
① I、II、III、IV装置可盛放的试剂是
I ;II ;III ;IV (将下列有关试剂的序号填入空格内)。
A、NaOH溶液 B、酸性KMnO4溶液 C、溴水 D、品红溶液
②能说明SO2气体存在的现象是 。
③确定含有乙烯的现象是 。
Ⅰ.为制取较纯净的溴苯和验证反应机理,某化学课外小组设计了实验装置(如右图)。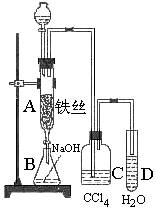
先向分液漏斗中加入苯和液溴,再将混合液慢慢滴入反应器A(A下端活塞关闭)中。
(1)写出A中反应的化学方程式
(2)实验结束时,打开A下端的活塞,让反应 液流入B中,充分振荡,目的是
液流入B中,充分振荡,目的是  。
。
(3)C中盛放CCl4的作用是 。
(4)能证明苯和液溴发生的是取代反应,而不是加成反应,可向试管D中加入AgNO3溶液,若产生淡黄色沉淀,则能证明。设计另外一种方案证明之(写出操作、现象及结论)
Ⅱ.含苯酚的工业废水处理的参考方案如下: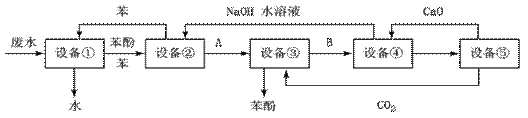
回答下列问题:
(1)设备①进行的是操作____________(填写操作名称),实验室这一步操作所用的仪器是:____________;
(2)由设备②进入设备③的物质A是 ,由设备③进入设备④的物质B是 ;
(3)在设备③中发生反应的化学方程式为_____________________;
(4)在设备④中, 物质B的水溶液和CaO反应,产物是 、 和水,可通过________操作(填写操作名称)分离产物;
(5)上图中,能循环使用的物质是C6H6、CaO、______、______。
现拟在实验室里利用空气和镁粉为原料制取少量氮化镁(Mg3N2)。已知实验中可能会发生下列反应:


可供选择的装置和药品如下图所示(镁粉、还原铁粉均已干燥,装置内所发生的反应是完全的,整套装置的末端与干燥管相连)。
回答下列问题:
(1)在设计实验方案时,除装置A、E外,还应选择的装置(填字母代号)及其目的分别是________________________________________________________________________________
_______________________________________________________________________________。
(2)连接并检查实验装置的气密性。实验开始时,打开自来水的开关,将空气从5升的储气瓶压入反应装置,则气流流经导管的顺序是(填字母代号)______________________________。
(3)通气后,如果同时点燃A、F装置的酒精灯,对实验结果有何影响? __________,原因是_____________________________________________________________________________。
(4)请设计一个实验,验证产物是氮化镁:________________________________________
_______________________________________________________________________________。
有如下图所示六组制取漂白粉的装置,请依据题意回答问题。
(1)有下列几项优缺点:a.不容易控制反应速率;b.容易控制反应速率;c.有副反应发生;d.可防止副反应发生;e.污染环境;f.可防止污染环境。请对上图所示的甲、乙、丙三套装置的优缺点作出评析,选择符合题目要求的选项填在下列空格内。
| |
优点 |
缺点 |
| ①甲装置 |
|
|
| ②乙装置 |
|
|
| ③丙装置 |
|
|
(2)上图所示装置中,甲由A、B两部分组成;乙由C、D、E三部分组成;丙由F、G两部分组成。请从图A~G各部分装置中选取合理的组成部分,组装成一套较完善的实验装置,装置的连接顺序(按气流从左到右的方向)是__________。
(3)实验中若用100 mL 12 mol·L-1的浓盐酸与足量的MnO2反应,最终生成Ca(ClO)2的物质的量总是__________(填“大于”“小于”或“等于”)0.15 mol,其原因是(假定各步反应均无反应物损耗,且用无副反应发生)________________________________________。