实验室制取蒸馏水的装置中,温度计应位于______________________________,蒸馏烧瓶中放沸石的作用是___________________________________,冷凝管中冷凝水的流向应当是_________________________。
某研究性学习小组查阅资料得知,漂白粉与硫酸反应可以制得氯气,化学方程式为:Ca(ClO)2+CaCl2+ 2H2SO4
2H2SO4 2CaSO4+2Cl2↑+2H2O 。他们设计了如下制取氯气并验证其性质的实验。
2CaSO4+2Cl2↑+2H2O 。他们设计了如下制取氯气并验证其性质的实验。
试回答:
(1)该实验中A部分的装置是 (填写装置的序号)。
(2)请你设计一个实验 ,证明洗气瓶C中的Na2SO3已经被氧化(简述实验步骤):
,证明洗气瓶C中的Na2SO3已经被氧化(简述实验步骤):
。
(3)写出D装置中发生反应的离子方程式 。
(4)该实验存在明显的缺陷,请你提出改进的方法 。
(5)该小组又进行了如下实验:称取漂白粉2.0 g,研磨后溶解,配制成250 ml 溶液,取25 ml 加入到锥形瓶中,再加入过量的KI溶液和过量的H2SO4溶液,静置。待完全反应后,用0.1 mol/L的Na2S2O3溶液作标准溶液滴定反应生成的碘,已知反应式为:
2Na2S2O3 + I2 = Na2S4O6 + 2NaI
反应完成时,共用去Na2S2O3 20.0 ml。则该漂白粉中Ca(ClO)2的质量分数为:
实验室用乙醇和浓H2SO4反应制取乙烯时,常发现反应混合液变黑,同时制得的乙醇具有刺激性气味,它是浓H2SO4氧化了乙醇的缘故。试求:
现有以下盛放于洗气瓶中的药品:
| A.溴水 | B.浓NaOH溶液 | C.澄清石灰水 |
| D.酸性KMnO4 E.品红溶液,请设计实验方案证明所制得的乙烯中混有CO2、SO2,同时乙烯能与溴水反应。 |
①写出气体通过洗气瓶时试剂放置的先后顺序(可重复选用) 。
②证明存在SO2的实验现象是 ;
③证明存在CO2的实验现象是 ,
④证明C2H4与溴水反应的实验现象是 。
关于下列各实验装置的叙述中,正确的是 ( )
| A.装置①常用于分离互不相溶的液体 | B.装置②可用于吸收NH3 |
| C.装置③可用于制备乙酸乙酯 | D.装置④可用于收集NO、CO2等气体 |
海洋植物如海带、海藻中含有大量的碘元素,碘元素以碘离子的形式存在。实验室里从海藻中提取碘的流程如下图: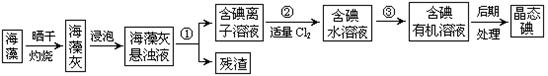
(1)指出提取碘的过程中有关的实验操作名称:① ,③ ;
过程②中有关反应的离子方程式为 。
(2)提取碘的过程中,可供选择的有机试剂是
| A.甲苯、酒精 | B.四氯化碳、苯 | C.汽油、乙酸 | D.汽油、甘油 |
(3)从含碘的有机溶液中提取碘和回收有机溶剂,还须经过蒸馏,指出右面实验装置图中的错误之处: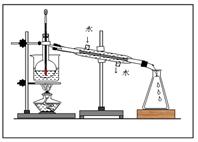
① ;
② ;
③ 。
(4)进行上述蒸馏操作时,使用水浴加热的原因是 ,最后晶态碘在 里聚集。
图为实验室制乙酸乙酯的装置。









 (1)在大试管中配制一定比例的乙醇、乙酸和浓H2SO4混合液的方法为:
(1)在大试管中配制一定比例的乙醇、乙酸和浓H2SO4混合液的方法为:
 (2)装置中通蒸汽的导管要插在饱和Na2CO3溶液的液面以上,不能插在溶液
(2)装置中通蒸汽的导管要插在饱和Na2CO3溶液的液面以上,不能插在溶液 中,目的是:
中,目的是:  (3)浓H2SO4的作用:
(3)浓H2SO4的作用:  (4)饱和Na2CO3的作用:
(4)饱和Na2CO3的作用:  (5)试管中加入沸石的作用:
(5)试管中加入沸石的作用:  (6)实验室生成的乙酸乙酯其密度比水 (填“大”或“小”),
(6)实验室生成的乙酸乙酯其密度比水 (填“大”或“小”), 有 的气味。
有 的气味。
实验室配制500ml 0.1mol·L-1的Na2CO3溶液,回答下列问题:
(1)应用托盘天平称取碳酸钠粉末 g。
(2)配制时应选用的仪器有500ml容量瓶,托盘天平、烧杯、药匙、 。
(3)若实验时遇到下列情况,所配溶液的浓度偏大的是 。
| A.加水定容时超过刻度线,又吸出少量水至刻度线; | B.忘记将洗涤液转入容量瓶; |
| C.容量瓶洗涤后内壁有水珠而未作干燥处理; | |
| D.称量碳酸钠粉末时左盘放砝码,右盘放药品; |
E、定容时俯视刻度线。
现用5mol·L-1的氢氧化钠溶液配制1mol·L-1的氢氧化钠溶液,则所取原氢氧化钠溶液与蒸馏水的体积比约为
| A.1:5 | B.1:4 | C.3:1 | D.1:1 |
(8分)用98%的浓硫酸(其密度为1.84g/cm3)配制100mL1.0mol·L-1稀硫酸,若实验仪器有:
A.100mL量筒 B.托盘天平 C.玻璃棒 D.50mL容量瓶
E.10mL量筒 F.胶头滴管 G.50mL烧杯 H.100mL容量瓶
(1)需量取浓硫酸的体积为 mL。
(2)实验时选用的仪器有(填序号)
(3)配制过程中,下列情况会使配制结果偏高的是(填序号)
①定容时俯视刻度线观察液面
②容量瓶使用时未干燥
③定容后经振荡、摇匀、静置,发现液面低于刻度线,再加蒸馏水补至刻度线
(4)在容量瓶使用方法中,下列操作不正确的是(填序号)
A.使用容量瓶前检查它是否漏水
B.容量瓶用蒸馏水洗净后,再用待配液润洗
C.将氢氧化钠固体放在天平托盘的滤纸上,准确称量并放入烧杯中溶解后,立即注入容量瓶中
D.将准确量取的18.4mol·L-1的硫酸,注入已盛有3 0mL水的100mL的容量瓶中,加水至刻度线
0mL水的100mL的容量瓶中,加水至刻度线
E.定容后塞好瓶塞,用食指顶住瓶塞,用另一只手的手指托住瓶底,把容量瓶倒转摇匀
实验室需用480mL 0.100 mol/L的CuSO4溶液,下列配置方法正确的是:
| A.称取7.68gCuSO4固体,加入480mL水 | B.称取12.0g胆矾配制成480mL溶液 |
| C.称取8.0gCuSO4固体,加入500mL水 | D.称取12.5 g胆矾配制成500mL溶液 |
用下图所示装置制取表中的四种干燥、纯净的气体(图中加热及气体收集装置均已略去;必要时可以加热;a、b、c、d表示相应仪器中加入的试剂)。
| |
气体 |
a |
b |
c |
d |
| A |
CO2 |
稀盐酸 |
CaCO3 |
饱和Na2CO3 |
浓H2SO4 |
| B |
Cl2 |
浓盐酸 |
MnO2 |
NaOH溶液 |
浓H2SO4 |
| C |
SO2 |
稀H2SO4 |
Cu |
品红溶液 |
浓H2SO4 |
| D |
O2 |
H2O2 |
MnO2 |
浓H2SO4 |
浓H2SO4 |
上述方法中可以得到干燥、纯净的气体是
| A.CO2 | B.Cl2 | C.SO2 | D.O2 |
下列除杂方法正确的是
| A.乙烷气体中混有乙烯,通入氢气,使乙烯发生加成反应 |
| B.氯化钠溶液中混有少量硫酸钠,加入适量硝酸钡溶液,过滤 |
| C.乙醇中混有乙酸,加入氢氧化钠后,分液 |
| D.二氧化碳气体中混有少量的二氧化硫,通入酸性高锰酸钾溶液 |
欲除去混在苯中的少量苯酚,下列实验方法正确的是
| A.分液 | B.加入氢氧化钠溶液后,充分振荡,静置后分液 |
| C.加入过量溴水,过滤 | D.加入FeCl3溶液后,过滤 |
一化学兴趣小组的同学通过如下实验提取海带中的碘:
①粉碎海带,加一定量的氢氧化钾溶液后高温灰化;
②用水浸泡海带灰,过滤;
③用盐酸酸化滤液,加入碘酸钾(KIO3)氧化溶液中的碘离子(I—),生成碘单质;
④用四氯化碳溶液萃取水溶液中的碘。
请回答下列问题:(共6分)
(1)实验步骤③中相关的化学反应的方程式为
(2)实验步骤③中也可用H2O2代替KIO3,相关化学反应的方程式为
。
(3)检验用四氯化碳萃取碘后的水溶液是否还有碘单质的实验方法是
。