实验室用下图所示装置制备干燥纯净的氯气,并进行氯气的性质实验。请回答下列问题:
(1)A中盛有浓盐酸,B中盛有MnO2,则烧瓶中发生反应的化学方程式为:
 (2)C中盛有饱和食盐水,其作用是 ,D中浓硫酸的作用是 。
(2)C中盛有饱和食盐水,其作用是 ,D中浓硫酸的作用是 。
(3)F中是FeCl2溶液,F中发生反应的离子方程式为
(4)G中是AgNO溶液,现象是
(5)H中盛有Na0H溶液,其作用是 。
短周期元素的单质X、Y、Z在通常状况下均为气态,并有右图转化关系(反应条件略去),已知:
a.常见双原子单质分子中,X分子含共价键最多。
b.甲分子中含10个电子,乙分子含有18个电子。
(1)X的电子式是_______________________。
(2)实验室可用下图所示装置(缺少收集装置,夹持固定装置略去)制备并收集甲。
①在图中方框内绘出收集甲的仪器装置简图。
②试管中的试剂是____________________。(填写化学式)
③烧杯中溶液由无色变为红色,其原因是(用电离方程式表示)_________________________。 (3)磷在Z中燃烧可生成两种产物,其中一种产物丁分子中各原子最外层不全是8电子结构,丁的化学式是__________。
(3)磷在Z中燃烧可生成两种产物,其中一种产物丁分子中各原子最外层不全是8电子结构,丁的化学式是__________。
现有:淀粉溶液、蛋清、葡萄糖溶液,区别它们时,下列试剂和对应现象依次是( ) 试剂:①新制Cu(OH)2
试剂:①新制Cu(OH)2  ②碘水 ③浓硝酸
②碘水 ③浓硝酸 现象:a. 变蓝色 b. 砖红色沉淀 c. 变黄色
现象:a. 变蓝色 b. 砖红色沉淀 c. 变黄色
| A.②-a、①-c、③-b | B.③-a、②-c、①-b |
C.②-a、③-c、①-b | D.②-c、③-a、①-b |
下列物质的转化或分离错误的是( )
| A.煤干馏可转化为焦炉气、煤焦油、焦炭等 | B.原油分馏可分离出汽油、煤油、柴油等 |
| C.从海水中得到的无水MgCl2可用电解的方法获得镁 | |
| D.从碘水中得到碘,可用酒精萃取 |
某研究性学习小组查阅资料得知:漂白粉与硫酸溶液反应可制取氯气,化学方程式为:Ca(C1O)2+CaCl2+H2SO4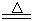 2CaSO4+2Cl2↑+2H2O,该组学生针对上述反应设计如下装置来制取氯气并验证其性质。
2CaSO4+2Cl2↑+2H2O,该组学生针对上述反应设计如下装置来制取氯气并验证其性质。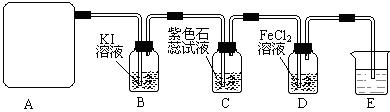
试回答下列问题:
(1)每生成1 mol Cl2,上述化学反应中转移的电子个数为______ (NA表示阿伏加德罗常数)。
(2)该实验中A处可选用装置__________ _____ (填写装置的序号)。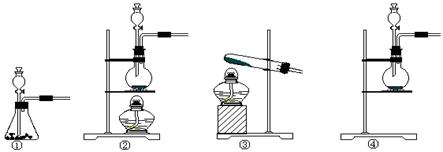
(3)装置B中发生反应的离子方程式为________________________________________。
(4)装置C中的现象为___________________________________________________,
试结合反应方程式解释其原因 __________________________________ _
_________________________________ 。
(5)装置E中的试剂是______________(任填一种合适试剂的名称),其作用是________
_______________________________ ______。
(6)请帮助该学习小组同学设计一个实验,证明装置D中有FeCl3生成(请简述实验 步骤)
步骤)
_________________________________________________________________________
_________________________ __________________________ ______________
__________________________ ______________
乙酸乙酯是重要的有机合成中间体,广泛应用于化学工业。实验室用乙酸与乙醇反应制备乙酸乙酯。为证明浓硫酸在该反应中起到了催化剂和吸水剂的作用,某同学利用上图所示装置进行了以下四个实验 ,实验开始先用酒精灯微热3min,再加热使之微微沸腾3min。实验结束后充分振荡试管Ⅱ再测有机层的厚度,实验记录如下:
,实验开始先用酒精灯微热3min,再加热使之微微沸腾3min。实验结束后充分振荡试管Ⅱ再测有机层的厚度,实验记录如下:
| 实验 编号 |
试管Ⅰ中的试剂 |
试管Ⅱ中试剂 |
测得有机层的厚度/cm |
| A |
2mL乙醇、2mL乙酸、1mL 18mol·L-1浓硫酸 |
|
5.0 |
| B |
3mL乙醇、2mL乙酸 |
0.1 |
|
| C |
3mL乙醇、2mL乙酸、6mL 3mol·L-1硫酸 |
1.2 |
|
| D |
3mL乙醇、2mL乙酸、盐酸 |
1.2 |
(1)试管Ⅱ中试剂的名称为 ,其作用是
,使用干燥管的目的是 。
(2)分析比较实验 (填实验编号)的数据,可以推测出浓硫酸的吸水性提高了乙酸乙酯的产率。浓硫酸的吸水性能够提高乙酸乙酯产率的原因是 。
(3)实验D的目的是与实验C相对照,证明H+对酯化反应具有催化作用。实验D中应加入盐酸的体积和浓度分别是 mL和 mol·L-1。
括号内物质为杂质,下列除去杂质的做法不正确的是
A.乙酸乙酯(乙酸和乙醇):用饱和Na2CO3溶液洗涤后分液 |
B.乙烷(乙烯):用浓溴水洗气 |
C.乙醇(乙酸):用NaOH溶液中和后分液 |
D.乙醇(水):用生石灰吸水后蒸馏 |
下列各实验,不可能成功的是( )
①蒸馏普通酒精制无水乙醇;②苯与浓硫酸混合加热至60℃制硝基苯;③用苯和溴水混合制溴苯;④用裂化汽油从碘水中提取碘
| A.只有①和④ | B.只有②和③ | C.只有①和③ | D.①②③④ |
用下列实验装置进行的实验中,不能达到相应实验目的的是
| A.装置甲:防止铁钉生锈 | B.装置乙:可制得金属锰 |
| C.装置丙:实验室制取乙酸乙酯 | D.装置丁:验证HCl气体在水中的溶解性 |
下列实验操作或步骤正确的是( )
| A.在制备乙酸乙酯的过程中,在大试管中加入药品的顺序是乙醇,浓硫酸,乙酸 |
| B.做CH4与氯气取代反应实验时,将装有甲烷,氯气混合气体的大试管直接放在强光下照射 |
| C.为验证钠可以和乙醇反应生成氢气,将少量钠单质放入到含40%乙醇的饮用白酒中 |
| D.在制备乙酸乙酯实验中,将产生的蒸气经导管通入到饱和NaOH溶液中 |
(12 分)实验室制乙烯通常采用95%的乙醇与浓硫酸(体积比为1:3)混合加热到170℃制得,请根据实验回答下列问题。
(1)其制备原理可用化学方程式表示为: ,浓硫酸的作用是 。
反应装置中除了加入乙醇和浓硫酸外,还需要加入 (填物质名称)
(2)请从以下装置中选择该反应的反应装置( )
(3)反应过程中乙醇常被炭化,溶液中有黑色物质出现,随着反应进行炭化现象越来越严重,同时制得的乙烯气体中通常会含有CO2、SO2等气体,为确认混合气体中含有乙烯和二氧化硫,可让混合气体依次通过下图实验装置。(可供选择的试剂:品红溶液、氢氧化钠溶液、溴水、酸性高锰酸钾溶液、浓硫酸,试剂可重复使用。)
A.①②中盛放的试剂分别为① ;② ;(填试剂名称)
B.能说明二氧化硫气体存在的现象是 。
C.能确认含有乙烯的现 象是 。
象是 。
Ⅰ.下图是实验室制备乙酸乙酯的装置图,填写下列空白。
(1)试管A中加入沸石的作用是:__________。导管B的作用是导气和___________。
(2)试管C中的饱和碳酸钠溶液作用是:溶解乙醇、中和乙酸、____________。装置中通蒸汽的导管要插在溶液的液面以上,不能插在溶液中,目的是:________________。
(3)要将乙酸乙酯从试管C的混合物中分离出来,必须用到的仪器是_________。
Ⅱ.下图是实验室石油分馏的装置图,填写下列空白。
(4)A仪器的名称是____________,B仪器的名称是____________,B仪器内的水流方向是_______________(选答“上进下出”或“下进上出”)。
某化学小组利用浓盐酸和二氧化锰在加热条件下制取氯气,并利用氯气进行有关的探究实验 ,制取氯气的装置如图I和Ⅱ。
,制取氯气的装置如图I和Ⅱ。
(1)制取氯气的反应的离子方程式 ;
(2)装置Ⅱ中小试管的作用为 ;
(3)装置I与装置Ⅱ比较,装置I的主要优点为: 。
(4)将生成的氯气通入水中,可制得氯水,氯水见光易分解生成 气体。
(5)氯气能使湿润的红色布条褪色。对于使红色布条褪色的物质,同学们的看法不一致,认为氯水中存在的几种粒子都有可能,请利用中学实验室常见试剂,设计实验,得出正确结论。
| 提出问题 |
收集资料 |
提出假设 |
验证假设 |
得出结论 |
| 氯水中何种物质能使湿润的红色布条褪色? |
①Cl2有强氧化性 ②Cl2与冷水反应生成盐酸和HClO ③HClO有强氧化性 |
① 。 ②盐酸使布条褪色。 ③ 。 ④H2O使布条褪色 |
验证假设①:把红色干布条放入充Cl2的集气瓶,布条不褪色; 验证假设②: 。 验证假设④:把红色布条放在水里,布条不褪色。 |
使红色布条褪色的物质是 。 |
下图是实验室用来验证乙烯与氢气反应产物的装置,请回答下列问题:湖北
(1)方框内装置用来制取乙烯,现有下列仪器及用品:①碎瓷片②石棉网和铁架台③圆底烧瓶④温度计(量程100℃)⑤温度计(量程200℃)⑥酒精灯⑦单孔塞⑧双孔塞⑨导管。
其中不需用的仪器及用品有 (填序号)湖北
(2)写出制乙烯化学方程式:
(3)碱石灰的作用是:
(4)溴水的作用是:
(5)出现什么现象可说明生成了乙烷?
海藻中含有丰富的碘元素(以I-形式存在)。实验室中提取碘的流程如下:
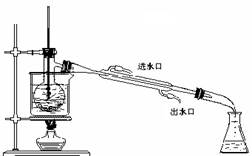
(1)实验操作③的名称是 ,所用主要仪器名称为 。
(2)提取碘的过程中,可供选择的有机试剂是 (填序号)。
| A.酒精(沸点78℃) | B.四氯化碳(沸点77℃) |
| C.甘油(沸点290℃) | D.苯(沸点80℃) |
(3)为使从含碘有机溶液中提取碘并回收溶剂顺利进行,采用水浴加热蒸馏(如上图所示)。请指出图中实验装置中错误之处
① _ ___,② ___
(4)实验中使用水浴的原因是 ,最后晶体碘聚集在 (填仪器名称)中。
(5)②处反应化学方程式