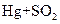2.0g Cu2S和CuS的混合物在酸性溶液中用400 mL 0.075 mol·L-1 KMnO4溶液处理,发生反应如下:
8 MnO4_ + 5 Cu2S + 44 H+ ="===" 10 Cu2+ + 5 SO2 + 8 Mn2+ + 22 H2O
6 MnO4_ + 5 CuS + 28 H+ ="===" 5 Cu2+ + 5 SO2 + 6 Mn2+ + 14 H2O
(1)上述两个反应具有完全相同的_____________(可多选)
A氧化剂 B还原剂 C氧化产物 D还原产物
(2) 反应后煮沸溶液,赶尽SO2,剩余的KMnO4恰好与350 mL 0.10 mol·L-1(NH4)2Fe(SO4)2溶液完全反应。配平KMnO4与(NH4)2Fe(SO4)2反应的离子方程式:
□MnO4_ + □Fe2+ + □H+——□Mn2++ □Fe3++ □_______
KMnO4溶液与混合物反应后,剩余KMnO4的物质的量为_________mol。
(3)混合物中Cu2S的质量分数为_________%。(写出解题过程)
实验室用MnO2和浓盐酸共热来制氯气:MnO2 + 4HCl (浓) ="= " MnCl2 + Cl2↑+ 2H2O
⑴该反应中的还原产物是
⑵在反应方程式中标明电子转移的方向和数目
⑶如反应中转移了0.4mol电子,则产生的气体在标准状况下体积为
已知2KClO3+I2=2KIO3+Cl2,下列对此反应的说法不正确的是
| A.氧化产物与还原产物的物质的量比为2︰1 |
| B.若在标准状况下产生11.2 LCl2,转移电子的物质的量为1mol |
| C.上述反应说明:I2的还原性强于Cl2 |
| D.上述反应属于置换反应 |
FeS与一定浓度HNO3反应,生成Fe2(SO4)3.Fe(NO3)3.NO2.NO和H2O,当NO2和NO的体积为1∶1时实际参加反应的FeS与HNO3的物质的量之比是( )
A.4∶9 |
B.2∶9 | C.2∶11 | D.1∶7 |
在反应5KCl+KClO3+3H2SO4=3Cl2↑+3K2SO4+3H2O中,氧化剂是__________,还原剂是__________;氧化剂具有__________性;被氧化和被还原的原子数之比是__________。
(1)质量都为3 g的镁和铝,物质的量之比为 ;将它们分别放入适量的盐酸溶液中恰好完全反应,则消耗的盐酸的物质的量之比为 。
(2)在50 mL NaNO3和Na2SO4的混合溶液中,c (Na+) =" 1" mol/L,往其中加入50 mL BaCl2溶液恰好完全反应,后得到2.33 g白色沉淀,则原混合溶液中c (NO3-)= mol/L。
(3)已知Cu3P中P为 -3价,在反应 11P+15CuSO4+24H2O=5Cu3P+6H3PO4+15H2SO4中,①被氧化的P和被还原的P的物质的量之比为 ;
②当有8 molH2O参加反应,上述反应转移的电子数目约为 个;
③上述反应中7.5 mol CuSO4氧化的P原子的物质的量为 。
(1)在一定条件下可以进行如下反应:H2O +R2O8n-+Mn2+→MnO4-+RO42-+ H+ (未配平),又知该反应中氧化剂与还原剂的物质的量之比为5:2,则R2O8n-中n的值为 。
(2)反应 2KMnO4 + 16HCl =" 2KCl" + 2MnCl2 + 5Cl2↑ + 8H2O 可用于实验室制取氯气
①用双线桥表示出该反应的电子转移情况:
2KMnO4 + 16HCl =" 2KCl" + 2MnCl2+ 5Cl2↑+ 8H2O
②在标准状况下,该反应产生2.24 L Cl2时,消耗氧化剂 mol,被氧化的物质的质量为 g。
亚运会上使用的发令枪所用的“火药”成分是氯酸钾和红磷,经撞击发出响声,同时产生白色烟雾。撞击时发生反应的化学方程式为:5KClO3+6P="3" P2O5+5KCl,则下列有关叙述错误的是
| A.上述反应中Cl的化合价由+5价变为-1价 |
| B.P2O5是P被还原后所得的产物 |
| C.该反应氧化剂与还原剂物质的量之比为5 : 6 |
| D.上述反应中消耗3 mol P时,转移电子的物质的量为15 mol |
对于反应KMnO4+ HCl——KC1+ MnCl2+Cl2+ H2O(未配平),若有0.1 mol KMnO4参加反应,下列说法不正确的是
| A.被氧化的HCl为0.5 mol | B.生成0.5 mol Cl2 |
| C.参加反应的HC1为0.8 mol | D.HCl体现了酸性和还原性 |
有下列反应:2KMnO4 + 5K2SO3 + 3H2SO4══ 6K2SO4 + 2MnSO4 + 3H2O ,在反应中还原产物和氧化产物的物质的量之比为
| A.1∶4 | B.1∶3 | C.2∶5 | D.3∶2 |
在反应KClO3 + 6HCl="=" KCl +3Cl2↑+3H2O中,被氧化与被还原的氯原子个数比为( )
| A.1:6 | B.6:1 | C.1:5 | D.5:1 |
已知:还原性HSO3¯>I¯,氧化性IO3¯> I2 。在含3 mol NaHSO3的溶液中逐滴加入KIO3溶液。加入KIO3和析出I2的物质的量的关系曲线如右图所示。
下列说法正确的是

| A.反应过程中的氧化产物均为SO3 |
| B.a点时剩余NaHSO3的物质的量为1.2 mol |
| C.b点时的还原产物可能是KI或NaI |
| D.当溶液中I¯与I2的物质的量之比为1:1时,加入的KIO3为9/8mol |
(1)写出 CO与氧化铜反应的化学方程式并标明电子转移的方向和数目
(2)2.8gCO的物质的量为 mol,含有 个原子,完全与氧化铜反应时失去电子 mol。
在反应8NH3 + 3Cl2 = 6NH4Cl + N2中,被氧化的氨和末被氧化的氨的质量之比为
| A.1:3 | B.3:1 | C.1:1 | D.3:8 |
氧化还原反应有多种分类方法,其中根据参与电子转移的元素种类不同的分类方法最常见。下列反应中电子转移发生在相同价态的同种元素之间的有________(填反应编号,下同);电子转移发生在不同价态的同种元素之间的有________;电子转移发生在不同元素之间的有__________。下列反应中转移电子数为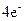 的有_____________。
的有_____________。
①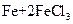 ===
===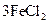
 ②
②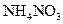

 ③
③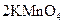
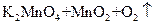
 ④
④
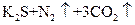
⑤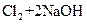 ===
===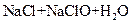
 ⑥
⑥