硫代硫酸钠(Na2S2O3)可作为还原剂,已知25.0mL0.0100mol/LNa2S2O3溶液恰好把22.4mL(标准状况下)Cl2完全转化为Cl 离子, 则S2O32- 将转化成( )
离子, 则S2O32- 将转化成( )
| A.S2- | B.S | C.SO32- | D.SO42- |
一定条件下硝酸铵受热分解的化学反应方程式为:5NH4NO3 = 2HNO3 + 4N2 + 9H2O,在反应中被还原与被氧化的氮原子数之比为
| A.5:3 | B.4:5 | C.5:4 | D.3:5 |
工业上制取金刚砂的化学方程式如下:SiO2+3C=SiC+2CO↑。在这个氧化还原反应中,氧化剂和还原剂的物质的量之比为
| A.1︰2 | B.2︰1 | C.5︰3 | D.3︰5 |
24 mL浓度为0.05 mo1/L的Na2SO3溶液恰好与20 mL浓度为0.02 mol/L的K2Cr2O7溶液完全反应。已知Na2SO3被K2Cr2O7氧化为Na2SO4,则元素Cr在还原产物中的化合价为 ( )
| A.+2 | B.+3 | C.+4 | D.+5 |
某容器中发生一个化学反应,反应过程中存在H2O、ClO﹣、CN﹣、HCO3﹣、N2、Cl﹣六种离子。在反应过程中测得ClO﹣和N2的物质的量随时间变化的曲线如图所示.下列有关判断中不正确的是
| A.还原剂是含CN﹣的物质,氧化产物不只有N2 |
| B.氧化剂是ClO﹣,还原产物是HCO3﹣ |
| C.参与反应的氧化剂与还原剂的物质的量之比为5:2 |
| D.标准状况下若生成2.24LN2则转移电子1mol |
实验研究发现,硝酸发生氧化还原反应时,硝酸的浓度越稀,对应还原产物中氮元素的化合价越低。现有一定量的铝粉和铁粉的混合物与一定量很稀的硝酸充分反应,反应过程中无气体放出。在反应结束后的溶液中逐滴加入5mol/L NaOH溶液,所加的NaOH溶液的体积(mL)与产生沉淀的物质的量(mol)关系如图所示,下列说法不正确的是( )

| A.稀硝酸与铝粉、铁粉反应,其还原产物为硝酸铵 |
| B.图中C点对应溶液体积为48mL |
| C.原硝酸溶液中含硝酸的物质的量为0.5mol |
| D.样品中铝粉和铁粉的物质的量之比5:3 |
向27.2gCu和Cu2O的混合物中加入某浓度的稀硝酸0.5L,固体物质完全反应,生成NO 和Cu(NO3)2。在所得溶液中加入1.0mol/L 的NaOH溶液1.0L,此时溶液呈中性,金属离子已完全沉淀,沉淀质量为39.2g。下列有关说法不正确的是 ( )
| A.Cu与Cu2O 的物质的量之比为2:1 |
| B.硝酸的物质的量浓度为2.6mol/L |
| C.产生的NO在标准状况下的体积为4.48L |
| D.Cu、Cu2O与硝酸反应后剩余HNO3为0.2mol |
现将1mo1Cu2S与144g FeO投入到足量稀硝酸溶液中,充分反应得到Fe(NO3)3、Cu(NO3)2、CuSO4的混合溶液,并产生NO气体。则最终反应所得NO物质的量为
| A.4 mo1 | B.5 mo1 | C.6 mo1 | D.7 mo1 |
已知酸性K2Cr2O7溶液可与FeSO4反应生成Fe3+和Cr3+。现将硫酸酸化的K2Cr2O7溶液与FeSO4溶液混合,充分反应后再向所得溶液中加入KI溶液,混合溶液中Fe3+的物质的量随加入的KI的物质的量的变化关系如下图所示,下列说法中不正确的是( )

| A.图中AB段的氧化剂为K2Cr2O7 |
| B.图中BC段发生的反应为2Fe3++2I-=2Fe2++I2 |
| C.开始加入的K2Cr2O7为0.25mol |
| D.开始加入的K2Cr2O7与FeSO4的物质的量比为1:3 |
已知RxO42-+MnO4-+H+→RO2+Mn2++H2O变化过程中,0.2molRxO42-参加反应,共转移0.4mol电子,则x为()
| A.2 | B.3 | C.4 | D.5 |
等物质的量的下列化合物与足量浓盐酸反应,得到氯气物质的量最多的是
己知:MnO4-+H++Cl-→Mn2++C12↑+H2O(未配平)
C1O3-+H++Cl-→C12↑+H2O(末配平)
ClO-+H++Cl-→C12↑+H2O(未配平)
| A.KC1O3 | B.KMnO4 | C.MnO2 | D.Ca(C1O)2 |
若NA表示阿伏伽德罗常数,下列说法正确的是
| A.0.lmol氯气与铁反应,转移0.2NA电子 |
| B.0.lmol过氧化钠与水反应,转移0.2NA电子 |
| C.0.lmol铁与高温水蒸汽反应,转移0.3NA电子 |
| D.0.lmol二氧化锰与足量浓盐酸反应,有0.4NACl-被氧化 |
水热法制备Fe3O4纳米颗粒的反应为:
3Fe2++2S2O32-+O2+xOH-===Fe3O4+S4O62-+2H2O,下列说法中错误的是
| A.每生成1 mol Fe3O4,反应转移的电子总数为4 mol |
| B.Fe2+和S2O32-都是还原剂 |
C.1 mol Fe2+被氧化时,被Fe2+还原的O2的物质的量为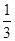 mol mol |
| D.x=4 |
心脏起搏器一般是给心跳缓慢的病人使用。某种类型的心脏起搏器工作时发生下列反应:4Li+2SOC12=4LiC1+S+SO2,下列有关判断正确的是
| A.还原剂只有锂 |
| B.SOC12中每个原子都达到8电子稳定结构 |
| C.氧化产物包括LiCl和SO2 |
| D.生成1. 12 LSO2时,反应转移电子为0.2 mol |