还原2.4×10-3 mol [XO(OH)3]+ 到X元素的低价态时,消耗0.2mol·L—1的Na2SO3溶液30 mL,则X元素反应后的价态是 ( )
| A.+1 | B.-1 | C.0 | D.-2 |
将足量的铜屑加入到100 mL浓度均为2 mol·L-1的HNO3和H2SO4的混合溶液中,充分反应后,转移电子的物质的量为 ( )
| A.0.6 mol | B.0.8 mol | C.0.45 mol | D.0.4 mol |
Na2FeO4是一种高效多功能水处理剂,应用前景十分看好。一种制备Na2FeO4的方法可用化学方程式表示如下:2FeSO4+6Na2O2=2Na2FeO4+2Na2O+2Na2SO4+O2↑,对此反应下列说法中正确的是
| A.Na2O2只作氧化剂 |
| B.Na2FeO4既是氧化产物又是还原产物 |
| C.O2是还原产物 |
| D.2 mol FeSO4发生反应时,反应中共有8 mol电子转移 |
乙二酸可以被强氧化剂氧化为CO2,现有0.10mol/L乙二酸溶液20mL,恰好被4×10-3molVO2+ 所氧化,则此反应的还原产物VOn+中n的值为( )
| A.5 | B.4 | C.3 | D.2 |
现有等物质的量的铜和银的混合物17.2克,与50.0mL的浓硝酸恰好完全反应,产生气体4.48L(标准状况),则下列说法正确的是
| A.产生的气体是0.2molNO2 |
| B.硝酸的物质的量浓度为12mol/L |
| C.反应中被还原和未被还原的硝酸物质的量之比为3:2 |
| D.要使产生的气体恰好完全被水吸收需要通入氧气0.075mol |
3.16 g KMnO4与50mL 12 mol·L-1过量浓盐酸完全反应(假设浓盐酸无挥发),化学方程式如下:2KMnO4+16HCl=2KCl+2MnCl 2+ 5Cl2↑+8H2O, 通过计算回答:
(1)未被氧化的HCl的物质的量是 ;
(2)产生的Cl2在标准状况下的体积为多少升?
(3)在反应后的溶液中加足量的AgNO3溶液可生成多少克沉淀?
含有a mol FeBr2的溶液中,通入x mol Cl2。下列各项为通Cl2过程中,溶液内发生反应的离子方程式,其中不正确的是
| A.x=0.4a,2Fe2++Cl2=2Fe3++2Cl- |
| B.x=0.6a,2Br-+ Cl2=Br2+2Cl- |
| C.x=a,2Fe2++2Br-+2Cl2=Br2+2Fe3++4Cl- |
| D.x=1.5a,2Fe2++4Br-+3Cl2=2Br2+2Fe3++6Cl- |
在热的稀硫酸溶液中溶解了45.6gFeSO4。当加入200mL0.5mol•L-1KNO3溶液后,使其中的Fe2+全部转化成Fe3+,KNO3溶液也完全反应,并有NxOy气体逸出,则该NxOy是
| A.N2O | B.NO | C.N2O3 | D.NO2 |
亚硝酸(HNO2)参加反应时,既可作氧化剂,也可作还原剂。当它作还原剂时,可能生成的产物是
| A.NH3 | B.N2 | C.N2O3 | D.HNO3 |
a mol FeS与b mol FeO投入到V L、c mol·L-1的稀硝酸溶液中充分反应,产生NO气体,所得澄清溶液的成分可看作是Fe(NO3)3、H2SO4的混合液,则反应中未被还原的硝酸可能为( )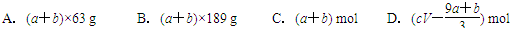
一定条件下硝酸铵受热分解的化学方程式为:5NH4NO3=2HNO3+4N2+9H2O,在反应中被氧化与被还原的氮原子数之比为 ( )
| A.5∶3 | B.5∶4 | C.1∶1 | D.3∶5 |
已知硫化亚铜与一定浓度的硝酸共热,所得溶液中只有硝酸铜和硫酸铜,放出一氧化氮和二氧化氮两种气体,且两种气体的物质的量之比为3:7,则参加反应的硫化亚铜和作氧化剂的硝酸的物质的量之比为
| A.4:25 | B.2:17 | C.1:7 | D.3:8 |
实验室常利用以下反应制取少量氮气:NaNO2+NH4Cl=NaCl+N2↑+2H2O关于该反应的下列说法正确的是( )
| A.NaNO2是氧化剂 |
| B.N2既是氧化剂,又是还原剂 |
| C.NH4Cl中的氮元素被还原 |
| D.每生成1mol N2时,转移电子的物质的量为6mol |
6.4 g铜跟60 mL 8mol/L的硝酸充分反应,硝酸的还原产物有NO、NO2。铜完全溶解后,测得溶液中H+的物质的量为n mol,此时溶液中所含NO3-的物质的量为 ( )
| A.(n+0.2) mol | B.(n+0.4) mol | C.0.28 mol | D.0.31 mol |