浙江省“温州八校”高三返校联考化学试卷
化学与科学、技术、社会、环境密切相关。下列有关说法中不正确的是
| A.工业上,用焦炭在电炉中还原二氧化硅得到含杂质的粗硅 |
| B.煤经过气化和液化两个物理变化,可变为清洁能源 |
| C.如将纳米材料分散到液体分散剂中,该分散系可发生丁达尔现象,由此可推测纳米材料的直径为1~100 nm之间 |
| D.将苦卤浓缩、氧化,鼓入热空气或水蒸气提取海水中的溴 |
化学教材中,常借助于图像,这一表现手段清晰地突出实验装置的要点、形象地阐述化学过程
的原理。下列有关化学图像表现的内容正确的是
Na2FeO4是一种高效多功能水处理剂,应用前景十分看好。一种制备Na2FeO4的方法可用化学方程式表示如下:2FeSO4+6Na2O2=2Na2FeO4+2Na2O+2Na2SO4+O2↑,对此反应下列说法中正确的是
| A.Na2O2只作氧化剂 |
| B.Na2FeO4既是氧化产物又是还原产物 |
| C.O2是还原产物 |
| D.2 mol FeSO4发生反应时,反应中共有8 mol电子转移 |
在三个密闭容器中分别充入Ne、H2、O2三种气体,当它们的温度和密度都相同时,这三种气体的压强(p)从小到大的是
| A.p (Ne) < p (H2) < p (O2) | B.p (O2) < p (Ne) < p (H2) |
| C.p (H2) < p (O2) < p (Ne) | D.p (H2) < p (Ne) < p (O2) |
设NA表示阿伏加德罗常数的值,下列说法正确的是
| A.通常状况下,3.36升氯气与2.7克铝充分反应转移的电子数小于0.3NA |
| B.100g 98%的浓硫酸溶液中含氧原子个数为4NA |
| C.1mol二氧化硅晶体中含有2NA个硅氧键 |
| D.0.1L 3mol·L-1的NH4NO3溶液中含有的NH4+数目为0.3NA |
SO2通入足量Fe(NO3)3稀溶液中,溶液由棕色变为浅绿色,但立即又变为棕黄色,这时若滴入BaCl2溶液,会产生白色沉淀。针对上述一系列变化过程中,下列说法中不正确的是
| A.上述过程中,最终被还原的是NO3-- |
| B.从上述过程中可以得出结论,氧化性:HNO3>Fe3+>稀H2SO4 |
| C.上述过程中,会产生一种无色无味的难溶于水的气体 |
| D.假设通入的SO2完全反应,则同温同压下,SO2和逸出气体的体积为1∶1 |
“暖冰”是韩国首尔大学科学家将水置于一个足够强的电场中,在20℃时,水分子瞬间凝固形成的。某老师在课堂上做了一个如右图所示的实验,发现烧杯中酸性KMnO4溶液褪色。若将烧杯中的溶液换成含有少量KSCN 的FeCl2溶液,则溶液呈血红色。则下列说法中不正确的是
| A.在电场作用下,水分子间更易形成氢键,因而可以制得“暖冰” |
| B.水凝固形成20℃时的“暖冰”所发生的变化是化学变化 |
| C.该条件下H2燃烧生成了既具有氧化性又具有还原性的物质 |
| D.该条件下H2燃烧的产物中可能含有一定量的H2O2 |
固体粉末X中可能含有Fe、FeO、CuO、MnO2、KCl和K2CO3中的若干种。为确定该固体粉末的成分,某同学依次进行了以下实验:
①将X加入足量水中,得到不溶物Y和溶液Z
②取少量Y加入足量浓盐酸,加热,产生黄绿色气体,并有少量红色不溶物
③向Z溶液中滴加AgNO3溶液,生成白色沉淀
④用玻璃棒蘸取溶液Z于广泛pH试纸上,试纸呈蓝色 分析以上实验现象,下列结论正确的是
| A.X中一定不存在FeO | B.不溶物Y中一定含有Fe和CuO |
| C.Z溶液中一定含有KCl、K2CO3 | D.Y中不一定存在MnO2 |
部分氧化的FeCu合金样品(氧化产物为Fe2O3、CuO)共5.76 g,经如下处理:
下列说法正确的是
| A.滤液A中的阳离子为Fe2+、Fe3+、H+ | B.样品中CuO的质量为4.0 g |
| C.V=448 | D.原样品中Fe元素的质量分数为41% |
短周期元素X、Y、Z、W的原子序数依次增大,且原子最外层电子数之和为13。X的原子半径比Y的小,X与W同主族,Z是地壳中含量最高的元素。下列说法正确的是
| A.原子半径的大小顺序:r(Y)>r(Z)>r(W) |
| B.元素Z、W的简单离子的电子层结构不同 |
| C.元素Y的简单气态氢化物的热稳定性比Z的强 |
| D.只含X、Y、Z三种元素的化合物,可能是离子化合物,也可能是共价化合物 |
如图是四种常见有机物的比例模型示意图。下列说法正确的是
| A.甲能使酸性KMnO4溶液褪色 |
| B.乙可与溴水发生取代反应而使溴水褪色 |
| C.丙中的碳碳键是介于碳碳单键和碳碳双键之间的独特键 |
| D.丁在稀硫酸作用下可与乙酸发生取代反应 |
一定体积的某气态烃与过量氧气的混合物充分反应后恢复到原温度、压强(标准状况),混合气体体积缩小了二分之一。下列四种气态烃中,符合条件的是
| A.乙烷 | B.乙烯 | C.乙炔 | D.丙烷 |
室温下,将1mol的CuSO4·5H2O(s)溶于水会使溶液温度降低,热效应为ΔH1,将1mol的CuSO4(s)溶于水会使溶液温度升高,热效应为ΔH2;CuSO4·5H2O受热分解的化学方程式为:CuSO4·5H2O(s) CuSO4 (s) +5H2O(l),热效应为ΔH3。则下列判断正确的是
CuSO4 (s) +5H2O(l),热效应为ΔH3。则下列判断正确的是
| A.ΔH2>ΔH3 | B.ΔH1<ΔH3 | C.ΔH1+ΔH3=ΔH2 | D.ΔH1+ΔH2=ΔH3 |
下图Ⅰ、Ⅱ分别是甲、乙两组同学将反应“AsO +2I-+2H+
+2I-+2H+ AsO
AsO +I2+H2O”设计成的原电池装置,其中C1、C2均为碳棒。甲组向图Ⅰ烧杯中逐滴加入适量浓盐酸;乙组向图ⅡB烧杯中逐滴加入适量40% NaOH溶液。下列叙述中正确的是
+I2+H2O”设计成的原电池装置,其中C1、C2均为碳棒。甲组向图Ⅰ烧杯中逐滴加入适量浓盐酸;乙组向图ⅡB烧杯中逐滴加入适量40% NaOH溶液。下列叙述中正确的是
| A.甲组操作时,电流计(G)指针发生偏转 |
| B.甲组操作时,溶液颜色变浅 |
| C.乙组操作时,C2做正极 |
| D.乙组操作时,C1上发生的电极反应为 |
I2+2e-===2I-
某兴趣小组以废弃的易拉罐、漂白粉、氢氧化钠等为原料制造了一种新型环保电池,并进行相关实验,如图所示。电池的总反应方程式为2Al+3ClO-+2OH-===3Cl-+2AlO +H2O。下列说法正确的是
+H2O。下列说法正确的是
| A.电池的负极反应式为:ClO-+H2O+2e-===Cl-+2OH- |
| B.当有0.1 mol Al完全溶解时,流经电解液的电子数为1.806×1023个 |
| C.往滤纸上滴加酚酞试液,b极附近颜色变红 |
| D.b极附近会生成蓝色固体 |
在平衡体系:CaCO3(s)  CaO(s) + CO2中仅含有碳酸钙、氧化钙及二氧化碳气体。原压强为P,体积为V,在t0时刻,将容器体积缩小为原来的一半并保持不变。若固体所占体积可忽略,且温度维持不变,则此体系中压强(P 纵坐标)跟时间(t 横坐标)的关系为
CaO(s) + CO2中仅含有碳酸钙、氧化钙及二氧化碳气体。原压强为P,体积为V,在t0时刻,将容器体积缩小为原来的一半并保持不变。若固体所占体积可忽略,且温度维持不变,则此体系中压强(P 纵坐标)跟时间(t 横坐标)的关系为
一定条件下,0.3 mol X(g)与0.3 mol Y(g)在体积为1L的密闭容器中发生反应:
X(g)+3Y(g) 2Z(g),下列示意图合理的是
2Z(g),下列示意图合理的是 
某密闭容器中充入等物质的量的A和B,一定温度下发生反应A(g)+xB(g)  2C(g),达到平衡后,在不同的时间段,下列说法中正确的是
2C(g),达到平衡后,在不同的时间段,下列说法中正确的是
| A.30~40 min间该反应使用了催化剂 |
| B.化学方程式中的x=1,正反应为吸热反应 |
| C.30 min时降低温度,40 min时升高温度 |
| D.8 min前A的平均反应速率为0.08 mol·L-1·min-1 |
在1100 ℃,一定容积的密闭容器中发生反应:FeO(s)+CO(g)  Fe(s)+CO2(g) ΔH=a kJ/mol(a>0),该温度下K=0.263,下列有关该反应的说法正确的是
Fe(s)+CO2(g) ΔH=a kJ/mol(a>0),该温度下K=0.263,下列有关该反应的说法正确的是
| A.若生成1 mol Fe,则吸收的热量小于a kJ |
| B.若升高温度,正反应速率加快,逆反应速率减慢,则化学平衡正向移动 |
| C.若容器内压强不随时间变化,则可以判断该反应已达到化学平衡状态 |
| D.达到化学平衡状态时,若c(CO)=0.100 mol/L,则c(CO2)=0.0263 mol/L |
人体血液内的血红蛋白(Hb)易与O2结合生成HbO2,因此具有输氧能力,CO吸入肺中发生反应:CO+HbO2 O2+HbCO,37 ℃时,该反应的平衡常数K=220。HbCO的浓度达到HbO2浓度的0.02倍,会使人智力受损。据此,下列结论错误的是
O2+HbCO,37 ℃时,该反应的平衡常数K=220。HbCO的浓度达到HbO2浓度的0.02倍,会使人智力受损。据此,下列结论错误的是
A.CO与HbO2反应的平衡常数K= |
| B.人体吸入的CO越多,与血红蛋白结合的O2越少 |
| C.当吸入的CO与O2浓度之比大于或等于0.02时,人的智力才会受损 |
| D.把CO中毒的病人放入高压氧仓中解毒,其原理是使上述平衡向左移动 |
关于可逆反应:aA(g)+bB(g)  cC(g)+dD(g) ΔH的有关图像如下:
cC(g)+dD(g) ΔH的有关图像如下:
则下列不正确的是
| A.p1<p2 T1>T2 |
| B.减小压强,正逆反应速率都减小,平衡右移 |
| C.ΔH>0 ΔS>0 |
| D.升高温度,混合气体的平均摩尔质量增大 |
电导率可用于衡量电解质溶液导电能力的大小,且电导率越大溶液的导电能力越强。室温下 ,用0.l00 mol·L-1的NH3· H2O 滴定10 .00mL 浓度均为0 . 100 mol·L-1HCl和CH3COOH的混合液,电导率曲线如图所示。下列说法正确的是
| A.① 溶液中c(H +)为0 . 200 mol·L-1 |
| B.溶液温度高低为① >③ >② |
| C.③ 点后因离子数目减少使电导率略降低 |
| D.③ 点时溶液中有c ( C1一)>(CH3 COO一) |
下列溶液中各微粒的浓度关系正确的是
A.室温下,pH=7的醋酸和醋酸钠的混合溶液中:c(CH3COO-)>c(Na+)
B.将10 mL 0.l mol·L-1 Na2CO3溶液逐滴滴加到10 mL 0.l mol·L-1盐酸中:
c(Na+) >c(Cl-) >c(HCO3-) >c(CO32-)
C.等pH的氨水、KOH溶液、Ba(OH)2溶液中:c(NH4+) = c(K+) = c(Ba2+)
D.0.2 mol·L-1的某一元弱酸HA溶液和0.l mol·L-1NaOH溶液等体积混合后的溶液:
2c(OH-) + c(A-) = 2c(H+) + c(HA)
常温下,用 0.10 mol·L-1 NaOH溶液分别滴定20.00 mL 0.10 mol·L-1 HCl溶液和20.00 mL 0.10 mol·L-1 CH3COOH溶液,得到2条滴定曲线,如下图所示,则下列说法正确的是
| A.图2是滴定盐酸的曲线 |
| B.a与b的关系是:a<b |
| C.E点对应离子浓度由大到小的顺序为: c(CH3COO-)>c(Na+)>c(H+)>c(OH-) |
| D.这两次滴定都可以用甲基橙作为指示剂且颜色变化为红变橙 |
雾霾严重影响人们的生活与健康。某地区的雾霾中可能含有如下可溶性无机离子:Na+、NH4+、Mg2+、Al3+、SO42-、NO3-、Cl- 。某同学收集了该地区的雾霾,经必要的预处理后试样溶液,设计并完成了如下的实验: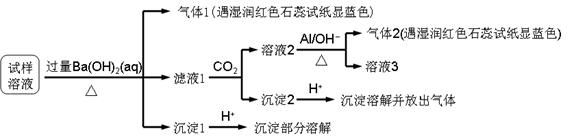
已知:3NO3- + 8Al + 5OH- + 2H2O  3NH3 + 8AlO2-
3NH3 + 8AlO2-
根据以上的实验操作与现象,该同学得出的结论不正确的是
| A.试样中肯定存在NH4+、Mg2+、SO42-和NO3- | B.试样中一定不含Al3+ |
| C.试样中可能存在Na+、Cl- | D.该雾霾中可能存在NaNO3、NH4Cl和MgSO4 |
现有A、B、C、D四种短周期元素,它们之间的关系如下:
Ⅰ.原子半径:A < C < B < D Ⅱ.原子的最外层电子数:A + C =" B" + D = 8
Ⅲ.原子的核外电子层数:B =" C" = 2A Ⅳ.B元素的主要化合价:最高正价 + 最低负价 = 2
请回答:
(1)由A、B两种元素组成的常见气体,其电子式为 ;只有A和B两种元素组成的属于离子晶体的化合物可能为 (用化学式表示)。
(2)由D元素形成的氢氧化物,与强碱溶液反应的离子方程式为 。
(3)由B、C元素组成的化合物BC3,该化合物具有强氧化性,与水反应生成两种酸和一种无色气体,该气体常温下遇空气变红棕色,写出该化合物与水反应的化学方程式 。
(4)由A、B和C三种元素组成的盐,常温下其水溶液显酸性,则0.1 mol·L-1该盐溶液中浓度最大的离子为 (写离子符号)。
(5)由A、B、C和D四种元素组成的配位化合物己,写出己的化学式 ;写出检验化合物己中所含阳离子的实验方法 。
某制糖厂以甘蔗为原料制糖,同时得到大量的甘蔗渣,对甘蔗渣进行综合利用,不仅可以提高经济效益,而且还可防止环境污染。现按下列方式进行综合利用: 
按要求完成问题:
(1)C的官能团名称: ,D的结构简式: ;
(2)写出化学方程式(有机物用结构简式表示):E→F: ,H→I ;
(3)写出下列转化的反应类型:E→G: ,E→H: ;
(4)已知X是B的同分异构体,且满足下列三个条件:
①X为六元环状化合物,含有母体:
②X的母体: 上四个碳原子各连接1个支链或取代基。
上四个碳原子各连接1个支链或取代基。
③l mol X与足量的金属钠反应放出2molH2。
则符合上述条件的X的结构简式共有 种(选填A、B、C、D)。
A.3 B.4 C.5 D.6
淀粉水解的产物(C6H12O6)用硝酸氧化可以制备草酸,装置如图所示(加热、搅拌和仪器固定装置均已略去):实验过程如下:①将1∶1的淀粉水乳液与少许硫酸(98%)加入烧杯中,水浴加热至85℃~90℃,保持30 min,然后逐渐将温度降至60℃左右;②将一定量的淀粉水解液加入三颈烧瓶中;③控制反应液温度在55~60℃条件下,边搅拌边缓慢滴加一定量含有适量催化剂的混酸(65%HNO3、98%H2SO4的质量比为2:1.5)溶液;④反应3h左右,冷却,过滤后再重结晶得草酸晶体。
硝酸氧化淀粉水解液过程中可发生下列反应:
C6H12O6+12HNO3→3H2C2O4+9NO2↑+3NO↑+9H2O
C6H12O6+8HNO3→6CO2+8NO↑+10H2O
3H2C2O4+2HNO3→6CO2+2NO↑+4H2O
请回答下列问题:
(1)实验①加入98%硫酸少许的目的是: 。
(2)冷凝水从a口进入,但实验中若混酸滴加过快,将导致草酸产量下降,其原因是 。
(3)检验淀粉是否水解完全所用的试剂为 。
(4) 当尾气中n(NO2):n(NO)=1:1时,过量的NaOH溶液能将NOx全部吸收,发生的化学反应方程式为: 。
(5) 将产品在恒温箱内约90℃以下烘干至恒重,得到二水合草酸。用KMnO4标准溶液滴定,该反应的离子方程式为:2MnO4- + 5H2C2O4 + 6H+ = 2Mn2+ + 10CO2↑+ 8H2O
称取该样品0.12 g,加适量水完全溶解,然后用0.020 mol·L-1的酸性KMnO4溶液滴定至终点(杂质不参与反应),此时滴定终点的现象为 。滴定前后滴定管中的液面读数如图所示,则该草酸晶体样品中二水合草酸的质量分数为 。
Ⅰ、向Cu、Cu2O和CuO组成的混合物中,加入1 L 0.6 mol·L -1HNO3溶液恰好使混合物溶解,同时收集到2240 mL NO气体(标准状况)。(已知:Cu2O+2H+=Cu+Cu2++H2O)
(1)Cu2O跟稀硝酸反应的离子方程式 。
(2)若将上述混合物用足量的H2加热还原,所得到固体的质量为 g。
(3)若混合物中含0.1 mol Cu,将该混合物与稀硫酸充分反应,至少消耗H2SO4的物质的量为 。
Ⅱ、一定温度下,向一容积为5 L的恒容密闭容器中充入0.4 mol SO2和0.2 mol O2,发生反应:2SO2(g)+O2(g)  2SO3(g)。当反应达到平衡时,容器内压强变为起始时的0.7倍。
2SO3(g)。当反应达到平衡时,容器内压强变为起始时的0.7倍。
请回答下列问题:
(4)判断该反应达到化学平衡状态的标志是 (填字母)。
| A.SO2、O2、SO3三者的浓度之比为2∶1∶2 | B.容器内气体的压强不变 |
| C.容器内混合气体的密度保持不变 | D.SO3的物质的量不再变化 |
E.SO2的生成速率和SO3的生成速率相等
(5) SO2的转化率 。
 粤公网安备 44130202000953号
粤公网安备 44130202000953号