已知Cu2S与一定浓度的HNO3可发生以下反应: 3Cu2S+26HNO3=3CuSO4+3Cu(NO3)2+15NO2↑+5 NO↑+13H2O 下列说法正确的是( )
| A.Cu2S既是还原剂,又是氧化剂 | B.3mol Cu2S发生反应,有24mol电子转移 |
| C.产物中只有CuSO4是氧化产物 | D.参加反应的HNO3中有10/13氧化剂 |
金属钛(Ti)性能优越,被称为继铁、铝制后的“第三金属”。工业上以金红石为原料制取Ti的反应为:aTiO2 + bCl2 + cC 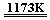 aTiCl4 + cCO 反应①
aTiCl4 + cCO 反应①
TiCl4 +2Mg 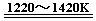 Ti + 2MgCl2 反应②
Ti + 2MgCl2 反应②
关于反应①、②的分析不正确的是
① TiCl4在反应①中是还原产物,在反应②中是氧化剂;② C、Mg在反应中均为还原剂,被还原;③在反应①、②中Mg的还原性大于C,C的还原性大于TiCl4;④a=1,b=c=2;⑤每生成19.6 g Ti,反应①、②中共转移4.8 mol e-。 (Ti 相对原子质量49)
A.①②④ B.②③④ C.③④ D.②⑤
实验室用Na2SO3还原MnO4-,如果还原含有2.4×10-3 mol MnO4-的溶液时,消耗30 mL0.2 mol•L-1的Na2SO3溶液,则Mn元素在还原产物中化合价为( )
| A.+1 | B.+2 | C.+4 | D.+5 |
在反应8NH3 + 3Cl2= 6NH4Cl + N2中,被氧化的氨与未被氧化的氨的物质的量之比为:( )
| A.8∶3 | B.6∶1 | C.3∶1 | D.1∶3 |
在反应3Cu2S+22HNO3=6Cu(NO3)2+3H2SO4+10NO↑+8H2O中,1mol还原剂失去电子的物质的量为: ( )
| A.6mol | B.8mol | C.10mol | D.12mol |
氧化还原反应中实际上包含氧化和还原两个过程。下面是一个还原过程的反应式:NO3-+4H++3e-=NO+2H2O ;
KMnO4、Na2CO3、Cu2O、Fe2(SO4)3四种物质中的一种物质(甲)能使上述还原过程发生。
(1)写出并配平该氧化还原反应的方程式:
(2)反应中硝酸体现了 、 性质。
(3)反应中若产生0.2mol气体,则转移电子的物质的量是 mol。
(4)若1mol甲与某浓度硝酸反应时,被还原硝酸的物质的量增加,原因是:
(5)KMnO4在酸性溶液中发生还原反应的反应式:
在反应11P+15CuSO4+24H2O=5Cu3P+6H3PO4+15H2SO4中,每摩尔CuSO4能氧化P的物质的量为
| A.1/5 mol | B.2/5 mol | C.3/5mol | D.11/5 mol |
将n molCu2S的与足量的稀硝酸反应,生成硝酸铜、硫酸、一氧化氮和水,则参加反应的硝酸中被还原的硝酸的物质的量是
| A.4n mol | B.10n mol | C.10n/3 mol | D.2n/3 mol |
有一混合溶液,其中只含有Fe2+、Cl-、Br-、I- (忽略水的电离),其中Cl-、Br-、I-的个数比为
(忽略水的电离),其中Cl-、Br-、I-的个数比为 2∶3∶4,向该溶液中通入氯气,使溶液中Cl-和Br-的个数比为3∶1,求通入氯气的物质的量与溶液中剩余的Fe2+的物质的量之比。(已知:还原
2∶3∶4,向该溶液中通入氯气,使溶液中Cl-和Br-的个数比为3∶1,求通入氯气的物质的量与溶液中剩余的Fe2+的物质的量之比。(已知:还原 性I->Fe2+>Br->Cl-)
性I->Fe2+>Br->Cl-)
在反应3BrF3 + 5H2O = HBrO3 + Br2 +9HF + O2↑中,若有5molH2O做还原剂,被水还原的BrF3的物质的量为( )
| A.3mol | B.10/3mol | C.7.5mol | D.无法计算 |
a mol  FeS与b mol FeO投入到V L、c mol·L-1的硝酸溶液中充分反应,产生NO气体,所得澄清溶液成分可看作是Fe(NO3)3、H2SO4的混合液,则反应中未被还原的硝酸可能为( )
FeS与b mol FeO投入到V L、c mol·L-1的硝酸溶液中充分反应,产生NO气体,所得澄清溶液成分可看作是Fe(NO3)3、H2SO4的混合液,则反应中未被还原的硝酸可能为( )
①(a+b)×63 g ②(a+b)×189 g ③(a+b)mol ④(Vc- )mol
)mol
| A.①④ | B.②③ | C.①③ | D.②④ |
已知在酸性溶液中,下列物质氧化KI时,自身发生如下变化:
Fe3+→Fe2+ ; MnO4-→Mn2+ ; IO3-→I2;HNO2→NO。
如果分别用等物质的量的这些物质氧化足量的KI,得到I2最多的是
| A.Fe3+ | B.MnO4- | C.IO3- | D.HNO2 |
对于反应:2H2S+SO2===3S+2H2O,被氧化的硫原子与被还原的硫原子的质量之比为
| A.1:1 | B.2:1 | C.3:1 | D.1:2 |
在3S + 6KOH = 2K2S + K2SO3 + 3H2O反应中,作氧化剂的S原子与作还原剂的S原子的物质的量之比是:
| A.1∶2 | B.2∶1 | C.1∶3 | D.3∶1 |