现有四瓶贴有A、B、C、D标签的溶液,它们可能是K2CO3、Ba(NO3)2、NaHSO4和K2SO4溶液。现进行如下实验,并记录部分现象(如下图):
据此完成下列回答:
(1)写出各物质的化学式
A、 B、
C、 D、
(2)写出下列反应的离子方程式:
A + B反应:
沉淀a+溶液b:
(3)检验物质D中阴离子的方法为 (说明实验操作、现象与结论等)。
(8分) 元素及其化合物的知识是高中化学重要的组成部分,是考查化学基本概念和理论、化学计算、化学实验知识的载体。
(1)元素周期表1-20号元素中,某两种元素的原子序数相差3,周期数相差1。
①这样的两种元素的组合有________种。
②若这样的两种元素形成的化合物中原子数之比为1∶1。
写出其中一种化合物的名称:_____________;
(2)A是自然界存在最广泛的ⅡA族元素,常以化合物F存在.从单质A起始发生的一系列化学反应可由下图表示:
请回答下列问题:
①F的化学式为_______ _,D的电子式为________________。
②E与水反应的化学方程式为_____________________;
③实际生产中,可由F为原料制备单质A,写出制备过程的化学方程式(不需考虑综合经济效益) 。
下列框图涉及到的物质所含元素中,除一种元素外,其余均为1~18号元素。
已知:A、F为无色气体单质,B为具有刺激性气味的气体,C为黑色氧化物,E为红色金属单质(部分反应的产物未列出)。请回答下列问题:
(1)D的化学式为 ;E原子外围电子排布式为 _______
(2)A与B生成D的反应在工业上是生产 的反应原理之一。
(3)E与G的稀溶液反应的离子方程式为 .
(4)B和C反应的化学方程式为 。
(5)J、K是同种金属的不同氯化物,K为白色沉淀。写出SO2还原J生成K的离子方程式
(12分)X、Y、Z是三种常见金属元素的化合物,它们的颜色各不相同,并且都含有一种相同元素。其中X是淡黄色固体,A、D是无色无味气体,G是一种常见金属,F是白色胶状沉淀,W是红褐色沉淀。各物质之间存在下列相互转化关系(部分反应物或产物已略去)。
请用化学用语回答下列问题:
(1)写出X的电子式__________;D的结构式__________。
(2)写出下列反应的化学方程式:
①B+Z→I+Y:_______________________
②D+G→E+H:_______________________
③M→W:_______________________
(3)写出n(X):n(Y)=2:1时与水混合的反应的离子方程式:____________
A、B、C、D均为中学化学常见的物质,它们间的反应关系如下图所示。
(1)若A是可溶性强碱,B是正盐,D不溶于稀硝酸,则B的化学式为 。有关反应的化学变化的化学方程式为 。
(2)若B是正盐,D既可溶于盐酸又可溶于NaOH溶液。
①A是NaHCO3时,该反应的离子方程式为: 。
②A是一种淡黄色固体,且A与B以物质的量之比为2∶1相混合时,推知B的化学式为: 。
(3)若A是碳化钙(CaC2),A与B的溶液反应时只生成气体C、CaCO3和水;则B的化学式为 ;
在一定条件下可实现下图所示物质之间的转化:
请填写下列空白:
(1)孔雀石的主要成分是CuCO3·Cu(OH)2(碱式碳酸铜),受热易分解,图中的F是______(填化学式)。
(2)写出明矾溶液与过量NaOH溶液反应的离子方程式: 。
(3)写出B电解生成E和D的反应方程式: 。
(4)图中所得G和D都为固体,混合后在高温下可发生反应,写出该反应的化学方程式 ,该反应消耗了2 molG,则转移的电子数是 。
下图是部分短周期元素的单质及其化合物的转化关系图(有关反应的条件及生成的H2O已略去),已知:a.A、B、C、D是非金属单质,其中B、C、D在常温常压下是气体。b.反应①②是化工生产中的重要反应。c.化合物E是形成酸雨的污染物之一,化合物K是常用的氮肥。d.化合物L具有漂白性,可由Cl2与NaOH溶液反应制得。e.化合物J由两种元素组成,其相对分子质量为32。
请按要求填空:
(1)A元素在元素周期表中的位置____________________。
(2)反应③的化学方程式:________________________。
(3)C的结构式:_____ ___;
F的一种用途:_________________________。
(4)L的溶液与化合物E反应的离子方程式:_________ 。
(5)化合物J的化学式: ________________________。
在下图所示的物质转化中,A、C均为常见的金属单质,并且在冷的H的浓溶液中均会发生钝化;E为固体非金属单质。B为红色固体氧化物,X为常见无色液体。L溶液的焰色为黄色,且能使酚酞变红(反应过程中生成的水及其他产物已略去)。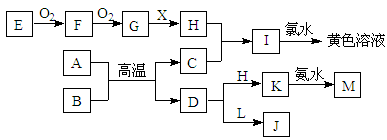
回答以下问题:
(1)H的化学式为 。
(2)L的电子式为 。
(3)A与B反应的化学方程式为 。
(4)K与足量的氨水反应的离子方程式为 。
(8分) 下图的转化关系中,A、C、D是常见的气体单质,D气体在常温下呈黄绿色。F气体极易溶于水,且液态常作制冷剂,B的焰色反应为黄色。图中的部分反应产物或反应物已略去。
(1)写出G的化学式: 。
(2)写出F的电子式: 。
(3)写出D单质和E溶液反应的离子方程式: 。
(4)写出电解B溶液的化学方程式: 。
A、B、C、D四种物质都含有一种共同的元素,A是常见的金属,C的溶液呈现黄色,A、B、C、D之间有如图所示转化关系。
试回答下列问题:
(1)A是___________,C是_________________。
(2)C的溶液与NaOH溶液混合后产生的现象是______________________________。
(3)反应①的反应类型是___________________。
(4)从A、B、C三种物质中任选一种,从它们所含共同元素的价态上预测所选物质具有氧化性或还原性,并设计实验验证。
预测性质___________________________________________
主要操作___________________________________________
可能的现象__________________________________________
短周期元素形成的常见非金属固体单质A与常见金属单质B,在加热条件下反应生成化合物C,C与水反应生成白色沉淀D和臭鸡蛋气味的气体E,氢氧化物D既能溶于强酸,也能溶于强碱。A在空气中燃烧产生刺激性气体G,G在大气中能导致酸雨的形成。请回答下列问题:
(1)组成单质A的元素位于周期表中第 周期第 族。
(2)C与水反应的化学方程式为: 。
(3)G与氯酸钠在酸性溶液中反应可生成消毒剂二氧化氯。
①该反应的离子方程式为 。
②该反应的氧化产物为 。
③当生成2mol二氧化氯时,转移电子 mol。
(4)酸雨在放置过程中pH不断减小,用化学方程式解释其主要原因 。
[6分]物质A~J均由短周期元素组成,并有如下图转化关系,A是常见液体,D、F为组成元素相同的无色气体,B、E、G、H是单质,且E是常见光太阳电池中的半导体材料,G、H呈气态,且H呈黄绿色。
请回答下列问题:
(1)A的电子式为 。
(2)I的化学式为 。
(3)B与C反应的化学方程式为 。
(4)H与氢氧化钠溶液反应的离子方程式为 。
在某澄清、透明的黄色溶液中,可能含有NH4+、Fe3+、Ba2+、Al3+、SO42-、I-、Cl-离子。进行下述实验(所加试剂均过量)。
(1)沉淀 A的化学式是 ,气体A的化学式是 ;
(2)待测液中一定存在 ;一定不存在 ______ 用离子方程式表示上述离子一定不存在的原因 。
(3)写出溶液C与过量氨水反应的离子方程式 。
已知A为淡黄色固体,T、R为两种常见的用途很广的金属单质,D是具有磁性的黑色晶体,C是无色无味的气体,H是白色沉淀,W溶液中加入KSCN出现红色。
(1)写出下列物质的化学式:
A: D: E: N: 。(每空1分)
(2)B与E混和得到H并在潮湿空气中变成M的过程中,可能观察到的现象: ;
(3)按要求写方程式:
B和R反应生成N的离子方程式: ;
M→W的离子方程式: 。
X、Y、Z、W是中学化学中常见的四种气体。已知:X、Y、Z三种气体都能对大气造成污染,在工业上都可以用碱液吸收;X是化石燃料燃烧的产物之一,是形成酸雨的物质;Y是一种单质,通常状况下是黄绿色,它的水溶液具有漂白作用;Z是硝酸工业和汽车尾气中的有害物质之一,能与水反应;W气体的水溶液滴入酚酞变红色。
请回答下列问题:
(1)X、Y两种气体按物质的量之比1:1在水溶液中能发生反应,化学方程式为 。
(2)科学家发现,Z在催化剂条件下能与W反应,反应产物中的单质应是(填化学式) ;该反应是氧化还原反应,则其中的氧化剂是(填化学式) 。
(3)在Z与水的反应中,氧化剂与还原剂的物质的量之比为 。
(4)检验W气体的方法是 。