(8分) 下图的转化关系中,A、C、D是常见的气体单质,D气体在常温下呈黄绿色。F气体极易溶于水,且液态常作制冷剂,B的焰色反应为黄色。图中的部分反应产物或反应物已略去。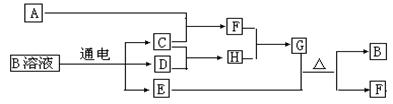
(1)写出G的化学式: 。
(2)写出F的电子式: 。
(3)写出D单质和E溶液反应的离子方程式: 。
(4)写出电解B溶液的化学方程式: 。
(8分) 下图的转化关系中,A、C、D是常见的气体单质,D气体在常温下呈黄绿色。F气体极易溶于水,且液态常作制冷剂,B的焰色反应为黄色。图中的部分反应产物或反应物已略去。
(1)写出G的化学式: 。
(2)写出F的电子式: 。
(3)写出D单质和E溶液反应的离子方程式: 。
(4)写出电解B溶液的化学方程式: 。