辽宁省沈阳郊联体高一下学期期中化学文试卷
一元硬币的外观有银白色的金属光泽,一些同学认为它可能是铁制成的,为证明其想法,有同学拿磁铁来吸引一下。就这一过程而言,属于科学探究中的
| A.实验 | B.假设 | C.观察 | D.做结论 |
在体积为VL的密闭容器中,通入a mol NO和b molO2,反应后容器内氮原子数和氧原子数之比为
A. |
B. |
C. |
D.无法确定 |
区别SO2和CO2气体可选用的方法是
| A.通入澄清石灰水中 | B.通入品红溶液中 |
| C.用带火星的木条检验 | D.通入石蕊溶液中 |
在下列反应中,硫元素表现出还原性的是
| A.稀硫酸与锌粒反应 | B.三氧化硫与水反应 |
| C.浓硫酸与铜反应 | D.二氧化硫与氧气反应 |
氯气是一种重要的工业原料。工业上利用反应在3Cl2+2NH3=N2+6HCl检查氯气管道是否漏气。下列说法错误的是
| A.若管道漏气遇氨就会产生白烟 | B.该反应利用了Cl2的强氧化性 |
| C.该反应属于复分解反应 | D.生成1molN2有6mol电子转移 |
下列酸在与金属发生反应时,其中S或N元素的化合价不会发生变化的是
| A.稀硫酸 | B.浓硫酸 | C.稀硝酸 | D.浓硝酸 |
关于元素周期表的下列叙述,错误的是
| A.元素周期表揭示了化学元素的内在联系,是化学发展史上的重要里程碑之一 |
| B.在周期表中,把电子层数相同的元素排成一横行,称为一周期 |
| C.元素周期表中,总共有18个纵行,18个族 |
| D.第IA族的元素又称为碱金属(除了H),第VIIA族的元素又称为卤素 |
已知某元素的原子序数,则不能推出该元素原子的
| A.质子数 | B.中子数 | C.电子数 | D.核电荷数 |
碳元素有的三种原子: 、
、 、
、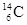 ,下列各项对三种原子均不同的是
,下列各项对三种原子均不同的是
| A.元素种类 | B.核电荷数 | C.电子层数 | D.中子数 |
运用元素周期律分析下面的推断,其中不正确的是
| A.锂(Li)与水反应比钠与水反应剧烈 |
| B.砹(At)为有色固体,AgAt难溶于水也不溶于稀硝酸 |
| C.在氧气中,铷(Rb)的燃烧产物比钠的燃烧产物更复杂 |
| D.HBrO4的酸性比HIO4的酸性强 |
海水淡化是指除去海水中的盐分以获得淡水的工艺过程,其方法较多,如反渗透法、电渗析法、离子交换法等,下列方法中也是用来进行海水淡化的是
| A.过滤法 | B.萃取法 | C.分液法 | D.蒸馏法 |
X、Y、Z、W是中学化学中常见的四种气体。已知:X、Y、Z三种气体都能对大气造成污染,在工业上都可以用碱液吸收;X是化石燃料燃烧的产物之一,是形成酸雨的物质;Y是一种单质,通常状况下是黄绿色,它的水溶液具有漂白作用;Z是硝酸工业和汽车尾气中的有害物质之一,能与水反应;W气体的水溶液滴入酚酞变红色。
请回答下列问题:
(1)X、Y两种气体按物质的量之比1:1在水溶液中能发生反应,化学方程式为 。
(2)科学家发现,Z在催化剂条件下能与W反应,反应产物中的单质应是(填化学式) ;该反应是氧化还原反应,则其中的氧化剂是(填化学式) 。
(3)在Z与水的反应中,氧化剂与还原剂的物质的量之比为 。
(4)检验W气体的方法是 。
(1)原子序数11-17的元素,自钠到氯,电子层数相同,最外层电子数从 增加到 ,随着核电荷数依次递增,原子半径依次 ,核对外层电子的引力逐渐 ,失电子能力逐渐 ,得电子能力逐渐 ,因此,金属性逐渐 ,非金属性逐渐 。
(2)元素金属性的强弱,可以从它的单质与水或酸反应置换氢的 程度,以及它的最高价氧化物的水化物的 强弱来判断。元素非金属性的强弱,可以从它的最高价氧化物的水化物的 强弱,或它的单质跟H2生成气态氢化物的 及氢化物的 来判断。
(3)元素的性质随着原子序数的递增而呈 的变化,这个规律叫做元素周期律。
下表给出14—17号元素的一些性质,请回答:
| |
14Si |
15P |
16S |
17Cl |
| 单质与H2 反应的条件 |
高温 |
磷蒸气与 H2能反应 |
加热 |
光照或点燃 时发生爆炸 |
| 最高价氧化 物的水化物 |
H4SiO4 弱酸 |
H3PO4 中强酸 |
H2SO4 强酸 |
HClO4 最强含氧酸 |
(1)它们所形成的氢化物中稳定性最差的是 ,还原性最差的是 。
(2)四种元素的非金属性随着元素原子序数的递增而逐渐 ,试从原子结构的角度加以解释 。
(3)一定条件下,反应H2S+Cl2=2HCl+S能否发生?简述理由 。
 粤公网安备 44130202000953号
粤公网安备 44130202000953号