A、B、C、D均为中学化学所学的常见物质,它们之间的转化关系如下列各图所示(部分反应条件或产物已略去).请按要求回答下列问题:


(1)若A、B、C、D均含有同一种短周期元素X,它们的转化关系如图l所示:
①常温下,若A为化合物,C为红棕色气体,D为强电解质,则X所在周期表中的位置是 ;用方程式表示A溶于水,使酚酞变红的原因: .
②常温下,若A为固体单质,D为强电解质,则D可能的化学式为 、 .符合上述条件且含有离子键的C的电子式: .
(2)若A、B、C均含有同一种短周期元素Y,它们的转化关系如图2所示:
若Y的周期数等于主族序数;盐A溶液显酸性:盐B溶液显碱性,且焰色反应为黄色;C为两性氢氧化物。请用离子方程表示B溶液显碱性的原因: ;在实验室里,欲使A溶液中的阳离子全部沉淀出来转化为C,所发生化学反应的离子方程式为_____________。
一种新型高效净水剂PAFC-聚合氯化铁铝[AlFe(OH)nCl(6-n)]m,应用非常广泛。
为测定PAFC中Al的含量,采用如图所示流程进行。
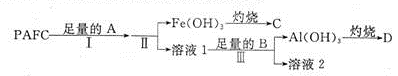
请回答下列问题:
(1)①步骤I中的试剂A是 (填“氨水”或“氢氧化钠溶液”)。
②步骤III的离子方程式为
③实验室进行“灼烧”时所需的陶瓷仪器有
④溶液2中存在的电荷守恒式为 ;向溶液2中滴加少量NaOH溶液,则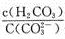 (填“变大”、“变小”或“不变”)。
(填“变大”、“变小”或“不变”)。
(2)C和某一金属在高温下发生反应可用于焊接钢轨,其化学反应方程式为 ;某同学在实验室中进行此反应,反应结束后将所得固体溶于足量的稀硫酸,滴加KSCN溶液无明显现象,由此该同学确定该固体混合物中无Fe203,他的判断是否正确? (填“是”或“否”);其理由是
(用离子方程式等释)
在一定条件下,下列各物质可发生如图所示的变化(反应中生成的水没有写出)

(1)B的化学式是
(2)A的电子式是
(3)已知气体F是一种漂白剂,写出D和F反应的化学方程式:
(4)写出反应II的离子方程式:
A~H都是初中化学中常见的物质,已知B为黑色固体,D为红色固体单质,F为红色固体,H溶液中的溶质是一种盐.它们的转化关系如图所示.请回答:

(1)物质B、E和F的化学式为B 、E 、F ;
(2)反应①的化学方程式为: ,其反应类型为 。
下图是无机物A~M在一定条件下的转化关系(部分产物及反应条件未列出)。其中,I是由第三周期元素组成的单质中熔点最高的金属, K是一种红棕色气体。
请填写下列空白:
(1)在周期表中,组成单质I的元素位于第__________周期_________族。
(2)在反应⑦中氧化剂与还原剂的物质的量之比为___________________。
(3)在②、③、⑥、⑨中既属于化合反应又属于非氧化还原反应的是__________(填序号)
(4)反应④的离子方程式是__________________________________。
(5)将化合物D与KNO3、KOH共融,可制得一种“绿色”环保高效净水剂K2FeO4(高铁酸钾),同时还生成KNO2和H2O。该反应的化学方程式是 _________________________。
以下均为中学化学常见物质,存在如下转化关系(部分产物已省略)。通常C为气体单质,G为紫黑色固体单质。实验室中,常用固体E在B的催化下加热制取气体单质H。

(1)G的化学式 ;F的电子式
(2)反应②的离子方程式 ;
(3)写出另外一种实验室制取H的化学方程式 ;
(4)D溶液中阳离子的焰色反应火焰呈 色;可用 试剂检验D溶液中大量存在的阴离子。
(8分)现有A、B、C、D四种短周期元素, A分别与B、C、D结合生成甲、乙、丙三种化合物, 且甲、乙、丙3分子中含相同数目的质子数,C、D结合生成化合物丁。有关元素的单质和甲、乙、丙、丁四种化合物的转化关系如下图:

(1)写出B+乙→甲+C的化学反应方程式______________________。
(2)根据以上条件可以确定A、B、C、D四种元素中的三种,不能被确定的第四种元素是_______。(填写序号)
① A ② B ③ C ④ D
(3) 依据下列条件可以进一步确定上述第四种元素:
①甲与丙以及乙与丙均能够发生反应,②甲、丙、丁都是无色有刺激性气味的物质。
据此,请回答下列问题:
A.写出上述第四种元素在周期表中的位置 。
B.写出C+丙→乙+丁的化学反应方程式 。
下图是一些常见的单质、化合物之间的转化关系图,有些反应中的部分物质被略去。反应①常被应用于野外焊接钢轨,F是海水中含有盐的主要成分,J为D、G反应产物形成的水溶液。

请回答下列问题:
(1)B的化学式为 。
(2)反应②在工业上通常称之为 工业。
(3)写出反应③的离子方程式 。
(4)写出反应④的化学方程式 。
下图表示有关物质之间的转化关系,A、C、E、G为非金属单质,其中A、G在常温下为气体,E遇淀粉变蓝,K是一种常用的食品添加剂,L是常见的无色无味液体,I为淡黄色固体,J的焰色反应呈浅紫色(透过蓝色钴玻璃).
(1)B、I代表的物质化学式分别为_______________________。
(2)写出反应②的离子方程式:②_______________________。
(3)选出实验室保存C单质的注意事项_______________(A.无色瓶;B.棕色瓶;C.橡胶塞;D.玻璃塞),除此之外还采取了什么特殊保存方法:__________________________。
(4)已知A、C、E均能与G反应,按其反应条件要求由高到低顺序为 ____________(用化学式表示)
(5)A与H溶液反应,其氧化产物和还原产物的物质的量的比为1:1,写出此反应的化学反应方程式____________________。
常见的五种盐X、Y、Z、M、N,它们的阴离子可能是SO42-、Cl-、NO3-、CO32-,阳离子可能是Ag+、NH4+、Na+、Al3+、Cu2+、Ba2+、Fe3+,已知:
①M的焰色反应呈黄色。
②五种盐均溶于水,水溶液均为无色。
③X的溶液呈中性,Y、Z、N的溶液呈酸性,M的溶液呈碱性。
④若在这五种盐的溶液中分别加入Ba(NO3)2溶液,只有X、Z的溶液不产生沉淀。
⑤若在这五种盐的溶液中,分别加入氨水,N和Z的溶液中生成沉淀,继续加氨水,Z中沉淀消失。
⑥把X的溶液分别加入到Y、Z、N的溶液中,均能生成不溶于稀硝酸的沉淀。
请回答下列问题:
(1)五种盐中,一定不含有的阳离子是_________;所含阴离子相同的两种盐的化学式是_____________。
(2)M的化学式为_______________,M溶液显碱性的原因是________________(用离子方程式表示)。
(3)X和Z的溶液反应的离子方程式是______________;N和氨水反应的离子方程式是__________________。
(4)若要检验Y中所含的阳离子,正确的实验方法是______________________。
某固体混合物可能含Al、(NH4)2SO4、MgCl2、A1Cl3、FeCl2、NaCl中的一种或几种,现对该混合物作如下实验,所得现象和有关数据如图(气体体积已换算成标况下体积):
回答下列问题:
(1)混合物中是否存在FeCl2_____________(填“是”或“否”);
(2)混合物中是否存在(NH4)2SO4_____________(填“是”或“否”),你的判断依据是________________。
(3)写出反应④的离子反应式:_________________________。
(4)请根据计算结果判断混合物中是否含有AlCl3(填“是”或“否”),你的判断依据是_________。
下图所示各物质是由1~20号元素中部分元素组成的单质或其化合物,图中部分反应条件未列出。已知C、H是无色有刺激性气味的气体,D是一种黄绿色的气体单质,物质J可用于泳池消毒。反应②和④是化工生产中的重要反应,反应⑤是实验室制备气体C的重要方法。
请回答下列问题:
(1)I中所含化学键类型_______________,
(2)G的水溶液呈酸性,用离子方程式表示其原因_______________________
(3)实验室制备气体C的化学方程式___________________________
(4)已知含7.4gI的稀溶液与200mL1mol/L的H溶液反应放出11.56kJ的热量,写出该反应的热化学方程式_________________________________
(5)物质A由三种元素组成,1 mol A与水反应可生成1 mol B和2 mol C,A化学式为_______________。
有A、B、C、D、E、F六种元素,原子序数依次增大,A、B、C、D、E均为短周期元素,A元素原子核内只有一个质子,元素A与B形成的气态化合物甲在标准状况下的密度为0.759g•L-1,C元素原子的最外层电子数是其电子层数的3倍,E与C同主族.均含D元素的乙(金属阳离子)、丙、丁微粒间的转化全为非氧化还原反应:均含F元素的乙(单质)、丙、丁微粒间的转化全为氧化还原反应.
请回答下列问题:
(1)单质B的结构式:________________________。
(2)F元素周期表中的位置:_______________________。
(3)均含有F元素的乙与丁在溶液中发生反应的离子方程式___________________;均含有D元素的乙与丁在溶液中发生反应的离子方程式________________________。
(4)由A、C元素组成化合物良和A、E元素组成的化合物辛,式量均为34.其中庚的溶沸点比辛_______(填“高”或“低”),原因是_________________。
物质A、B、C、D、E、F、G、H、I、J、K有下图转化关系,其中气体D、E为单质,
请按要求回答下列问题。

(1)金属A元素在周期表的位置是 ,G的化学式是__________。
(2)写出反应“C→F”的离子方程式 ;
(3)写出反应“I→J”的离子方程式 ;
(4)写出金属 H与水蒸气在高温下反应的化学方程式 。
A.B C.D.E.F六种物质的转化关系如图所示(反应条件和部分产物未标出)

(1)若A为短周期金属单质,D为短周期非金属单质,且所含元素的原子序数A是D的2倍,所含元素的原子最外层电子数D是A的2倍,F的浓溶液与A D反应都有红棕色气体生成,则A为 ,反应④的化学方程式为 .
(2)若A为常见的金属单质,D F是气态单质,反应①在水溶液中进行,则反应②(在水溶液中进行)的离子方程式是 .
(3)若A.D.F都是短周期非金属元素单质,且A.D所含元素同主族,A.F所含元素同周期,则反应①的化学方程式为 .