A~H都是初中化学中常见的物质,已知B为黑色固体,D为红色固体单质,F为红色固体,H溶液中的溶质是一种盐.它们的转化关系如图所示.请回答:
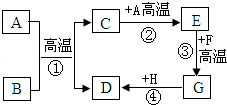
(1)物质B、E和F的化学式为B 、E 、F ;
(2)反应①的化学方程式为: ,其反应类型为 。
A~H都是初中化学中常见的物质,已知B为黑色固体,D为红色固体单质,F为红色固体,H溶液中的溶质是一种盐.它们的转化关系如图所示.请回答:

(1)物质B、E和F的化学式为B 、E 、F ;
(2)反应①的化学方程式为: ,其反应类型为 。