浙江省瑞安市四校高三上学期第一次联考化学试卷
化学与社会、生活密切相关。下列有关说法错误的是
| A.明矾中铝离子水解产生的胶体具有很强的吸附作用而常用于净水 |
| B.地球上99%以上的溴蕴藏在大海中,因此溴被称为“海洋元素” |
| C.目前加碘盐中添加的含碘物质是KI,可用氯水和淀粉溶液鉴定食盐是否加碘 |
| D.为减少污染、提高燃烧效率,可将煤气化或液化获得清洁燃料 |
分类是重要的化学学习方法。下列对应关系正确的是
| A.混合物——液氯、漂白粉 | B.碱性氧化物——Al2O3、Na2O2 |
| C.强电解质—— NH4Cl、HClO | D.非电解质—— NH3、SO2 |
下列说法正确的是
| A.168O、188O为不同的核素,有不同的化学性质 |
| B.H2、SO2、NH3三种气体都可用浓硫酸干燥 |
| C.分散系中分散质粒子的直径:Fe(OH)3悬浊液 > Fe(OH)3胶体 > FeCl3溶液 |
| D.陶瓷、玻璃、水泥、大理石的主要成分都是硅酸盐 |
按照阿伏伽德罗定律,下列叙述不正确的是
| A.同温同压下两种气体的体积之比等于物质的量之比 |
| B.同温同压下两种气体的物质的量之比等于密度之比 |
| C.同温同压下两种气体的密度之比等于摩尔质量之比 |
| D.同温同体积下两种气体的物质的量之比等于压强之比 |
下列说法中正确的是
| A.酸根离子中不可能含有金属元素 |
| B.酸性氧化物在一定条件下,都可以与碱反应生成盐和水 |
| C.一种元素可能有多种氧化物,但是同种化合价只对应一种氧化物 |
| D.还原产物只有还原性,氧化产物只有氧化性 |
下列有关物质制备说法不正确的是
| A.电解饱和食盐水制得金属Na |
| B.电解熔融MgCl2制得金属Mg |
| C.高温下CO还原赤铁矿可用于炼铁 |
| D.高温下焦炭还原二氧化硅制得粗硅 |
实验是化学的基础。下列说法正确的是
| A.过氧化钠、氯水、浓硝酸通常都要密封保存于棕色试剂瓶中 |
| B.盛溴的试剂瓶里加少量水以减少溴的挥发 |
| C.钾、钠、白磷都应保存在水中 |
| D.做焰色反应实验时所用铂丝,每次用完后用稀硫酸洗涤后再使用 |
经氯气消毒的自来水,用以配制以下溶液,不会使溶液变质的是
| A.AgNO3溶液 | B.FeCl2溶液 | C.Na2CO3溶液 | D.NaCl溶液 |
由铝屑、盐酸、氢氧化钠溶液反应制取1mol Al(OH)3,至少需要消耗HCl和NaOH的物质的量为
| A.0.25mol,0.25mol | B.0.75mol,0.75mol |
| C.1mol,1mol | D.3mol,3mol |
某生配制480ml 0.1mol/L的NaOH溶液,下列操作可使所配制的溶液的浓度偏大的是
| A.烧杯中溶液转移到容量瓶中时,未洗涤烧杯 |
| B.移液时,有少量液体溅出 |
| C.定容时,俯视刻度线 |
| D.定容摇匀后发现液面下降,继续加水至刻度线 |
下列各组物质中,Y既能与X反应又能与Z反应的是
| 编号 |
X |
Y |
Z |
| ① |
N2 |
Mg |
CO2 |
| ② |
FeCl3溶液 |
Cu |
浓硝酸 |
| ③ |
氨水 |
Al(OH)3 |
稀硫酸 |
| ④ |
KOH溶液 |
SiO2 |
盐酸 |
A.①② B.①④ C.①②③ D.①②④
下列变化过程不涉及氧化还原反应的是
| A.将一小块钠放在石棉网上加热,生成淡黄色物质 |
| B.向新制氯水中加入足量亚硫酸钠溶液,氯水褪色 |
| C.向纯碱溶液中滴加酚酞,溶液变红色 |
| D.向氢碘酸中滴加FeCl3溶液,产生棕色物质 |
下列各组离子在指定溶液中,一定能大量共存的是
| A.加入Mg能放出H2的溶液中:Mg2+,NH4+,Cl-,SO42- |
| B.含有NaClO的溶液中:K+,Al3+,Br-,S2- |
| C.澄清透明溶液:Cu2+、SO42-、HCO3-、H+ |
| D.使甲基橙变红的溶液中:Fe2+,MnO4-,Na+,SO42- |
物质的分离与提纯是化学实验研究常用的方法。下列混合体系分离提纯对应的方法不正确的是
| 选项 |
A |
B |
C |
D |
| 混合体系 |
溴水 |
酒精与水 |
固体碘和氯化铵 |
混有少量KCl的KNO3粉末 |
| 分离方法 |
萃取、分液 |
加生石灰,蒸馏 |
加热 |
配成热的饱和溶液、降温结晶 |
在给定条件下,下列划横线的物质在化学反应中能被完全消耗的是
| A.常温下,将1 g铝片投入20 mL 18.4 mol·L-1的硫酸中 |
| B.向100 mL 3 moI·L-1的硝酸中加入5.6 g铁 |
| C.用50 mL浓盐酸与足量MnO2共热 |
| D.在5×107 Pa、500 ℃和铁触媒催化的条件下,用3 mol氢气和2 mol氮气合成氨 |
下列实验不合理的是
| A.证明非金属性强弱 S>C>Si | B.四氯化碳萃取碘水中的碘 |
| C.制备并收集少量NO气体 | D.制备少量氧气 |
下列各组在溶液中的反应,不管反应物的量是多少,都能用同一离子方程式表示的是
| A.FeBr2与Cl2 | B.Ba(OH)2与H2SO4 |
| C.HCl与Na2CO3 | D.NaHCO3与Ca(OH)2 |
用NA表示阿伏加德罗常数的值,下列说法中正确的是
| A.标准状况下,11.2LCCl4中含有分子的数目为0.5NA |
| B.标准状况下,2.24LCl2通入水中生成NA个HClO |
| C.1.6gO2与O3组成的混合物中所含O原子数为0.1NA |
| D.25℃时pH=13的NaOH溶液中含有OH-的数目为0.1NA |
下列各反应的化学方程式中,不正确的是
A.将点燃的镁条伸入充满CO2气体的集气瓶中:2Mg + CO2 2MgO+C 2MgO+C |
| B.大理石溶于醋酸:CO3 2- + 2CH3COOH = 2CH3COO- + CO2↑+ H2O |
| C.向NH4HSO4稀溶液中逐滴加入Ba(OH)2稀溶液至SO42-刚好沉淀完全: Ba2+ + 2OH- + NH4+ + H+ + SO4 2- = BaSO4↓+ NH3·H2O + H2O |
| D.向淀粉KI溶液中滴加稀硫酸,在空气中放置一段时间后溶液变蓝: |
4H+ +4I- + O2 = 2I2 +2H2O
将一定量铁粉和铜粉的混合物加入由稀硫酸和稀硝酸组成的混合溶液中,充分反应后金属粉末有剩余,下列有关推断正确的是
| A.反应过程中不可能产生H2 |
| B.往反应后的溶液中加入KSCN溶液会变血红色 |
| C.剩余的金属粉末中一定有铜 |
| D.往反应后的溶液中加入足量的稀H2SO4,则金属粉末的质量一定会减少 |
将一定量的CO2气体通入2L未知浓度的NaOH溶液中,在所得溶液中逐滴加入稀盐酸至过量,并将溶液加热,产生的气体与HCl的物质的量的关系如图所示(忽略气体的溶解和HCl的挥发),下列说法不正确的是
| A.O点溶液中所含溶质的化学式为NaOH、Na2CO3 |
| B.常温下,a点溶液pH>7 |
| C.标准状况下,通入CO2的体积为4.48L |
| D.原NaOH溶液的物质的量浓度为2.5mol/L |
在一个氧化还原反应的体系中,共有H2O、ClO-、CN-、HCO3-、N2、Cl-六种物质。在反应过程中测得ClO-和N2的物质的量随时间变化的曲线如图所示。下列有关判断中正确的是
| A.还原剂是含CN-的物质,氧化产物只有N2 |
| B.氧化剂是ClO-,还原产物是HCO3- |
| C.配平后氧化剂与还原剂的化学计量数之比为4:1 |
| D.标准状况下,若生成2.24LN2,则转移电子数为NA |
某混合溶液中可能含有下列离子中的若干种:NH4+、Na+、Al3+、Fe2+、Fe3+、AlO2-、SO42-、I-、NO3-、CO32-,已知各离子的浓度均约为0.1mol/L,现取两份20mL该溶液进行如下实验:
第一份加入足量盐酸,产生气体在空气中变为红棕色,在反应后的溶液中加入BaCl2溶液,有白色沉淀产生。第二份逐滴滴加NaOH溶液至过量,产生沉淀但不溶解,同时逸出气体。根据上述实验情况,以下说法错误的是
| A.该混合溶液中一定不含有Fe3+、AlO2-、Al3+、CO32- |
| B.该混合溶液通过继续进行焰色反应可以间接确定是否含有I- |
| C.该混合溶液中肯定含有Fe2+、NH4+、SO42-、NO3- |
| D.向该混合溶液中滴加酚酞试液后呈红色 |
A、B、C、D四种短周期元素,A元素的一种同素异形体是自然界硬度最大的单质,C与A同主族,C元素的原子序数是B的2倍,工业上以D元素的单质与石灰乳为原料制造漂白粉。按要求回答下列问题:
(1)B的原子结构示意图为 ;镁条在气体B中燃烧生成的物质是 (填化学式);
(2)A的非金属性强于C,请用一个化学反应方程式表示___________ ;
(3)元素B、D形成的化合物BD3能与水反应生成具有漂白性的物质X,写出该反应的化学方程式 。
铝、铁及其化合物在国民经济、日常生活中占有非常重要的地位。请回答下列问题:
(1)铝在自然界中以 态(填“游离”或“化合”)存在;铁的氧化物中常用作红色油漆和涂料的是 (填化学式),该氧化物与铝粉在高温下反应的化学方程式为 ;
(2)用离子方程式表示除去铁粉中混有的铝粉 ;
(3)下列对Fe2+的检验方法不合理的是 。
| A.向某溶液中滴入KSCN溶液呈血红色,说明不含Fe2+ |
| B.向某溶液中通入Cl2,然后再加入KSCN溶液变成血红色,说明原溶液中含有Fe2+ |
| C.向某溶液中加NaOH溶液得白色沉淀,再逐渐变为红褐色,说明该溶液中含有Fe2+ |
| D.向某溶液中滴入酸性高锰酸钾溶液,溶液紫红色褪去,说明该溶液中含有Fe2+ |
以下均为中学化学常见物质,存在如下转化关系(部分产物已省略)。通常C为气体单质,G为紫黑色固体单质。实验室中,常用固体E在B的催化下加热制取气体单质H。

(1)G的化学式 ;F的电子式
(2)反应②的离子方程式 ;
(3)写出另外一种实验室制取H的化学方程式 ;
(4)D溶液中阳离子的焰色反应火焰呈 色;可用 试剂检验D溶液中大量存在的阴离子。
某研究小组以粗盐和碳酸氢铵(NH4HCO3)为原料,采用以下流程制备纯碱和氯化铵。
已知盐的热分解温度: NH4HCO3 36℃; NaHCO3 270℃; NH4Cl 340℃; Na2CO3 >850℃
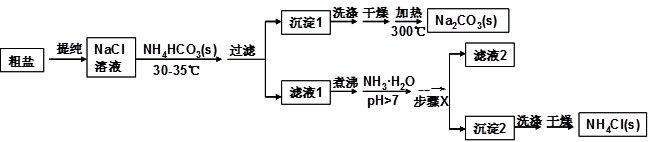
(1)粗盐中含有Ca2+、Mg2+、SO42-等杂质离子,使用的试剂有:①NaOH ②BaCl2 ③HCl ④Na2CO3,其加入的顺序合理的是
| A.①③④② | B.①②④③ | C.③②④① | D.①②③④ |
过滤中用到玻璃棒的作用是 ;
(2)如何判断粗盐中SO42-是否已除尽? ;
(3)从NaCl溶液到沉淀1的过程中,需蒸发浓缩。在加入固体NH4HCO3之前进行蒸发浓缩优于在加入NH4HCO3之后,原因是 ;
(4)写出沉淀1受热分解的化学方程式 ;
(5)为提高NH4Cl产品的产率和纯度,需在滤液中加入氨水,理由是 ;
步骤X包括的操作有 ;
(6)采用“甲醛法”测定工业产品中氯化铵的纯度(假定杂质不与甲醛反应),反应原理为:4NH4Cl+6HCHO→(CH2)6N4+4HCl+6H2O 某技术人员称取1.5g该样品溶于水,加入足量的甲醛并加水配成100mL溶液。从中取出10mL,滴入酚酞再用0.1mol/L的NaOH溶液滴定,到滴定终点时消耗NaOH溶液25.00mL。则该样品中氯化铵的质量分数为 。
 粤公网安备 44130202000953号
粤公网安备 44130202000953号