下图所示各物质是由短周期部分元素组成的单质或其化合物,图中部分反应条件及物质未列出。已知:A、C、D、F均为单质,C、E、F、G常温下是气体,J为白色沉淀,既能溶于B,又能溶于E;物质B、G可以使湿润的红色石蕊试纸变蓝,且B的焰色反应呈黄色。反应④是化肥工业的重要反应。
请回答下列问题:
(1)A的元素在元素周期表中的位置是 ,物质B的电子式为 。
(2)上述反应①~⑥中,属于化合反应的是 ,反应⑤的离子方程式为 。
(3)在I的水溶液滴加B溶液至过量的过程中,所观察到的现象为 。
X、Y、Z、W均为中学化学的常见物质,一定条件下它们之间有如图所示转化关系(其他产物已略):下列说法不正确的是
| A.若W是单质铁,则Z溶液可能是FeCl2溶液 |
| B.若X是金属铝,则W可能是强碱 |
| C.若W是氢氧化钠,则X与Z可能反应生成Y |
| D.若X为氧气,则X与Y的相对分子质量可能相差12 |
如图为含有同一种元素的a、b、c、d、e五种物质的转化关系。
其中a是单质,b是气态氢化物,c、d是氧化物,e是该元素最高价氧化物对应的水化物,则a可能是( )
①C ②N2③S ④F2
| A.只有①和③ | B.只有④ | C.①②③ | D.①②③④ |
据下图的转化关系及现象回答下列问题。已知白色沉淀是碳酸钙
(1)固体X的名称______________;A的化学式______________。
(2)写出反应①②③④的化学方程式
①________________________________;
②________________________________;
③________________________________;
④________________________________。
目前,世界上生产的镁有60%来自海水,其生产流程图如下
(1)贝壳的主要化学成分为 。(写化学式)
(2)写出反应②的离子方程式: 。
(3)写出Mg与CO2反应的化学方程式 。
(4)电解氯化镁所得的氯气,除用于生产盐酸外,请举出氯气在工业上的另一种用途(用化学方程式表示) 。
(8分) 下图的转化关系中,A、C、D是常见的气体单质,D气体在常温下呈黄绿色。F气体极易溶于水,且液态常作制冷剂,B的焰色反应为黄色。图中的部分反应产物或反应物已略去。
(1)写出G的化学式: 。
(2)写出F的电子式: 。
(3)写出D单质和E溶液反应的离子方程式: 。
(4)写出电解B溶液的化学方程式: 。
已知A、B、C、D之间的转化关系为:A + B → C + D,则下列有关说法不正确的是
A.若A为Fe,D为氢气,则B可能是酸,也可能是水
B.若A、D为化合物,B为水,则C可能是气体单质,也可能是化合物
C.若A、B、C、D均为化合物,该反应一定属于复分解反应
D.若A、B、C、D均为10电子微粒,且C是可使湿润的红色石蕊试纸变蓝的气体,则D 在常温下一定呈液态
如图的各方框表示有关的一种反应物或生成物(某些物质已经略去),其中常温下A、C、D为无色气体,B为液体,C能使湿润的红色石蕊试纸变蓝,由X受热分解生成的A、B、C的物质的量之比为1:1:1.

(1)写出下列各物质的化学式:D:______;F: 。
(2)写出X分解为A、B、C的化学方程式 。
(3)写出G→E变化的离子方程式 。
A、B、C、D四种物质之间有下图所示的转化关系。已知:A是空气中的主要成分,B、C、D均为化合物,且C为红棕色气体。
请回答下列问题:
(1)写出A和C的名称或化学式: A ,C ;
(2)在上图D→C的过程中,D表现出强 (填“氧化性”或“还原性”);
(3)在D的稀溶液中滴入NaOH溶液,其反应的离子方程式是 。
化合物F是合成吲哚﹣2﹣酮类药物的一种中间体,其合成路线如图:
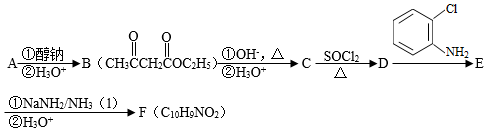
已知:Ⅰ.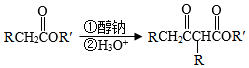
Ⅱ.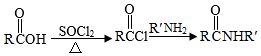
Ⅲ.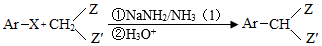
Ar为芳基;X=Cl,Br;Z或Z′=COR,CONHR,COOR等。
回答下列问题:
(1 )实验室制备A的化学方程式为 ,提高A产率的方法是 ; A的某同分异构体只有一种化学环境的碳原子,其结构简式为 。
(2)C→D的反应类型为 ; E中含氧官能团的名称为 。
(3)C的结构简式为 ,F的结构简式为 。
(4)Br2和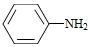 的反应与Br2和苯酚的反应类似,以
的反应与Br2和苯酚的反应类似,以 和
和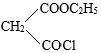 为原料合成
为原料合成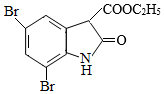 ,写出能获得更多目标产物的较优合成路线(其它试剂任选)。
,写出能获得更多目标产物的较优合成路线(其它试剂任选)。
苯佐卡因是临床常用的一种手术用药。以甲苯为起始原料的合成路线如图。
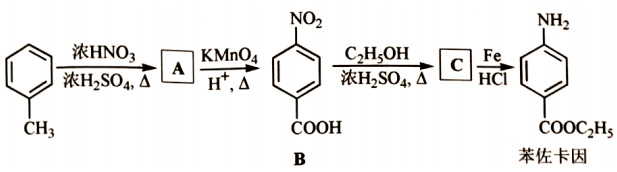
回答问题:
(1)甲苯分子内共面的H原子数最多为 个。
(2)A的名称是 。
(3)在A的同分异构体中,符合下列条件的是 ( 写出一种结构简式)。
①与A具有相同官能团
②属于芳香化合物
③核磁共振氢谱有5组峰
(4)B中官能团名称为 。
(5)B→C的反应方程式为 。
(6)反应过程中产出的铁泥属于危化品,处理方式为 ( 填编号)。
a.高温炉焚烧
b.填埋
c.交有资质单位处理
(7)设计以甲苯和丙三醇为原料合成3﹣苄氧基﹣1,2﹣丙二醇(  )的路线 (其他试剂任选)。
)的路线 (其他试剂任选)。
已知:在于HCl催化下丙酮与醇ROH反应生成缩酮。缩酮在碱性条件下稳定。在酸中水解为丙酮和醇ROH。
X、Y、Z是三种常见的单质,甲、乙是两种常见的化合物,这些单质和化合物之间存在如图所示的关系,下列说法正确的是
| A.X、Y、Z一定都是非金属单质 |
| B.X、Y、Z一定都是金属单质 |
| C.X、Y、Z中至少有一种是非金属单质 |
| D.X、Y、Z中至少有一种是金属单质 |
中学化学中,常见无机物A、B、C、D、E、X、Y存在如下图转化关系(部分生成物和反应条件略去)。下列推断正确的是( )

A.若A是CaC2,X是H2O,则Y一定是溴水
B.若A是金属钠,X是H2O,则E一定能还原Fe2O3
C.若Y是NaOH,C是白色沉淀,则A与X一定发生置换反应
D.若Y是氧气,D是氧化物,则A与X一定发生氧化还原反应
银铜合金广泛应用于航空工业。从切割废料中回收银并制备铜的化工产品工艺如下:
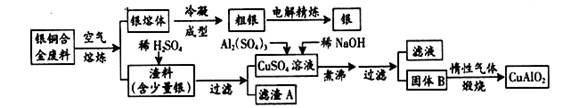
(注:Al(OH)3和Cu(OH)2开始分解的温度分别为450℃和80℃)
(1)滤渣A与稀HNO3反应,产生的气体在空气中迅速变为红棕色,该气体变色的化学方程式为 。
(2)固体混合物B的组成为 ;在生成固体B的过程中,需控制NaOH的加入量,若NaOH过量,则因过量引起的反应的离子方程式为 。
(3)若银铜合金中铜的质量分数为63.5%,理论上5.0kg废料中的铜可完全转化为____mol CuAlO2(Cu 的相对原子量取63.5),至少需要1.0mol·L-1的Al2(SO4)3溶液 L。
有三种金属单质A、B、C,其中A的焰色反应为黄色,B、C是常见金属,且C的合金用量最大。三种金属单质A、B、C与气体甲、乙、丙及物质D、E、F、G、H之间发生如下转化关系(图中有些反应的产物和反应的条件没有标出)。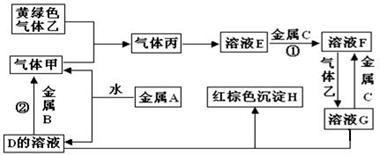
请根据以上信息回答下列问题:
(1)写出下列物质的化学式:A________、H__________、乙_______、C的一种氧化物是具有磁性的黑色晶体,该氧化物的化学式是 ;
(2)写出下列反应的化学方程式:
反应①_____________________________________;
反应②_____________________________________。
(3)检验溶液G中金属阳离子的常用方法是 。