据下图的转化关系及现象回答下列问题。已知白色沉淀是碳酸钙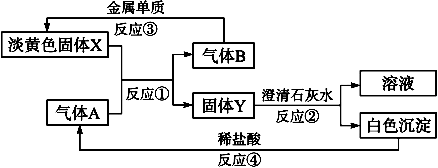
(1)固体X的名称______________;A的化学式______________。
(2)写出反应①②③④的化学方程式
①________________________________;
②________________________________;
③________________________________;
④________________________________。
据下图的转化关系及现象回答下列问题。已知白色沉淀是碳酸钙
(1)固体X的名称______________;A的化学式______________。
(2)写出反应①②③④的化学方程式
①________________________________;
②________________________________;
③________________________________;
④________________________________。