氮元素的氢化物和氧化物在工业生产和国防建设中都有广泛应用,回答下列问题:
(1)氮元素原子的L层电子数为 ;
(2)NH3与NaClO反应可得到肼(N2H4),该反应的化学方程式为 ;
(3)肼可作为火箭发动机的燃料,与氧化剂N2O4反应生成N2和水蒸气。
已知:①N2(g)+2O2(g)= N2O4(1) △H1= -195kJ·mol-1
②N2H4(1) + O2(g)= N2(g) + 2H2O △H2= -534.2kJ·mol-1
写出肼和N2H4反应的热化学方程式 ;
(3)肼一空气燃料电池是一种碱性电池,该电池放电时,负极的反应式为 。
某小组对Cu与浓HNO3的反应进行研究。记录如下:
I.Cu与浓HN03反应的化学方程式是 。
II.探究实验1中溶液A呈绿色而不是蓝色的原因。
(1)甲认为溶液呈绿色是由Cu2+离子浓度较大引起的。乙根据实验记录,认为此观点不正确,乙的依据是 。
(2)乙认为溶液呈绿色是由溶解的NO2引起的。进行实验2:先将NO2通入B中,再鼓入N2。结果证实假设成立。则以上两步操作对应的现象分别是 、 。
(3)为深入研究,丙查阅资料,有如下信息:
i.溶有NO2的、浓HNO3呈黄色;水或稀HNO3中通少量NO2溶液呈无色。
ii.NO2溶于水,会发生反应2NO2+H2O =HNO3+HNO2HNO2是弱酸,只能稳定存在于冷、稀的溶液中,否则易分解。
iii.NO—2能与Cu2+反应:Cu2+(蓝色)+4 NO2- Cu(NO2)42-(绿色)
Cu(NO2)42-(绿色)
据此,丙进一步假设:
①可能是A中剩余的浓HNO3溶解了NO2得到的黄色溶液与Cu(NO3)2的蓝色溶液混合而形成的绿色;
②可能是A中生成了Cu(NO2)2—4使溶液呈绿色。
丙进行如下实验:
①亚硝酸分解的化学方程式是 。
②请用平衡原理解释加入稀H2SO4后绿色溶液变蓝的原因: 。
(4)根据实验得出结论:实验l中溶液A呈绿色的主要原因是 ,请依据实验现象阐述理由: 。
非金属单质A经如图所示的过程转化为含氧酸D,已知D为强酸,请回答下列问题:
(1)若A在常温下为固体,B是能使品红溶液褪色的有刺激性气味的无色气体。
①D物质的名称是________;请写出由B转化成 C的化学方程式____________________________
②在工业生产中大量排放的B气体被雨水吸收后形成了________而污染了环境。
(2)若A在常温下为气体,C是红棕色的气体。
①A、C的化学式分别是:A________;C________.请写出由C与H2O生成 D的化学方程式
____________________________________________________
②D的浓溶液在常温下可与铜反应并生成C气体,请写出该反应的离子方程式___________________________________________。
焊接钢铁时常用的焊药为氯化铵,其作用是消除焊接处的铁锈。发生的反应体系中共有六种物质:NH4Cl、FeCl3、N2、Fe2O3、Fe和X。
(1)根据题意,可判断出X是________(写化学式)。
(2)写出并配平该反应的化学方程式:_________________________;
(3)发生还原反应的物质是________,反应中2mol的氧化剂能___________(填“失去”或“得到”)_________mol电子。
(4)反应中被氧化产生了5.6L(标准状况)的气体时,被还原的物质的质量为____________。
哈伯因为氨气的合成曾获1918年诺贝尔奖。
(1)写出实验室由NH4Cl和Ca(OH)2加热制取氨气的化学方程式: ;
检验氨气已收集满的方法是:用湿润的 色石蕊试纸靠近集气瓶口,现象为试纸变为_____色;
(2)用图装置进行喷泉实验,若在水中加入酚酞,得到红色喷泉。该实验体现了氨气的两个重要性质分别是 、 ;
(3)自然界中固氮过程很多。打雷时发生的固氮反应方程式为 ;
(4)氨气是制取硝酸的基本原料。
①请写出氨催化氧化生成为NO的方程式 ;
②产物NO能发生下列反应:aNO+bO2+cH2O="==" dHNO3
从电子得失相等角度分析可知a:b= 。
稀薄燃烧发动机具有高效、经济、环保等优点,和普通汽车发动机对比如下:
(1)根据上表的数据可知“稀薄”的含义是( )
| A.发动机混合气中的汽油含量低 | B.发动机混合气中的空气含量低 |
| C.发动机混合气中氧气的含量低 | D.发动机混合气中氮气的含量低 |
(2)为何稀薄燃烧发动机产生的尾气中CO含量会减少?
(3)己知汽车尾气中的氮氧化物(以NOX表示)是氮气与氧气在高温下反应产生的。
试解释为何稀薄燃烧发动机产生的尾气中NOX含量也会减少?
(4)某种减少尾气中CO与NOX的方法是使用催化转换器,转换过程中发生反应的化学方程式为:CO + NOX → CO2 + N2(未配平)。若x=1.5,则化学方程式中CO2与N2的系数之比为 。
铜既能与稀硝酸反应,也能与浓硝酸反应,当铜与一定浓度硝酸反应时,可将方程式表示为:Cu+HNO3→Cu(NO3)2+NO↑+NO2↑+H2O (方程式未配平)
(1)硝酸在该反应中表现出的性质是_____________________。
(2)0.4molCu被硝酸完全溶解后,硝酸得到的电子数是________,如果得到的NO和NO2物质的量相同,则参加反应的硝酸的物质的量是________mol。
(3)0.3molCu被另一浓度的硝酸完全溶解后,如果此时产生的NO和NO2气体总体积在标准状况下为8.96 L,则被还原的硝酸的物质的量是_______mol,参加反应的硝酸的物质的量是______mol,产生的混合气体中NO和NO2体积比为_______。
磷矿石主要以磷酸钙和磷灰石
等形式存在。图(a)为目前国际上磷矿石利用的大致情况,其中湿法磷酸是指磷矿石用过量硫酸分解制备磷酸。图(b)是热法磷酸生产过各中由磷灰石制单质磷的流程。


部分物质的相关性质如下:
| 熔点/℃ |
沸点/℃ |
备注 |
|
| 白磷 |
44 |
280.5 |
|
| PH3 |
-133.8 |
-87.8 |
难溶于水,具有还原性 |
| SiF4 |
-90 |
-86 |
易水解 |
回答下列问题:
(1)世界上磷矿石最主要的用途是生产含磷肥料,约占磷矿石使用量的%。
(2)以磷灰石为原料,湿法磷酸过程中反应的化学方程式为:。现有1吨折合含有五氧化二磷约30%的磷灰石,最多可制得85℅的商品磷酸吨。
(3)如图(b)所示,热法生产磷酸的第一步是将二氧化硅、过量焦炭与磷灰石混合,高温反应生成白磷。炉渣的主要成分是:(填化学式)冷凝塔1的主要沉积物是:冷凝塔2的主要沉积物是:(4)尾气中主要含有,还含有少量、
和HF等,将尾气先通入纯碱溶液,可除去
再通入次氯酸钠溶液,可除去(均填化学式)
(5)相比于湿法磷酸,热法磷酸工艺复杂,能耗高,但优点是:。
硝酸铵在现代农业生产和国防中都占有重要地位,下图是云南天然气化工厂合成硝酸铵的简要生产工艺流程:
回答下列问题:
(1)N2的电子式 ,合成氨的反应中,若生成1g氨放出热量a KJ,写出该反应的热化学方程式 。
(2)氨催化氧化的化学方程式是 ,
试从化学反应速率和化学平衡原理分析温度、压强对合成氨反应的影响 。
(3)若输送NH3的管道某处发生泄漏,检测的简单方法 。
(4)农业生产上长期、过量使用化肥硝酸铵,会加重土壤酸化,原因是(用离子方程式回答) 。
(5)25℃时,将x mol NH4NO3溶于一定量水中,向该溶液中滴加y L氨水后溶液呈中性,则滴加氨水过程中水的电离平衡将 (填“正向” “不”或“逆向”)移动,所滴加氨水的物质的量浓度为 (25℃时,Kb(NH3·H2O)="2.0" × 10-5 mol·L-1)。
下列框图中的字母分别代表一种常见的物质或其溶液,相互之间的转化关系如下图所示(部分产物及反应条件已略去)。
已知A、B为气态单质,F是地壳中含量最多的金属元素的单质:E、H、I为氧化物,E为黑色固体,H为红棕色粉末,I为红棕色气体;M为红褐色沉淀,Q为白色胶状物质。
请回答下列问题:
(1)组成单质F的元素在周期表中的位置是______;C中存在的化学键类型为____;E的化学式是___。
(2)A在B中燃烧的现象是_______ 。
(3) D+E→B的反应中,被氧化与被还原的物质的物质的量之比是_______。
(4)反应①的化学方程式为___________________________________ 。
(5)反应②的离子方程式为___________________________________。
(6)Y受热分解可生成H、I和氧气,.写出该反应的化学方程式:______________________。
A~G是中学化学常见物质,其中A为相同条件下密度最小的气体单质,E为红棕色气体。
(1)G的化学式是 。
(2)A和B反应生成C的化学方程式为 。
(3)检验C可选用的试剂是 (填字母)。
a.湿润的蓝色石蕊试纸 b.湿润的红色石蕊试纸 c.浓盐酸
(4)将盛满气体E的大试管倒扣在盛水的水槽中,发生反应的化学方程式为 ,现象为 。
(5)汽车尾气中含有CO和物质D,一种治理方法是在汽车排气管上装一个催化转化装置,使CO和D反应,生成另外两种无毒气体。该反应的化学方程式是 。
用如图所示装置做“铜与浓硝酸反应”的实验。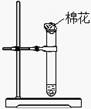
(1)从试剂瓶中取出一小块铜片放入试管中,需用的仪器是 。
(2)棉花应蘸 溶液(填化学式)。
(3)试管中除了溶液变成绿色外,还会出现的现象是 (填序号)。
A.有红棕色气体生成,上下颜色相同
B.有红棕色气体生成,上部颜色较浅
C.有红棕色气体生成,下部颜色较浅
(4)实验结束后,对试管内残留物的处理方法是 。
如图是部分短周期元素的单质及其化合物(或其溶液)的转化关系,已知B、C、D、E是非金属单质,且在常温常压下都是气体;化合物G的焰色反应为黄色,化合物I和J通常状况下呈气态;反应①是化工生产中的一种重要的固氮反应。
(1)单质E的结构式_____________
(2)F和H2O反应的化学方程式为_____________________________,该反应中被氧化与被还原的物质的物质的量之比是_________________
(3)铵盐H中阳离子的电子式_______________,检验H 中阳离子的方法是____________________
_____________________________________________________________________________
下面是中学化学中常用的玻璃仪器组成的实验装置图(根据需要可在广口瓶中加入液体)。
下面是中学化学中常用的玻璃仪器组成的实验装置图(根据需要可在广口瓶中加入液体或在干燥管中放入固体)。
请回答下列问题:
(1)用装置A收集NH3气体,气体应从_________________(填“①”或“②”)处通入。
(2)若用装置B做二氧化硫与烧杯中氢氧化钠溶液反应的实验,则其中广口瓶能否起到防倒吸作用(填“能”或“不能”)______________________。
(3)用C来收集NO2气体,最终得不到NO2,其发生反应的化学方程式为:___________________。
下图为氮及其化合物的类别与化合价对应的关系图。
(1)实验室制取氨气。
① 化学方程式是 。
② 可用向下排空气法收集氨气的原因是 。
③ 用水吸收多余的氨气时,如将导管直接插入水中,
会产生倒吸现象,产生该现象的原因是 。
(2)完成下列能生成NO的化学方程式:
① 体现N元素的还原性:
a. 汽车尾气中产生的NO:N2 + O2  2NO。
2NO。
b. 氨的催化氧化:_________。
② 体现N元素的氧化性:_________。
(3)NO2 易溶于水。将体积为V mL的试管充满NO2后倒扣在水中,见下图。
① NO2溶于水的化学方程式是_________。
② 使试管中NO2完全被水吸收的操作是________。