向由Cu、Cu2O和CuO组成的混合物中,加入10 mL 6 mol·L-1的稀硝酸溶液,恰好使混合物完全溶解,同时收集到标准状况下NO 224 mL。请回答以下问题:
(1)写出Cu2O与稀硝酸反应的离子方程式 。
(2)产物中硝酸铜的物质的量为 。
(3)若原混合物中有0.01molCu,则其中Cu2O的物质的量为 ,CuO的物质的量为 。
某校课外活动小组为了探究铜与稀硝酸反应产生的气体主要是NO而设计了下列实验,装置如图所示(加热装置和固定装置均已略去)。图中K为止水夹(处于关闭状态),F是一半空的注射器。
请回答有关问题:
(1)设计装置A的目的是 ;为达到此目的,应进行的操作是 。
(2)在完成(1)中的“操作”后,将装置B中铜丝插入稀硝酸,并微热之,观察到装置B中的现象是 ;B中反应的离子方程式为: 。
(3)装置E和F的作用是 ;为实现此作用,其操作方法是 。
(4)装置D的作用是 。
盛满NO、NO2、O2混合气体的大试管倒置于盛水的水槽中,水面上升且充满试管,则NO、NO2、O2三种气体的体积比不可能是

| A.5 : 6 : 7 | B.1 : 1 : 1 | C.4 : 8 : 5 | D.8 : 4 : 7 |
中新网报道美国准备试验绿色航天推进剂-离子液体火箭推进剂AF-M315E,其主要成分是羟基硝酸铵,它比肼燃烧释放能量更高,更安全、环保,预计最早将在今年进行卫星飞行试验。羟基硝酸铵的结构如图所示,下列说法不正确的是
| A.固态时羟基硝酸铵是离子晶体 |
| B.羟基硝酸铵中各原子共平面 |
| C.羟基硝酸铵中含有离子键和共价键 |
| D.9.6g羟基硝酸铵中含有0.2NA个离子 |
将充有n mL NO和m mL NO2气体的试管倒立于盛水的水槽中,然后通入n mL O2。m>n,则充分反应后,试管中气体在同温同压下的体积为
A. |
B. |
C. |
D. |
下面有关氨气的实验原理的分析中,不正确的是
| A.氨气的还原性可以解释氨气与氯化氢的反应实验 |
| B.NH3·H2O的热不稳定性可以解释实验室中可采用加热氨水的方法制取氨气 |
| C.检验铵盐的方法是将待检物取出少量放在试管中,加苛性钠溶液,加热,用湿润红色石蕊试纸在试管口检验是否产生氨气 |
| D.氨气极易溶解于水的性质可以解释氨气的喷泉实验 |
已知氨可以与灼热的氧化铜反应得到氮气和金属铜,用图中装置可以实现该反应(夹持装置已省略)。
回答下列问题:
(1)A中加入的物质是 ,发生反应的化学方程式是 。
(2)B中加入的物质是 ,其作用是 。
(3)实验时在C中观察到得现象是 ,发生反应的化学方程式是 。
(4)实验时在D中观察到得现象是 ,D中收集到的物质是 ,检验该物质的方法和现象是 。
常温常压下,将盛有20 mL NO2和O2的混合气体的大试管倒立在水槽中,水面上升至一定位置后不再变化,此时还有3 mL气体,则原混合气体中的NO2的体积可能是
| A.17.8 mL | B.14.8 mL | C.12.6 mL | D.12.4 mL |
32g铜与150mL一定浓度的硝酸恰好完全反应,产生的NO2和NO混合气体在标准状况下的体积为11.2L。则该硝酸的物质的量浓度为
| A.5mol/L | B.15mol/L | C.10mol/L | D.8mol/L |
铜粉放入稀硫酸溶液中,加热后无明显现象发生。当加入一种盐后,铜粉的质量减少,溶液呈蓝色,同时有气体逸出。该盐是
| A.Fe2(SO4)3 | B.Na2CO3 | C.KNO3 | D.FeSO4 |
检验试管中盛有的少量白色固体是铵盐的方法是
| A.将固体加热,用湿润的红色石蕊试纸在试管口检验,看是否变蓝 |
| B.加水溶解,用pH试纸测溶液的酸碱性 |
| C.加入NaOH溶液,加热,再滴入酚酞试液 |
| D.加入NaOH溶液,加热,用湿润的红色石蕊试纸在试管口检验,看是否变蓝 |
取铜镁合金完全溶于浓硝酸中,反应过程中硝酸被还原只产生0.896L NO2气体和0.672 L N2O4的气体(气体体积都已折算到标准状况),在反应后的溶液中加足量的氢氧化钠溶液,生成沉淀质量为3.7g。则合金中铜与镁的物质的量之比等于
| A.1 :1 | B.2 :1 | C.3 :2 | D.2 :3 |
某学习小组探究浓、稀硝酸氧化性的相对强弱,按下图装置进行实验(夹持仪器已略去)。实验表明浓硝酸能将NO氧化成NO2,而稀硝酸不能氧化NO。由此得出的结论是浓硝酸的氧化性强于稀硝酸。
可选药品:浓硝酸、3 mol/L稀硝酸、蒸馏水、浓硫酸、氢氧化钠溶液及二氧化碳。已知:氢氧化钠溶液不与NO反应,能与NO2反应。
2NO2+2NaOH====NaNO3+NaNO2+H2O
(1)实验应避免有害气体排放到空气中。装置③④⑥中盛放的药品依次是:
、 、 。
(2)装置①中发生反应的化学方程式是 。
(3)装置②的作用是 ,发生反应的化学方程式是 。
(4)若①中消耗铜片12.8g,产生的氮氧化物与O2完全反应转化为硝酸,试计算消耗标准状况下O2的体积为 L。
(5)该小组得出的结论所依据的实验现象是 。
(6)实验结束后,同学们发现装置①中溶液呈绿色,而不显蓝色。甲同学认为是该溶液中硝酸铜的质量分数较高所致,而乙同学认为是该溶液中溶解了生成的气体。同学们分别设计了以下4个实验来判断两种看法是否正确。这些方案中可行的是(选填序号字母) 。
| A.加热该绿色溶液,观察颜色变化 |
| B.加水稀释该绿色溶液,观察绿色变化 |
| C.向该绿色溶液中通入氮气,观察颜色变化 |
| D.向饱和硝酸铜溶液中通入浓硝酸与铜反应产生的气体,观察颜色变化 |
NOx是汽车尾气中的主要污染物之一。
(1)NOx能形成酸雨,写出NO2转化为HNO3的化学方程式: 。
(2)汽车发动机工作时会引发N2和O2反应,其能量变化示意图如下:
①写出该反应的热化学方程式: 。
②随温度升高,该反应化学平衡常数的变化趋势是_ 。
(3)在汽车尾气系统中装置催化转化器,可有效降低NOX的排放。
①当尾气中空气不足时,NOX在催化转化器中被还原成N2排出。写出NO被CO还原的化学方程式:
_ 。
②当尾气中空气过量时,催化转化器中的金属氧化物吸收NOX生成盐。其吸收能力顺序如下:12MgO <20CaO <38SrO<56BaO。原因是 ,元素的金属性逐渐增强,金属氧化物对NOX的吸收能力逐渐增强。
(4)通过NOx传感器可监测NOx的含量,其工作原理示意图如下:
①Pt电极上发生的是 反应(填“氧化”或“还原”)。
②写出NiO电极的电极反应式: 。
NO很容易与许多分子迅速发生反应,科学家发现在生物体中不断地产生NO,用于细胞间传递信息;NO还参与心血管系统、免疫系统以及中枢和外围神经系统的调控。
Ⅰ.(1)实验室用金属铜和稀硝酸制取NO的离子方程式为________________________。
(2)NO是有毒气体,某学生为防止污染,用分液漏斗和烧杯装配了一套简易的、能随开随用、随关随停的NO气体发生装置,如图所示。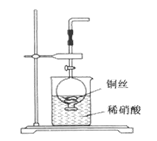
①实验室若没有铜丝,而只有小铜粒,在使用上述装置进行实验时,可用丝状材料包裹铜粒以代替铜丝进行实验,这种丝状材料的成分可以是________(填选项编号)。
| A.铁 | B.铝 | C.铂 | D.玻璃 |
②打开分液漏斗的活塞使反应进行,在分液漏斗中实际看到的气体是红棕色的,原因是________(用化学方程式表示)。
(3)以下收集NO气体的装置,合理的是________(填选项代号)。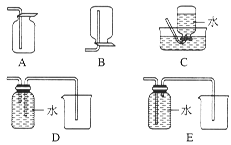
(4)假设实验中12.8 g Cu全部溶解,需要通入标况下________L O2才能使NO全部溶于水。
Ⅱ.用金属铜制取硝酸铜,从节约原料和防止环境污染的角度考虑,下列4种方法中最好的是________(填“甲”、“乙”、“丙”或“丁”)。
甲:铜 硝酸铜
硝酸铜
乙:铜 硝酸铜
硝酸铜
丙:铜 氯化铜
氯化铜 硝酸铜
硝酸铜
丁:铜 氧化铜
氧化铜 硝酸铜。
硝酸铜。