资料显示:“氨气可在纯氧中安静燃烧”。某校化学小组学生设计如下装置(图中铁夹等夹持装置已略去)进行氨气与氧气在不同条件下反应的实验。
(1)用装置A制取纯净、干燥的氨气,大试管内碳酸盐的化学式是_____ ___________。
(2)将产生的氨气与过量的氧气通到装置B(催化剂为铂石棉)中,用酒精喷灯加热:
①氨催化氧化的化学方程式是 ;试管内气体变为红棕色,该气体是__________________。
②停止反应后,立即关闭B中两个活塞。一段时间后,将试管浸入冰水中,试管内气体颜色变浅,请结合化学方程式说明原因 。
(3)将过量的氧气与A产生的氨气分别从a、b两管进气口通入到装置C中,并在b管上端点燃氨气:
①两气体通入的先后顺序是 。
②氨气燃烧的化学方程式是 。
下列说法正确的是
| A.根据反应3Fe+8HNO3=3Fe(NO3)2+2NO↑+4H2O可知:反应中HNO3表现酸性和氧化性 |
| B.根据反应H3PO3+2NaOH(足量)=Na2HPO3+2H2O可知:H3PO3属于三元酸 |
| C.根据反应5Fe2++MnO4-+8H+=5Fe3++Mn2++4H2O可知:用酸性KMnO4溶液可检验绿矾(FeSO4·7H2O)是否变质 |
| D.根据反应CuSO4+H2S=CuS↓+H2SO4可知:H2S的酸性比H2SO4强 |
某稀溶液中含有4 mol KNO3和2.5 mol H2SO4,向其中加入1.5 mol Fe,充分反应(已知NO3- 被还原为NO)。下列说法正确的是
| A.反应后生成NO的体积为28 L |
| B.所得溶液中的溶质只有FeSO4 |
| C.所得溶液中c(NO3-)="2.75" mol·L-1 |
| D.所得溶液中c(Fe2+):c(Fe3+)=1:1 |
向100 mL稀硫酸和稀硝酸的混合溶液中逐渐加入铁粉,产生气体的体积(相同状况)随铁粉质量增加的变化如图所示。下列分析错误的是.
A.原混合酸溶液的 |
B.OA段的反应为: |
C.AB段的反应为: |
| D.BC段气体产物为氢气 |
“摩尔盐”[ (NH4)2Fe(SO4)2·6H2O ] 是分析化学中的重要试剂。查阅文献得知:“摩尔盐”隔绝空气加热至500℃时可完全分解,但产物复杂。某学习小组欲探究其分解产物。
Ⅰ.【提出猜想】摩尔盐受热分解,小组同学认为分解产物可能有以下几种情况:
a.Fe2O3、SO3、NH3、H2O b.FeO、NH3、SO3、H2O
c.FeO、SO2、NH3、H2O d.Fe2O3、NH3、SO2、SO3、H2O
经认真分析,通过推理即可确定,猜想 不成立(填序号)。
Ⅱ.【实验探究】为检验分解产物,甲同学设计了如下实验装置。
请回答下列问题:
(1)B装置的容器名称是 。
(2)取一定量“摩尔盐”置于加热管A中,加热至分解完后打开K,再通入N2,目的是 。
(3)观察到A中固体逐渐变为红棕色,B、C中均产生白色沉淀。C中发生反应的离子方程式为_________________________。
(4)待A中剩余固体冷却至室温后,取少量置于试管中,加入稀硫酸溶解,再滴几滴KSCN溶液,可以观察到的现象是 。
(5)乙同学设计实验验证A中残留物不含FeO,操作方法及实验现象是:取少量A中残留物放入试管中, 。
Ⅲ.【实验反思】
乙同学认为:装置B中产生白色沉淀不能证明分解产物中一定含SO3,原因是 。
地下水中硝酸盐造成的氮污染已成为一个世界性的环境问题,某课题组利用Fe粉和酸性KNO3溶液反应模拟地下水脱氮过程,理想的脱氮原理为:4Fe + NO3- + 10H+ = 4Fe2+ + NH4+ + 3H2O。
(1)研究发现:随着KNO3溶液酸性的减弱,对应还原产物中氮元素的化合价越低。课题组用酸性弱的KNO3溶液进行实验,没有观察到气体生成,则该条件下KNO3的还原产物可能是 (化学式)。
(2)实验发现:反应一段时间后,反应体系中NH4+的浓度在增大,Fe2+的浓度却没有增大,可能的原因是 。
a.生成的Fe2+水解 b.Fe2+被氧化生成Fe3+ c.Fe2+被还原成Fe
(3)该课题组拟利用上述脱氮反应研究不同自变量对反应速率的影响。
可能用到的试剂和仪器:粗颗粒Fe粉、细颗粒Fe粉、2.0mol/L KNO3、0.1 mol/L H2SO4、蒸馏水、不同温度的恒温水浴、托盘天平、秒表、离子色谱仪等。
①设计实验方案:在不同的自变量(温度、铁粉颗粒的大小)时,测定 (要求所测得的数据能直接体现反应速率大小)。
②参照下表格式,拟定实验表格,完整体现实验方案(列出所选试剂体积、需记录的待测物理量和所拟定的数据:数据用字母表示)。
【提示】离子色谱仪能跟踪测定溶液中的c(NO3-)
| 物理量 实验序号 |
V(2.0mol/L KNO3)/ mL |
|
…… |
| 1 |
a |
|
…… |
| 2 |
a |
|
…… |
| 3 |
a |
|
…… |
③进一步的研究表明:将铁粉和活性炭同时加入上述KNO3溶液中,可以明显提高脱氮速率,其原因是 。
(本题12分)
磷是重要的非金属元素。磷单质及其化合物在工业生产中有着广泛的应用。
次磷酸钠(NaH2PO2)可用于化学镀镍等等。
完成下列填空
(1).磷原子的最外层电子排布的轨道表示式为 ______ ;氧原子核外电子云有 种不同的伸展方向,其最外层有 种不同运动状态的电子。NaH2PO2中涉及到四种元素,它们的原子半径由小到大的顺序为 。
(2).写出与磷同周期的主族元素中,离子半径最小的元素,其最高价氧化物对应水化物的电离方程式 。
(3).磷酸二氢钠主要用于制革、处理锅炉水及在食品工业、发酵工业中作缓冲剂。其水溶液呈酸性的原因是__________________________________________________。(请用文字描述)
已知Ca3(PO4)2与SiO2、C高温共热可以反应得到CaSiO3、P4蒸气和CO。
(4).写出该反应的化学方程式__________________________。
(5).每消耗24.0g碳时,有 mol电子发生转移。反应所得混合气体,折算成标况下,其气体密度为 g/L。
向一定量的Fe,FeO,Fe2O3,Fe3O4的混合物中,加入150mL 4mol/L的稀硝酸,恰好使混合物完全溶解,并放出标准状况下NO气体2.24L,往所得溶液中加KSCN溶液,无红色出现。若用一定量的氢气在加热条件下还原相同质量的该混合物,所得固体的物质的量可能为
| A.0.30 mol | B.028mol | C.0.25mol | D.0.22 mol |
制备下列物质的工业生产流程合理是
A.由SO2制亚硫酸钠: |
B.由NaCl制漂粉精: |
C.由NH3制硝酸: |
D.由乙烯制乙酸: |
(8分) “低碳”既是时尚,也是环保要求。“低碳”在工业生产中意义重大,充分利用原材料,不排放或减少排放“三废”,不同工厂今后联合生产等都是很好的“低碳”生产方式。下面是几个工厂利用废气、废渣(液)联合生产化肥硫酸铵的工艺:
请回答下列问题:
(1)工艺操作②为:____________。
(2)工业合成氨的化学方程式为:____________________。
(3)副产品的化学式为_________。该联合生产工艺中可以循环使用的物质是_________________。
(4)在实验室中检验合成氨厂排出的废气中是否含有氨气的方法是______________________。
(5)写出生成“产品”的化学方程式:_______________________
三氟化氮(NF3)是微电子工业中优良的等离子刻蚀气体,它在潮湿的环境中能发生反应:3NF3 +5H2O="=2NO" + HNO3 +9HF,下列有关该反应的说法正确的是
| A.NF3是氧化剂,H2O是还原剂 |
| B.HF是还原产物 |
| C.还原剂和氧化剂的物质的量之比是2:1 |
| D.NF3在潮湿的空气中泄漏会产生红棕色气体 |
把aL含硫酸铵、硝酸铵的溶液分成两等份,一份用b mol烧碱刚好把NH 转化为NH3,另一份与氯化钡溶液完全反应消耗c mol BaCl2。则原溶液中NO
转化为NH3,另一份与氯化钡溶液完全反应消耗c mol BaCl2。则原溶液中NO 的浓度为
的浓度为
A. |
B. |
C. |
D. |
有氯化钡稀溶液甲乙两试管分别通入SO2至饱和,若向甲试管中加入足量硝酸,乙试管中加入足量氢氧化钠溶液,则下列叙述正确的是
| A.甲、乙两试管都有白色沉淀生成 |
| B.甲、乙两试管都没有白色沉淀生成 |
| C.甲试管没有白色沉淀生成而乙试管有 |
| D.甲试管有白色沉淀生成而乙试管没有 |
实验是化学学习的基础。下列实验叙述正确的是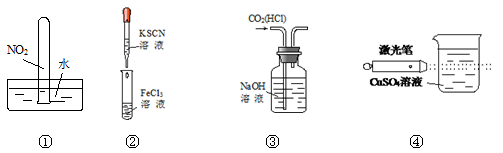
| A.实验①试管最终会充满水 |
| B.实验②试管中溶液变为血红色 |
| C.可用实验③装置除去CO2气体中含有的少量HCl杂质 |
| D.实验④检验硫酸铜溶液 |
下列除去杂质的操作方法正确的是
| A.NO中有少量的NO2:用水洗涤后再干燥 |
| B.食盐中有少量的NH4Cl:加过量的烧碱溶液后加热蒸干 |
| C.N2中有少量的O2:通过足量灼热的氧化铜 |
| D.硝酸中溶有少量NO2,可向硝酸中加入少量水,使NO2与水反应生成硝酸。 |