某实验过程如图所示,则图③试管中的现象是( )

| A.铜片溶解,产生无色气体,该气体遇空气变为红棕色 |
| B.铜片溶解,产生无色气体,该气体遇到空气不变色 |
| C.铜片溶解,放出红棕色有刺激性气味的气体 |
| D.无明显现象,因稀硫酸不与铜反应 |
氮及其化合物之间可以互相转化,请按照要求回答下列问题:
(1)实验室制取氨气。
① 实验室制取氨气的反应原理是利用了 类物质与 类物质的反应。
② 可用向下排空气法收集氨气的原因是 。
③ 用水吸收多余的氨气时,如将导管直接插入水中, 会产生倒吸现象,产生该现象的原因是 。
(2)完成下列能生成NO的化学方程式:
① 体现N元素的还原性:氨的催化氧化:____________。
② 体现N元素的氧化性:____________。
右图是用于干燥、收集并吸收多余气体的装置,下列方案正确的是( )
| 选项 |
X |
收集气体 |
 Y Y |
| A |
碱石灰 |
氯化氢 |
水 |
| B |
碱石灰 |
氨气 |
水 |
| C |
氯化钙 |
二氧化硫 |
氢氧化钠 |
| D |
氯化钙 |
一氧化氮 |
氢氧化钠 |
a mol Cu与含b mol HNO3的溶液恰好完全反应,则被还原的HNO3的物质的量一定是
| A.(b-2a) mol | B. mol mol |
C. mol mol |
D.2a mol |
下列有关硫酸和硝酸的叙述正确的是( )
| A.将浓硫酸和浓硝酸分别长期露置在空气中,浓度均会降低 |
| B.在常温下,浓硫酸和浓硝酸均能与铜剧烈反应 |
| C.稀硫酸和稀硝酸分别与金属反应时,S和N的化合物都会发生变化 |
| D.因为浓硫酸和浓硝酸都能与铁反应,所以常温下二者都不能用铁剂容器盛装 |
无色的混合气体甲,可能含有NO、CO2、NO2、NH3、N2中的某几种。将100mL甲气体经过下图实验的处理,结果得到酸性溶液,而几乎无气体剩余。则甲气体的组成为
| A.NH3、NO、CO2 | B.NH3、NO2、N2 |
| C.NH3、NO2、CO2 | D.NO、CO2、N2 |
以下物质间的每步转化都是通过一步反应能实现的是
| A.Al→Al2O3→Al(OH)3→NaAlO2 | B.Fe→FeO→Fe(OH)2→Fe(OH)3 |
| C.S→SO3→H2SO4→MgSO4 | D.N2→NO→NO2→HNO3 |
下列事实,可以证明氨水是弱碱的是
| A.氨水能跟氯化亚铁溶液反应生成氢氧化亚铁 |
| B.铵盐受热易分解 |
| C.0.1mol/L的氨水可以使酚酞试液变红 |
| D.0.1mol/L的NH4Cl溶液的pH约为5 |
下列说法正确的是
| A.铵盐不稳定,受热分解都产生氨气 |
| B.N2是空气中的主要成分之一,雷雨时可直接转化为NO2 |
| C.由于浓硫酸有强氧化性,因此不能用铁罐贮存浓硫酸 |
| D.Cl2与石灰乳反应可以制得含氯漂白剂 |
某混合气体中可能含有Cl2、O2、SO2、NO、NO2中的两种或多种气体,现将此无色混合气体通过品红溶液后,品红溶液褪色,把剩余气体排入空气中,很快变为红棕色,对于原混合气体成分的判断中正确的是
| A.肯定有NO和NO2 | B.肯定有SO2和NO |
| C.可能有Cl2和O2 | D.肯定没有Cl2、NO2,可能有O2 |
常温下,下列各组物质中,Y既能与X反应又能与Z反应的是( )
| |
X. |
Y |
Z |
| ① |
NaOH溶液 |
Al(OH)3 |
稀硫酸 |
| ② |
KOH溶液 |
SiO2 |
浓盐酸 |
| ③ |
O2 |
N2 |
H2 |
| ④ |
FeCl3溶液 |
Cu |
浓硝酸 |
A.①③ B.①④ C.②④ D.②③
下列反应起到了氮的固定作用的是( )
| A.N2和H2在一定条件下反应生成NH3 |
| B.NO和O2反应生成NO2 |
| C.NH3经催化氧化生成NO |
| D.由NH3制碳铵(碳酸氢铵)和硫铵(硫酸铵) |
下列有关氮元素及其化合物的表示正确的是
A.质子数为7、中子数为8的氮原子: |
B.溴化铵的电子式: |
C.氮原子的结构示意图: |
D.间硝基甲苯的结构简式: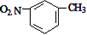 |