氢氟酸是一种弱酸,可用来刻蚀玻璃。已知25℃时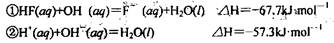
在20mL 0.1mol L-1氢氟酸中加入VmL 0.1 mol
L-1氢氟酸中加入VmL 0.1 mol L-1NaOH溶液,下列说法正确的是
L-1NaOH溶液,下列说法正确的是
常温下,向 20 mL 0.1 mol·L-1CH3COOH溶液中滴加0.1 mol·L-1NaOH溶液。下列说法正确的是
| A.当溶液的pH=7时:c(Na+) = c(CH3COO-) + c(CH3COOH) |
| B.当加入10 mL 0.1 mol·L-1NaOH溶液时:c(CH3COO-) +2 c(OH-) = c(CH3COOH) + 2c(H+) |
| C.当加入20 mL 0.1 mol·L-1NaOH溶液时:c(Na+) >c(OH-) >c(CH3COO-) > c(H+) |
| D.滴定过程中可能有:c(CH3COOH) >c(H+) >c(CH3COO-) >c(Na+) >c(OH-) |
在不同温度下,水溶液中c(H+)与c(OH-)有如图所示关系。下列条件关于离子共存说法中正确的是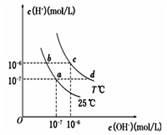
| A.d点对应的溶液中大量存在:Na+、K+、ClO-、Cl— |
| B.b点对应的溶液中大量存在:Fe2+、Ba2+、K+、NO3- |
| C.c点对应的溶液中大量存在:Na+、Ba2+、Cl-、Al3+ |
| D.a点对应的溶液中大量存在:CO32-、Na+、Cl-、SO42- |
常温下,用 0.1000 mol·L-1NaOH溶液滴定20.00 mL0.1000 mol·L-1CH3COOH溶液所得滴定曲线如右图.
下列说法正确的是 ( )
A.点 ①所示溶液中:c(CH3COO—) +2 c(OH—) = c(CH3COOH) + 2c(H+) ①所示溶液中:c(CH3COO—) +2 c(OH—) = c(CH3COOH) + 2c(H+) |
| B.点②所示溶液中:c(Na+)<c(CH3COO—) + c(CH3COOH) |
| C.点③所示溶液中:c(Na+)>c(OH—)>c(CH3COO—)> c(H+) |
| D.滴定过程中可能出现: c(CH3COOH)>c(H+)>c(CH3COO—)>c(Na+)>c(OH—) |
在25mL 0.1mol/L NaOH溶液中逐滴加入0.2mol/L CH3COOH溶液,曲线如图所示,下列有关离子浓度关系的比较,正确的是 
A.在A、B间任一点,溶液中一定都有c(Na+)>c(CH3COO-)>c(OH-)>c(H+)
B.在B点,a>12.5,且有c(Na+)=c(CH3COO-)=c(OH-)=c(H+)
C.在C点:c(CH3COO-)>c(Na+)> c(OH—)>c(H+)
D.在D点:c(CH3COO-)+ c(CH3COOH)=2 c(Na+)
已知 时,溶液的pH
时,溶液的pH 5.1,现用
5.1,现用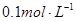 盐酸滴定20mL
盐酸滴定20mL 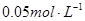 氨水,用甲基橙作指示剂,达到终点时所用盐酸的量是( )
氨水,用甲基橙作指示剂,达到终点时所用盐酸的量是( )
| A.10mL | B.5mL | C.大于10mL | D.小于5mL |
下列说法正确的是
| A.100℃时,Kw=10-12,此温度下pH=6的溶液一定显酸性 |
B.25℃时,0.1 mol/L的NaHSO3溶液pH=4,说明 在水溶液中只存在电离平衡 在水溶液中只存在电离平衡 |
| C.NH4Cl、CH3COONa、NaHCO3、NaHSO4溶于水,对水的电离都有促进作用 |
| D.25℃时,10 mL0.1 mol/LCH3COOH溶液与5 mL0.1 mol/LNaOH溶液混合,所得溶液中有2c(Na+)=c(CH3COO-)+c(CH3COOH) |
常温下下列各组离子在指定溶液中能大量共存的是( )
| A.pH=1 的溶液中:Fe2+、NO-3、SO24-、Na+ |
| B.由水电离出的 c(H+)=1×10-14mol/L 的溶液中:Ca2+、Cl-、HCO-3、K+ |
| C.c(H+)/c(OH-)=1×1012的溶液中:NH+4、Cl-、NO-3、Al3+ |
| D.c(Fe3+)=0.1mol/L 的溶液中:K+、ClO-、SO42-、SCN- |
一定温度下,水溶液中H+和OH-的浓度变化曲线如图,下列说法正确的是( )
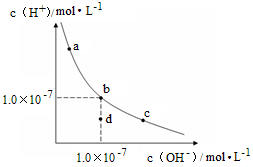
| A.升高温度,可能引起由c向b的变化 |
| B.该温度下,水的离子积常数为1.0×10-13 |
| C.该温度下,加入FeCl3可能引起由b向a的变化 |
| D.该温度下,稀释溶液可能引起由c向d的变化 |
常温下,下列各组离子在相应的条件下可能大量共存的是
| A.能使pH试纸变红的溶液中:CO32-、K+、Cl-、Na+ |
B.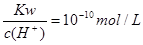 的溶液中:Na+、HCO3-、Cl-、K+ 的溶液中:Na+、HCO3-、Cl-、K+ |
| C.在c(OH-)/c(H+)=1×1012的溶液中:NH4+、Fe2+、Cl-、NO3- |
| D.由水电离产生的c(OH-)=1×10-12mol/L的溶液中:NO3-、Mg2+、Na+、SO42- |
用滴定法测定Na2CO3(含NaCl杂质)的质量分数,下列操作会引起测定值偏高的是( )
| A.试样中加入酚酞作指示剂,用标准酸液进行滴定 |
| B.滴定管用蒸馏水洗涤后,直接注入标准酸液进行滴定 |
| C.锥形瓶用蒸馏水洗涤后,直接加入待测溶液进行测定 |
| D.滴定管用蒸馏水洗涤后,直接注入待测液,取20.00mL进行滴定 |
40℃时,在氨-水体系中不断通入CO2,各种离子变化趋势如下图所示。下列说法不正确的是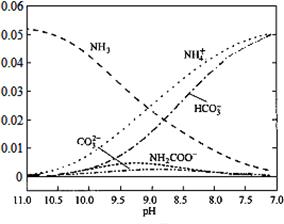
| A.在pH=9.0时,c(NH4+)>c(HCO3-)>c(NH2COOˉ)>c(CO32-) |
| B.不同pH的溶液中存在关系:c(NH4+)+c(H+)=2c(CO32-)+c(HCO3-)+c(NH2COOˉ)+c(OHˉ) |
C.随着CO2的通入,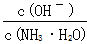 不断增大 不断增大 |
| D.在溶液中pH不断降低的过程中,有含NH2COOˉ的中间产物生成 |
室温下,将1.000mol•L-1盐酸滴入20.00mL 1.000mol•L-1氨水中,溶液pH和温度随加入盐酸体积变化曲线如图所示.下列有关说法正确的是( )

| A.a点由水电离出的c(H+)=1.0×10-14mol•L-1 |
| B.b点:c(NH4+)+c(NH3•H2O)=c(Cl-) |
| C.c点:c(Cl-)=c(NH4+) |
| D.d点后,容易温度略下降的主要原因是NH3•H2O电离吸热 |
下列有关说法不正确的是
A.将物质的量浓度为10-3mol/L的醋酸和pH=11的NaOH溶液等体积混合后,溶液显碱性
B.上图可表示常温下,稀释HA、HB两种酸的稀溶液时,溶液pH随加水量的变化,则同浓度的NaA溶液的pH大于NaB溶液
C.25℃时,pH=2的1.0 L 醋酸溶液中水电离出的H+的数目为10-12NA
D.某吸热反应能自发进行,则该反应一定是熵增的反应