下列说法错误的是( )
| A.碱性锌锰电池是二次电池 |
| B.铅蓄电池是二次电池 |
| C.二次电池又叫蓄电池,它放电后可以再充电使活性物质获得再生 |
| D.燃料电池的活性物质没有储存在电池内部 |
关于下列装置说法正确的是
| A.装置①中,盐桥中的K+移向CuSO4溶液 |
| B.用装置②精炼粗铜,电解液浓度保持不变 |
| C.可以用装置②在铜上镀银,c极为银 |
| D.装置③中一段时间后会有Fe(OH)2生成 |
铅蓄电池的电池反应为 Pb(s)+PbO2(s)+2H2SO4(aq) 2PbSO4(s)+2H2O(l),下列说法错误的是
2PbSO4(s)+2H2O(l),下列说法错误的是
| A.放电时电解质溶液的H+浓度逐渐减小 |
| B.利用铅蓄电池电解饱和食盐水制得Cl2 0.050 mol,这时电池内消耗的H2SO4的物质的量至少0.10 mol |
| C.充电时阴极的电极反应为 PbSO4(s) + 2e-="Pb(s)" + SO42-(aq) |
| D.放电时负极材料质量减小 |
Li﹣Al/FeS电池是一种正在开发的电动车用二次电池,该电池反应式为:2Al+6Li++3FeS=2Al3++3Li2S+3Fe.有关该电池的下列说法中,错误的是( )
| A.作为二次电源,该电池在使用的过程中至少存在3种形式的能量转化 |
| B.Li﹣Al在电池中作为负极材料,负极的电极反应式为Li﹣e﹣=Li+ |
| C.该电池替代现在电动车广泛使用的铅蓄电池可以减少重金属的污染 |
| D.充电时,阳极发生的电极反应式为:Li2S+Fe﹣2e﹣=2Li++FeS |
2013年3月我国科学家报道了如图所示的水溶液锂离子电池体系,下列叙述错误的是( )
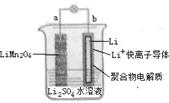
| A.a为电池的正极 |
| B.电池充电反应为LiMn2O4=Li1-xMn2Ox+xLi |
| C.放电时,a极锂的化合价发生变化 |
| D.放电时,溶液中Li+从b向a迁移 |
随着各地“限牌”政策的推出,电动汽车成为汽车届的“新宠”。特斯拉全电动汽车使用的是钴酸锂(LiCoO2)电池,其工作原理如图,A 极材料是金属锂和碳的复合材料(碳作为金属锂的载体),电解质为一种能传导Li+的高分子材料,隔膜只允许特定的离子通过,电池反应式LixC6+Li1﹣xCoO2 C6+LiCoO2.下列说法不正确的是
C6+LiCoO2.下列说法不正确的是
| A.据题意分析可知该隔膜只允许Li+通过,放电时 Li+从左边流向右边 |
| B.充电时,A为阴极,发生还原反应 |
| C.放电时,B为正极,电极反应式为:Li1﹣xCoO2+xLi++xe﹣=LiCoO2 |
| D.废旧钴酸锂(LiCoO2)电池进行“放电处理”让Li+进入石墨中而有利于回收 |
某酒精检测仪是以酸性燃料电池原理设计的,负极上的反应为:CH3CH2OH-4e-+ H2O=CH3COOH + 4H+。下列有关说法不正确的是
| A.检测时,电解质溶液中的H+向正极移动 |
| B.若有0.4mol电子转移,则在标准状况下消耗2.24L氧气 |
| C.电池反应的化学方程式为:CH3CH2OH + O2 = CH3COOH + H2O |
| D.正极上发生的反应为:O2 + 4e-+ 2H2O = 4OH- |
LED产品的使用为城市增添色彩。下图是氢氧燃料电池驱动LED发光的一种装置示意图。下列有关叙述正确的是
| A.a处通入O2 |
| B.b处为电池正极,发生了还原反应 |
| C.通入O2的电极发生反应:O2+4e-+4H+ = 2H2O |
| D.该装置将化学能最终转化为电能 |
高铁电池是一种可逆电池,该电池能长时间保持稳定的放电电压。高铁电池总反应为3Zn+2K2FeO4+8H20 3Zn(OH)2+2Fe(OH)3+4KOH。下列判断不正确的是
3Zn(OH)2+2Fe(OH)3+4KOH。下列判断不正确的是
| A.放电时,负极反应为Zn-2e-+2OH一=Zn(OH)2 |
| B.充电时,阴极pH增大 |
| C.放电时,若有6mol电子转移,则正极有10 mol OH一移向负极 |
| D.充电时,阳极反应为Fe(OH)3+5OH一+3e一=FeO42-+4H2O |
Mg-H2O2电池可用于驱动无人驾驶的潜航器。该电池以海 水为电解质溶液,示意图如下。该电池工作时,下列说法不正确的是

| A.Mg电极是该电池的负极 |
| B.H2O2在石墨电极上发生H2O2+2e-═2OH- |
| C.若隔膜为阳离子交换膜,则正极区有白色沉淀 |
| D.溶液中Cl-向正极移动 |
下列说法中正确的是
| A.在船体上镶嵌锌块,可以减缓船体被海水腐蚀的速率 |
| B.粗铜精炼时,电解液中的c(Cu2+)保持不变 |
| C.纯银在空气中久置变黑发生的是电化学腐蚀 |
| D.阴极电保护法是将被保护的金属与外加电源的正极相连 |
如图是利用一种微生物将废水中的有机物(假设是淀粉)的化学能直接转化为电能,并利用此电能在铁上镀铜,下列说法中正确的是
| A.质子透过离子交换膜由右向左移动 |
| B.铜电极应与X相连接 |
| C.M电极反应式:(C6H10O5)n + 7nH2O-24ne-= 6nCO2↑+ 24nH+ |
| D.当N电极消耗0.25 mol气体时,则铁电极增重16 g |
2015年斯坦福大学研究人员研制出一种可在一分钟内完成充放电的超常性能铝离子电池,内部用AlCl4–和有机阳离子构成电解质溶液,其放电工作原理如下图所示。下列说法不正确的是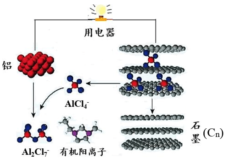
| A.放电时,铝为负极、石墨为正极 |
| B.放电时,有机阳离子向铝电极方向移动 |
| C.放电时的负极反应为:Al –3e- + 7AlCl4– = 4Al2Cl7– |
| D.充电时的阳极反应为:Cn + AlCl4––e- = CnAlCl4 |
一种微生物燃料电池如图所示,下列关于该电池说法正确的是
| A.a电极发生还原反应 |
| B.H+由右室通过质子交换膜进入左室 |
| C.b电极反应式为:2NO3-+10e-+12H+=N2↑+6H2O |
| D.电池工作时,电流由a电极沿导线流向b电极 |