下列反应完成后没有沉淀的是
| A.BaCl2溶液与Na2SO3溶液加足量稀HNO3 |
| B.Ba(OH)2溶液与KNO3溶液加足量稀H2SO4 |
| C.AgNO3溶液与Na2CO3溶液加足量稀盐酸 |
| D.Ca(OH)2溶液与FeCl3溶液加足量稀HNO3 |
下列物质间不能发生离子反应的是
| A.Na2SO4溶液与BaCl2溶液 | B.铝片插入Hg(NO3)2溶液 |
| C.NaNO3溶液与KCl溶液 | D.Na2CO3溶液与稀盐酸 |
在人类社会的发展进程中,金属起着重要的作用。
(1)以下有关金属单质的叙述正确的是。
A.金属钠非常活泼,在实验室中保存在石蜡油或煤油中
B.用坩埚钳夹住一小块铝箔,在酒精灯上加热,可观察到铝箔熔化,并有熔融物滴下
C.铁单质与水蒸气反应的化学方程式为:2Fe+3H2O(g) Fe2O3+3H2
Fe2O3+3H2
(2)把NaOH、MgCl2、AlCl3三种固体组成的混合物溶于足量水后,产生1.16g白色沉淀,再向所得浊液中逐渐加入1.00mol/LHCl溶液,加入HCl溶液的体积与生成沉淀的关系如图所示。

①A点的沉淀物的化学式为 。
②写出A点至B点发生反应的离子方程式: 。
③某溶液中溶有MgCl2和AlCl3两种溶质,若把两者分开,应选用的试剂为: 。
④原混合物中NaOH的质量是 g,C点(此时沉淀恰好完全溶解)HCl溶液的
体积为 mL。
下列化学反应的离子方程式错误的是( )
| A.Al(OH)3与盐酸反应:Al(OH)3+3H+===Al3++3H2O |
| B.Al2O3溶于过量NaOH溶液:Al2O3+2OH-===2AlO+H2O |
| C.铁溶于稀H2SO4中:2Fe+6H+===2Fe3++3H2↑ |
| D.Al(OH)3溶于NaOH溶液:Al(OH)3+OH-===AlO+2H2O |
在过量FeSO4溶液中加入稀硫酸,再滴入几滴NaClO溶液,溶液立即变黄。
(1)上述反应的离子方程式为____________________________。
(2)为检验上述反应中的氧化产物,取少许上述反应后的溶液,加入KSCN溶液,溶液变红,证明氧化产物为Fe3+;为检验上述反应中的还原产物,请填写实验操作、现象和匹配的结论:取少许上述反应后的溶液,______________________________。
(3)为证明上述反应后的溶液中仍存在过量的Fe2+,可向其中滴加_______________溶液。
下列离子方程式正确的是
A.碳酸氢钠水解:HCO3-+ H2O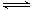 H3O++ CO32- H3O++ CO32- |
B.醋酸铵溶于水:CH3COONH4+ H2O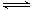 CH3COOH + NH3·H2O CH3COOH + NH3·H2O |
| C.硫酸钙悬浊液中加入碳酸钠:CaSO4(s) + CO32-(aq)=CaCO3(s) + SO42-(aq) |
| D.硫酸氢钠溶液中滴入氢氧化钡溶液呈中性:HSO4-+ OH-=SO42-+ H2O |
将0.4g NaOH和1.06 gNa2CO3混合并配成溶液,向溶液中逐滴加入0.1 mol/L的盐酸,下列图象能正确表示加入盐酸的体积和生成CO2的物质的量的关系的是
下列反应的离子方程式正确的是
A.向沸水中滴加FeCl3饱和溶液制备Fe(OH)3胶体:Fe3++3H2O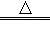 Fe(OH)3↓+3H+ Fe(OH)3↓+3H+ |
| B.向盐酸中滴加氨水:H++OH﹣═H2O |
| C.金属钠与水反应:2Na + 2H2O=2Na+ +2OH- +H2↑ |
| D.用FeCl3溶液腐蚀印刷电路铜板:Fe3++ Cu= Fe2++ Cu2+ |
有下列物质:①H2SO4;②金属铜;③Al2O3;④漂白粉;⑤蔗糖;⑥醋酸;⑦NO;⑧SiO2。
(1)请用序号填写空白:以上物质中属于混合物的是____________;能导电的是____________;属于弱电解质的是____________;能引起光化学烟雾的是____________;属于两性氧化物的是 ;可用作光导纤维原料的是 。
(2)写出H2SO4在水中的电离方程式: 。
(3)写出Al2O3溶于NaOH溶液的离子方程式:____________。
环戊二烯(  )是重要的有机化工原料,广泛用于农药、橡胶、塑料等生产。回答下列问题:
)是重要的有机化工原料,广泛用于农药、橡胶、塑料等生产。回答下列问题:
(1)已知: 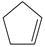 (g) =
(g) = 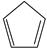 (g)+H 2(g) Δ H 1=100.3kJ·mol −1 ①
(g)+H 2(g) Δ H 1=100.3kJ·mol −1 ①
H 2(g)+ I 2(g) =2HI(g) Δ H 2=−11.0 kJ·mol −1 ②
对于反应:  (g)+ I 2(g) =
(g)+ I 2(g) = 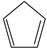 (g)+2HI(g) ③ Δ H 3=________kJ·mol −1。
(g)+2HI(g) ③ Δ H 3=________kJ·mol −1。
(2)某温度下,等物质的量的碘和环戊烯( 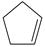 )在刚性容器内发生反应③,起始总压为10 5Pa,平衡时总压增加了20%,环戊烯的转化率为________,该反应的平衡常数 K p=________Pa。达到平衡后,欲增加环戊烯的平衡转化率,可采取的措施有________(填标号)。
)在刚性容器内发生反应③,起始总压为10 5Pa,平衡时总压增加了20%,环戊烯的转化率为________,该反应的平衡常数 K p=________Pa。达到平衡后,欲增加环戊烯的平衡转化率,可采取的措施有________(填标号)。
| A. |
通入惰性气体 |
B. |
提高温度 |
| C. |
增加环戊烯浓度 |
D. |
增加碘浓度 |
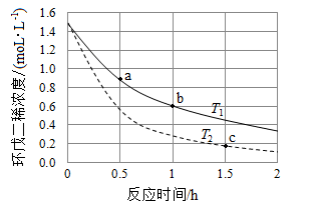
(3)环戊二烯容易发生聚合生成二聚体,该反应为可逆反应。不同温度下,溶液中环戊二烯浓度与反应时间的关系如图所示,下列说法正确的是__________(填标号)。
| A. |
T 1> T 2 |
| B. |
a点的反应速率小于c点的反应速率 |
| C. |
a点的正反应速率大于b点的逆反应速率 |
| D. |
b点时二聚体的浓度为0.45 mol·L −1 |
(4)环戊二烯可用于制备二茂铁(Fe(C 5H 5) 2结构简式为  ),后者广泛应用于航天、化工等领域中。二茂铁的电化学制备原理如下图所示,其中电解液为溶解有溴化钠(电解质)和环戊二烯的DMF溶液(DMF为惰性有机溶剂)。
),后者广泛应用于航天、化工等领域中。二茂铁的电化学制备原理如下图所示,其中电解液为溶解有溴化钠(电解质)和环戊二烯的DMF溶液(DMF为惰性有机溶剂)。
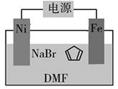

该电解池的阳极为________,总反应为________。电解制备需要在无水条件下进行,原因为________。
联氨(又称肼,N2H4,无色液体)是一种应用广泛的化工原料,可用作火箭燃料.回答下列问题:
(1)联氨分子的电子式为________,其中氮的化合价为________.
(2)实验室中可用次氯酸钠溶液与氨反应制备联氨,反应的化学方程式为________.
(3)①2O2(g)+N2(g)═N2O4(l)△H1
②N2(g)+2H2(g)═N2H4(l)△H2
③O2(g)+2H2(g)═2H2O(g)△H3
④2N2H4(l)+N2O4(l)═3N2(g)+4H2O(g)△H4=﹣1048.9kJ•mol﹣1
上述反应热效应之间的关系式为△H4=________,联氨和N2O4可作为火箭推进剂的主要原因为________.
(4) 联氨为二元弱碱,在水中的电离方式与氨相似.联氨第一步电离反应的平衡常数值为________(已知:N2H4+H+⇌N2H5+的K=8.7×107;Kw=1.0×10﹣14).联氨与硫酸形成的酸式盐的化学式为________.
(5)联氨是一种常用的还原剂.向装有少量AgBr的试管中加入联氨溶液,观察到的现象是________.联氨可用于处理高压锅炉水中的氧,防止锅炉被腐蚀.理论上1kg的联氨可除去水中溶解的O2________kg;与使用Na2SO3处理水中溶解的O2相比,联氨的优点是________.
某校学生课外活动小组为测定Na元素的相对原子质量,甲同学设计的装置如右图,该装置(包括仪器、水和干燥剂)的总质量为ag,从实验室取出b g的钠(不足量,不含煤油)放入水中,塞紧瓶塞,完全反应后再称量此装置的总质量为cg。试回答:

(1)该反应的离子方程式为 ;
(2)此干燥管的作用是 ;若此钠块有少量被氧化,则测出的相对原子质量会比实际相对原子质量 (填“偏大”、“偏小”或“不变”);
(3)乙同学认为此设计方案会使测定结果 (填“偏大”、“偏小”或“不变”),建议在图中干燥管上再连一个同样的干燥管且该干燥管不参与称质量,其目的是 ,计算钠的相对原子质量的表达式为____________;
(4)丙同学为避免由于行动不够迅速产生偏差,又建议在广口瓶中再加入一定量煤油,其目的是_ ___。
下列解释事实的离子方程式不正确的是
| A.Na放入水中,产生气体:2Na + 2H2O =2Na+ + 2OH-+ H2↑ |
| B.FeCl3溶液滴在淀粉碘化钾试纸上,试纸变蓝:2Fe3+ + 2I-= 2Fe2+ + I2 |
| C.铁溶于稀硝酸,溶液变黄:3Fe + 8H+ + 2NO3-= 3Fe2+ + 2NO↑+ 4H2O |
| D.Al片置于NaOH溶液中,产生气体:2Al + 2OH-+ 2H2O =2AlO2- + 3H2↑ |
下列反应的离子方程式书写正确的是
| A.硫酸和氯氧化钡溶液反应:Ba2++SO42-=BaSO4↓ |
| B.碳酸钠与盐酸反应:Na2CO3+2H+=2Na++CO2↑+H2O |
| C.Ca(NO3)2溶液和Na2CO3溶液混合:Ca2++CO32-=CaCO3↓ |
| D.铁钉放入硫酸铁溶液中:Fe+Fe3+=2Fe2+ |