下列叙述错误的是( )
①热稳定性:H2O>HF>H2S
②密度:K<Na<Rb
③第ⅠA、ⅡA族元素的阳离子与同周期稀有气体元素的原子具有相同的核外电子排布
④HCl的形成过程: +
+ →
→
⑤元素周期表中从ⅢB族到ⅡB族10个纵行的元素都是金属元素
⑥结合质子的能力:S2->Cl-
⑦因为常温下白磷可自燃,而氮气须在放电时才与氧气反应,所以非金属性:P>N
A.①②④⑤ B.③⑤⑥⑦ C.②④⑤⑥ D.①③④⑦
X、Y、Z、W、R是短周期元素,原子序数依次增大。X原子核外各层电子数之比为1:2, Y原子和Z原子的核外电子数之和为20,W和R是同周期相邻元素,Y的氧化物和R的氧化物均能形成酸雨。
请回答下列问题:
(1)元素X的最高价氧化物的电子式为 ;元素Z的离子结构示意图为 。
(2)单质X和元素Y的最高价氧化物对应水化物的浓溶液发生反应的化学方程式为 ,Y、W的氢化物沸点高的是______(写化学式),原因是________
(3)元素W位于周期表的第 族, 其非金属性比元素R弱,用原子结构的知识解释原因 。
(4)R的一种氧化物能使品红溶液褪色,工业上用Y的气态氢化物的水溶液做其吸收剂,写出吸收剂与足量该氧化物反应的离子方程式 。
(5)Y和Z组成的化合物ZY,被大量用于制造电子元件。工业上用Z的氧化物、X单质和Y单质在高温下制备ZY,其中Z的氧化物和X单质的物质的量之比为1:3,则该反应的化学方程式为 。
短周期元素A、B、C、D在周期表中的位置如图所示:B、D最外层电子数之和为12。回答下列问题:
(1)与元素B、D处于同一主族的第2-5周期元素单质分别与H2反应生成1 mol气态氢化物对应的热量变化如下,其中能表示该主族第4周期元素的单质生成1 mol气态氢化物所对应的热量变化是_______(选填字母编号)。
a.吸收99.7kJ b.吸收29.7kJ c.放出20.6kJ d.放出241.8 kJ
(2)DB2通过下列工艺流程可制化工业原料H2DB4和清洁能源H2。

①查得:
| 化学键 |
H-H |
Br-Br |
H-Br |
| 键能(kJ/mol) |
436 |
194 |
362 |
试写出通常条件下电解槽中发生总反应的热化学方程式: 。
②根据资料:
| 化学式 |
Ag2SO4 |
AgBr |
| 溶解度(g) |
0.796 |
8.4×10-6 |
为检验分离器的分离效果,取分离后的H2DB4溶液于试管,向其中逐滴加入AgNO3溶液至充分反应,若观察到 ,证明分离效果较好。
③在原电池中,负极发生的反应式为 。
④在电解过程中,电解槽阴极附近溶液pH (填“变大”、“变小”或“不变”)。
⑤将该工艺流程用总反应的化学方程式表示为: 。该生产工艺的优点有 (答一点即可)。
(3)溴及其化合物广泛应用于医药、农药、纤维、塑料阻燃剂等,回答下列问题:海水提溴过程中,向浓缩的海水中通入________,将其中的Br-氧化,再用空气吹出溴;然后用碳酸钠溶液吸收溴,溴歧化为Br-和BrO3-,其离子方程式为________________ 。
有A、B、C、D、E、F六种短周期元素,其原子序数依次增大,A的单质分子内不含中子,B的某种同素异形体可以用于制作铅笔芯,C是形成氧化物种类最多的元素, D2—与E2+具有相同的电子层结构,F原子的最外层电子数与其电子层数相等。
(1)A单质的结构式 ;E2+的离子结构示意图 。
(2)C、D、E、F四种元素简单离子的离子半径由大到小的排列顺序为(用离子符号表示) 。
(3)由A和C两种元素可形成多种分子,其中有一种A、C原子个数比为3:1的分子,其电子式为 ;另一种分子中其原子个数比为2:1,已知在101kPa时,32.0g该液态化合物在氧气中燃烧,其中一种生成物为C元素形成的单质,放出热量624kJ (25℃时),写出该热化学方程式 。
(4)某抗酸药物只含A、B、D、E、F五种元素,取一定量该抗酸药进行如下实验:

过量试剂a是 ;通过计算可知该抗酸药的化学式为 。
A、B、W、D、E为短周期元素,且原子序数依次增大,质子数之和为39,B、W同周期,A、D同主族,A、W能形成两种液态化合物A2W和A2W2,E元素的周期序数与主族序数相等。试回答:
(1)E元素在周期表中的位置为 ,写出E的最高价氧化物与D的最高价氧化物的水化物反应的离子方程式 。
(2)由A、B、W三种元素组成的18电子微粒的结构简式为 。
(3)经测定A2W2为二元弱酸,其酸性比碳酸的还要弱,请写出其第一步电离的电离方程式 。常用硫酸处理BaO2来制备A2W2,写出该反应的化学方程式 。
(4)废印刷电路板上含有铜,以往的回收方法是将其灼烧使铜转化为氧化铜,再用硫酸溶解。现改用A2W2和稀硫酸浸泡废印刷电路板既达到上述目的,又保护了环境,试写出反应的离子方程式 。
(5)元素D的单质在一定条件下,能与A单质化合生成一种氢化物DA,熔点为800℃。DA能与水反应放氢气,若将1mol DA和1 mol E单质混合加入足量的水,充分反应后生成气体的体积是 L(标准状况下)。
有A、B、C、D、E、F六种短周期元素,其元素特征信息如下表:
| 元素编号 |
元素特征信息 |
| A |
A的单质是密度最小的物质 |
| B |
B的单质能与冷水剧烈反应,所得强碱性溶液中含有两种电子数相同的阴、阳离子 |
| C |
C的原子最外层电子数是其内层电子数的三倍 |
| D |
D与B同周期,该周期中D的简单离子半径最小 |
| E |
B、C、E组成的36电子的化合物Y是家用消毒剂的主要成分 |
| F |
F元素最高正价与最低负价的代数和为4 |
(1)D的离子结构示意图是___________;化合物Y所含的化学键名称___________;B2C2的电子式表示为 。

(2)D、E、F的简单离子半径由大到小的顺序是(用化学式表示)________________。
(3)写出两种均含A、B、C、F四种元素的化合物在溶液中相互
反应的离子方程式 。
(4)将一定质量的Mg和D的混合物投入500mL稀硫酸中,
固体全部溶解并产生气体.待反应完全后,向所得溶液中加入
NaOH溶液,生成沉淀的物质的量与加入NaOH溶液的体积关系如图所示.则固体混合物中Mg的质量为 ;原稀硫酸溶液的物质的量浓度为 。
下表为六种短周期元素的部分性质:
| 元素代号 |
X |
Y |
Z |
Q |
R |
T |
| 原子半径/10-10m |
0.77 |
0.74 |
0.75 |
1.17 |
0.99 |
1.10 |
| 主要化合价 |
+4、-4 |
-2 |
+5、-3 |
+4、-4 |
+7、-1 |
+5、-3 |
下列有关说法错误的是( )
A.X与Y可以形成阴离子XY32-
B.Z的氢化物的沸点比T的氢化物的沸点高
C.元素R的氧化物对应的水化物一定为强酸
D.由X形成的化合物XY2和XR4,其中XR4的沸点高
甲~庚元素在周期表中的相对位置如下表,己的最高氧化物对应水化物有强脱水性,甲和丁在同一周期,甲原子最外层与最内层具有相同电子数。下列判断正确的是( )

| A.丙与戊的原子序数相差27 |
| B.气态氢化物的稳定性:庚<己<戊 |
| C.丁的最高价氧化物可用于制造光导纤维 |
| D.常温下,甲和乙的单质均能与水剧烈反应 |
原子序数依次增大的A、B、C、D、E五种短周期元素,可以两两形成多种原子个数比为1:1的化合物,其中的甲、乙、丙、丁4种化合物有两种属于离子化合物。A、B的原子序数之和是元素D的一半。B既是组成蛋白质的必要元素,也是某些化肥的组成元素。只有C为金属元素,焰色反应呈黄色。请回答下列问题:
(1)元素E 的原子结构示意图为 。
(2)B和D形成的化合物甲,其相对分子质量在170~190之间,且D的质量分数约为70%,则该化合物的化学式为 。
(3)A和B形成的化合物乙为B4A4,在一定条件下可以电离出两种离子,其中一种为10e-的离子,该物质一定条件下的电离方程式为 。
(4)化合物C2D溶液在空气中长期放置会变质生成丙C2D2,用化学方程式表示该过程 。
(5)D和E形成的化合物丁中所有原子均满足8电子稳定结构,该化合物的电子式为 ;该物质遇水剧烈反应,产生有刺激性气味的混合气体X和Y,同时还有固体单质产生,已知X是能使品红褪色的气体,Y在标准状态下的密度为1.63g/L,该混合气体相对于H2的密度为21,上述过程对应的化学方程式为 。
某研究小组同学为确定干燥的X和Y混合气体中Y 的存在,设计方案如下:把干燥的X和Y与干燥的NH3混合,出现白烟,则证明有Y气体,你认为此方案 (填“正确”或“不正确”),理由是 。
(1)砷(As)与其化合物被广泛应用在农药、除草剂、杀虫剂以及含砷药物中。回答下列问题:
①砷是氮的同族元素,且比氮多2个电子层,砷在元素周期表中的位置: ;AsH3的热稳定性比NH3的热稳定性 (填“强”或“弱”)。
②As2O3俗称砒霜,As2O3是两性偏酸性氧化物,是亚砷酸(H3AsO3)的酸
酐,易溶于碱生成亚砷酸盐,写出As2O3与足量氢氧化钠溶液反应的离子
方程式 。
③As2S3和HNO3反应如下:As2S3+10H++10NO3-=2H3AsO4+3S+10NO2↑+2H2O,将该反应设计成原电池,则NO2应该在 (填“正极”或“负极”)附近逸出,该极的电极反应式为 。
(2)综合利用CO2对环境保护及能源开发意义重大。Li2O、Na2O、MgO均能吸收CO2。如果寻找吸收CO2的其他物质,下列建议合理的是 。
a.可在碱性氧化物中寻找
b.可在ⅠA、ⅡA族元素形成的氧化物中寻找
c.可在具有强氧化性的物质中寻找
已知A、B、C、D、E、F、G是原子序数依次递增的短周期元素,已知A和D,C和F为同一主族元素,A与B、A与G形成共价化合物,B原子的最外层电子数比次外层多3,G元素的最高正化合价与最低负化合价的代数和为6,E是同周期中离子半径最小的元素,F形成的化合物是造成酸雨的主要原因。请回答下列问题:
(1)七种元素中,非金属性最强的元素在周期表中的位置是 。
(2)由C、D形成的一种淡黄色固体的电子式 。画出G离子的结构示意图 。
(3)G元素的单质有毒,可用D的最高价氧化物对应的水化物的溶液吸收,其离子方程式为 。
(4)将两份足量的E单质分别加入到等体积等浓度的硫酸和NaOH溶液中,充分反应生成的气体的体积比为 。
(5)由A、B、C所形成的常见离子化合物是 (写化学式),该化合物与D的最高价氧化物对应的水化物的浓溶液加热时反应的离子方程式为 。
(6)已知一包白色晶体的混合物,经元素分析仪分析,包含以上七种元素中的若干种,为测定其组成,进行如下实验:
①称取固体2.37g溶于水,得到无色澄清溶液,再滴加过量的氯化钡溶液和稀盐酸,得到的白色沉淀经过滤、洗涤、干燥后,称得质量为4.66g
②再取等质量的该固体溶于水,逐滴滴加1mol/L的氢氧化钠溶液,得到的沉淀和滴加的氢氧化钠溶液体积的关系如图,该白色晶体的组成(用化学式表示)为 。

A、B、C、D、E五种短周期元素,它们的原子序数依次增大;A是元素周期表中原子半径最小的元素;B元素最高价氧化物对应的水化物与其氢化物反应生成一种盐X; D与A同主族,且与E同周期;E元素原子的最外层电子数是其次外层电子数的=3/4倍;C与E同主族。请回答下列问题:
(1)X的名称为_________,A、C、D构成的化合物中含有的化学键有 。
(2)下列各项中,能说明元素C比E非金属性强的事实有____________(填序号)。
①氢化物H2E的酸性比H2C强
②氢化物H2C的热稳定性比H2E强
③氢化物H2E的水溶液放置在空气中会变浑浊
④C与E组成化合物,C显负价
(3)将由BC和BC2组成的混合气体通入下图所示装置中,用来验证浓硝酸的氧化性比稀硝酸的氧化性强。
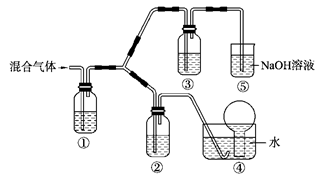
已知(ⅰ)浓硝酸能将气体BC氧化成BC2,而稀硝酸不能氧化BC。
(ⅱ)NaOH溶液与BC2反应的化学方程式为:
 2NaOH+2BC2 NaBC2+NaBC3 + H2O, NaOH溶液与BC气体不反应。
2NaOH+2BC2 NaBC2+NaBC3 + H2O, NaOH溶液与BC气体不反应。
装置①、②、③中盛放的药品依次是______、______、 ______。
(4)通入混合气体之前,应先通入一段时间某另外一种气体,试推测先通入的该气体可以是______(填一种气体的化学式)。
有A、B、C、D、E、F六种元素,原子序数依次增大,A、B、C、D、E均为短周期元素,D、F为常见金属元素。A元素原子核内只有一个质子,元素A与B形成的气态化合物甲在标准状况下的密度为0.759 g·L-1,C元素原子的最外层电子数是其电子层数的3倍,E与C同主族。均含D元素的乙(金属阳离子)、丙、丁微粒间的转化全为非氧化还原反应,均含F元素的乙(单质)、丙、丁微粒间的转化全为氧化还原反应。请回答下列问题:

(1)单质B的结构式:_____ ____。
(2)F元素周期表中的位置:_____ _____。
(3)均含有F元素的乙与丁在溶液中发生反应的离子方程式 。均含有D元素的乙与丁在溶液中发生反应的离子方程式_______ 。
(4)由A、C元素组成的化合物庚和A、E元素组成的化合物辛,相对分子质量均为34。其中庚的熔沸点比辛_________(填“高”或“低”),原因是___________________。
下表是元素周期表的一部分,针对所给的10种元素,完成下列各小题。
| 主族 周期 |
ⅠA |
ⅡA |
ⅢA |
ⅣA |
ⅤA |
ⅥA |
ⅦA |
0 |
| 2 |
|
|
|
C |
N |
O |
|
|
| 3 |
Na |
Mg |
|
Si |
|
S |
Cl |
Ar |
| 4 |
|
Ca |
|
|
|
|
|
|
(1)金属性最强的元素是 (填元素名称);
(2)第三周期中,最高价氧化物水化物酸性最强的是 (填化学式);
(3)C和N中,原子半径较小的是 ;
(4)Si是带来人类文明的重要元素之一,其氧化物常用于制造 (填一种高性能的现代通讯材料的名称);
(5)镁是一种重要的金属材料,工业上采用电解熔融氯化镁获得金属镁,该反应的化学方程式为 。
下表中列出了五种短周期元素A、B、C、D、E的信息,请推断后作答:
| 元素 |
有关信息 |
| A |
元素主要化合价为-2,原子半径为0.074nm |
| B |
所在主族序数与所在周期序数之差为4,同周期主族元素中原子半径最小 |
| C |
原子半径为0.102nm,其单质在A的单质中燃烧,发出明亮的蓝紫色火焰 |
| D |
最高价氧化物对应水化物,能按1:1电离出电子数相等(10个电子)的阴阳离子 |
| E |
原子半径为0.075nm,最高价氧化物对应水化物与其氢化物组成一种盐X |
(1)写出A、E两种元素符号 、 。
(2)画出B原子的核外电子排布式: ;写出D元素最高价氧化物对应水化物的电子式: 。
(3)盐X水溶液显 (选填“酸”、“碱”或“中”)性,用离子方程式解释其原因: 。
(4)D2CA3的溶液与B的单质能发生氧化还原反应,其反应的离子方程式为 。
(5)已知E元素的某种氢化物Y与A2的摩尔质量相同,Y在常温下为液态,Y的化学式为 ,Y所含的化学键为 。
(a)极性键 (b)非极性键 (c)离子键