只含碳、氢、氧的有机物,为便于研究其燃烧时,生成物与所需氧气的量的关系,可用通式(CxHy)m(H2O)n或(CxOy)m(H2O)n表示它们。(m、n、x、y 均为正整数)
例如:CH3OH、C2H5OH、C3H7OH等物质可用通式(CH2)m(H2O)n表示,其m分别为1,2,
3,n均为1。它们燃烧时所需的氧气和生成的二氧化碳的体积比均为3∶2。
(1)现有一类只含C、H、O的有机物。它们燃烧时所需消耗的氧气和生成的二氧化碳的体积比为5∶4(相同状况),按照上述要求,该类化合物的通式可表示为
(2)写出这类化合物分子量最小的物质的结构简式 。
(3)写出这类化合物中生成CO2与H2O的物质的量之比为1∶1,且能发生水解反应的物质的分子式 ,该物质能发生水解的同分异构体有 种。
(4)若某一类有机物可用通式(CxOy)m(H2O)n表示,则在相同的条件下,该类化合物完全燃烧时消耗的氧气体积为V1和生成的CO2体积为V2,则V1、V2必须满足的条件是
。
(5)现有一种有机物,它完全燃烧时,消耗氧气与生成CO2的体积比为3∶4,它具有两个羧基,其余的碳原子与相同的原子或原子团结合,取0.2625g该化合物恰好能与2500ml
0.10 00mol·L-1的NaOH完全中和,由此可知该化合物的分子式应是
结构简式为 。
有机物A是一种纯净的无色黏稠液体,易溶于水。为研究A的组成与结构,进行了如下实验:
| 实验步骤 |
解释或实验结论 |
| (1)称取A物质 18.0 g,升温使其汽化,测其密度是相同条件下H2的45倍。 |
试通过计算填空: (1)A的相对分子质量为_ _ |
(2)A的核磁共振氢谱如图: |
(2)A中含有_____种氢原子 |
| (3)另取A 18.0 g与足量的NaHCO3粉末反应,生成0.2 mol CO2,若与足量钠反应则生成0.2 mol H2。 |
(3)写出一个A分子中所含官能团的名称和数量___ |
| (4)将此18.0 g A在足量纯O2中充分燃烧,并使其产物依次缓缓通过浓硫酸、碱石灰,发现两者依次增重10.8 g和26.4 g。 |
(4)A的分子式为____ |
| (5)综上所述A的结构简式____ ___。 |
2012年2月20日《南方日报》A12版报道了如下几种饮料添加剂:对羟基苯甲酸甲酯、苯甲酸钠、塑化剂等,请回答以下相关问题:
(1)对羟基苯甲酸甲酯的分子式为________。请写出对羟基苯甲酸甲酯符合下列所有条件的任意一种同分异构体________。
A.有醛基 B.有苯环 C.苯环上氢只有一种
(2)苯甲酸钠________(填“难”或“易”)溶于水,其水溶液显________(选填“酸”、“碱”或“中”)性,理由是____________________________________________________________(用离子方程式表示)。
(3)邻苯二甲酸二丁酯是塑化剂之一,它的另外两种性质基本相同的同分异构体是______________________________________________________________________
乙烷和乙炔混合物共m mol,与n mol的氧气点燃后完全反应,得到CO和CO2的混合气体,以及36g水。试求:
(1)当m=0.8时,乙烷和乙炔的物质的量之比 。
(2)当m=1时,且反应后CO和CO2混合气体的物质的量是反应前氧气的物质的量的5/6时,则n= ,得到的CO和CO2的物质的量之比 。
(3)m的取值范围是 ,n的取值范围是 。
醇脱水是合成烯烃的常用方法,实验室合成环己烯的反应方程式和实验装置如下: 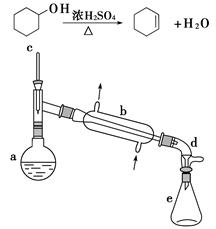
可能用到的有关数据如下:
| |
相对分 子质量 |
密度/ (g·cm-3) |
沸点/℃ |
溶解性 |
| 环己醇 |
100 |
0.961 8 |
161 |
微溶于水 |
| 环己烯 |
82 |
0.810 2 |
83 |
难溶于水 |
合成反应:
在a中加入20 g环己醇和2小片碎瓷片,冷却搅动下慢慢加入1 mL浓硫酸。b中通入冷却水后,开始缓慢加热a,控制馏出物的温度不超过90 ℃。
分离提纯:
反应粗产物倒入分液漏斗中分别用少量5% 碳酸钠溶液和水洗涤,分离后加入无水氯化钙颗粒,静置一段时间后弃去氯化钙。最终通过蒸馏得到纯净环己烯10 g。
(1)装置b的名称是__________。
(2)加入碎瓷片的作用是________;如果加热一段时间后发现忘记加瓷片,应该采取的正确操作是________(填正确答案序号)。
A.立即补加 B.冷却后补加
C.不需补加 D.重新配料
(3)本实验中最容易产生的副产物的结构简式为______________。
(4)分液漏斗在使用前必须清洗干净并______。在本实验分离过程中,产物应该从分液漏斗的________(填“上口倒出”或“下口倒出”)。
(5)分离提纯过程中加入无水氯化钙的目的是__________________。
(6)在环已烯粗产物蒸馏过程中,不可能用到的仪器有______(填正确答案序号)。
A.圆底烧瓶 B.温度计 C.吸滤瓶 D.球形冷凝管 E.接收器
为了测定某饱和卤代烃的分子中卤原子的种类和数目,可按下列步骤进行实验: 回答下列问题:
回答下列问题:
(1)准确量取11.40 mL液体所用仪器是________;
(2)加入过量硝酸的作用是___________________________________________;
(3)加入AgNO3溶液时产生的沉淀为浅黄色,则此卤代烃中的卤原子是________;
(4)已知此卤代烃液体的密度是1.65 g/mL,其蒸气对甲烷的相对密度是11.75,则此卤代烃每个分子中卤原子的数目为_______个;此卤代烃的结构简式为: _。
乌尔曼反应是偶联反应的一种,可以实现卤代苯与含氮杂环的反应。例如:
(1)化合物(Ⅰ)的分子式为 ;
(2)化合物Ⅳ是化合物Ⅱ的同系物,分子式为C8H9Br,Ⅳ为苯的对位二取代物,其核磁共振氢谱图共有4组峰,峰面积比为2:2:2:3,其结构简式为 (任写一种)。
(3)1mol化合物Ⅲ可以与 mol H2发生加成反应,产物结构简式为 。
(4)化合物Ⅳ的一种同分异构体Ⅴ的结构简式为 ,Ⅴ与氢氧化钠溶液醇溶液加热条件下反应的化学方程式为 。
,Ⅴ与氢氧化钠溶液醇溶液加热条件下反应的化学方程式为 。
(5)一定条件下, 与
与 也可以发生类似反应①的反应,参加反应的分子数之比为2:1,则生成的产物的结构简式为 。
也可以发生类似反应①的反应,参加反应的分子数之比为2:1,则生成的产物的结构简式为 。
(4分)核磁共振谱是测定有机物分子结构最有用的工具之一。瑞士科学家维特里希等三人即是利用核磁共振技术测定生物大分子的三维结构而获得2002年诺贝尔化学奖。在有机物分子中,不同位置的氢原子在质子核磁共振谱(PMR)中给出的峰值(信号)也不同,根据峰(信号)可以确定有机物分子中氢原子的种类和数目。例如:乙醛的结构式为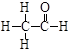 ,其PMR谱中有2个信号峰,其强度之比为3∶1。
,其PMR谱中有2个信号峰,其强度之比为3∶1。
(1)下列有机物分子中,在质子核磁共振谱中只给出一种峰(信号)的是________。
| A.CH3—CH3 | B.CH3CHO |
| C.CH3CH2OCH2CH3 | D.CH3COCH3 |
(2)化合物A和B的分子式都是C2H4Br2,A的PMR谱上只有1个峰,则A的结构简式为___________。B的PMR谱上有__________________个峰,强度比为________________。
(1)标准状况下,2.24LCH4、HCHO、C2H6的混合气充分燃烧后,生成CO2 0.14mol,该混合气体中C2H6的体积分数
(2)某气态不饱和烃在标准状况下的密度为2.41g/ L。取0.54 g该烃恰好与浓度为0.2 mol / L的溴水100mL完全反应,使溴水完全褪色。求该烃的分子式及结构简式
下图为苯和溴的取代反应的改进实验装置图。其中A为具支试管改制成的反应容器,在其下端开了一小孔,塞好石棉绒,再加入铁屑粉少量。
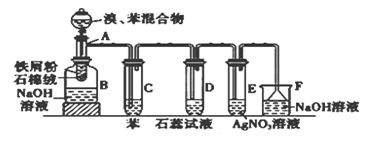
填写下列空白:(注:溴苯与NaOH溶液不可以发生水解反应)
(1)向反应容器A中逐滴加入溴和苯的混合液,几秒钟内就发生反应。写出A中所有反应的化学方程式___________________________。
(2)试管C中苯的作用是________________;反应开始后,观察D和E试管,看到的现象为D中___________;E中 ;
(3)在上述整套装置中,具有防倒吸的仪器有___________________(填字母)
(4)改进后的实验除①步骤简单,操作方便,成功率高;②各步现象明显;③对产品便于观察这3个优点外,还有一个优点是_______________。
某含苯环的化合物A,其相对分子质量为104,碳的质量分数为92.3%。
(1)A的分子式为 :
(2)A与溴的四氯化碳溶液反应的化学方程式为
(3)已知: 。请写出A与稀、冷的KMnO4溶液在碱性条件下反应的化学方程式 ;
。请写出A与稀、冷的KMnO4溶液在碱性条件下反应的化学方程式 ;
反应类型是 ;
(4)一定条件下,A与氢气反应,得到的化合物中碳的质量分数为85.7%,写出此化合物的结构简式 ;
(10分,每小题2分,共5小题)
(1)某炔烃B和H2充分加成后生成2,5-二甲基己烷,则B的结构简式为 ;
(2)碳原子数在10以内的烷烃的所有同分异构体中,一氯代物无同分异构体的有( )种
(3)某一元羧酸A,含碳的质量分数为50.0%,氢气、溴、溴化氢都可以跟A起加成反应。试求:A的结构简式
(4)在一定质量的烧瓶中盛10g11.6%的某醛溶液,然后与足量的银氨溶液充分混合放在热水浴中加热,安全反应后,倒去瓶中液体,仔细洗净、烘干后,烧瓶质量增加4.32g,通过计算,写出这种醛的结构简式
(5)0.2 mol某有机物和0.4 mol O2在密闭容器中燃烧后,产物为CO2、CO和H2O,产物经过浓H2SO4后,浓H2SO4增重10.8 g,通过灼热的CuO充分反应后,CuO失重3.2 g,最后通过碱石灰,碱石灰增重17.6 g。若等量该有机物与9.2 g 钠恰好反应。计算并回答:该有机物的名称 。
金属单质及其化合物常应用于有机物的反应和分析之中,某芳香族化合物A分子式为C8H10O2 为测定其结构做如下分析:
(1)为确定羟基的个数, 将1mol A与足量钠反应生成氢气22.4L(标准状况下),说明A分子中含羟基 个。
(2)核磁共振氢谱显示A有3个峰,峰面积之比为1:2:2,该物质的结构简式为 。
(3)A在Cu催化下可被氧气氧化生成有机物B,B的相对分子质量比A小4。试写出反应的方程式 。
(4)1mol B与足量银氨溶液充分反应生成有机物C,同时得到银 克。将生成的有机物C酸化后得到有机物D。已知A,D在一定条件下可缩聚生成高分子化合物E。写出E在足量NaOH溶液中水解的化学反应方程式
(5)有机物F是有机物B的一种同分异构体。1mol F与足量钠反应同样生成氢气22.4L(标准状况下),且F能使氯化铁溶液显紫色。试写出满足此条件的有机物F的结构简式 (只写出一种即可)。