某实验小组用燃烧分析法测定某有机物中碳和氢等元素的含量,随后又对其进行了性质探究。将已称量的样品置于氧气流中,用氧化铜作催化剂,在高温条件下样品全部被氧化为水和二氧化碳,然后分别测定生成的水和二氧化碳。实验可能用到的装置如下图所示,其中A、D装置可以重复使用。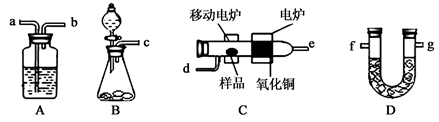
请回答下列问题:
(1)请按气体流向连接实验装置B→ →C→A→D→ (用装置编号填写)。
(2)B装置中制O2时所用的药品是 。实验中,开始对C装置加热之前,要通一段时间的氧气,目的是 ;停止加热后,也要再通一段时间的氧气,目的是 .。
(3)已知取2.3g的样品X进行上述实验,经测定A装置增重2.7g,D装置增重4.4g。试推算出X物质的实验式 。
(4)该小组同学进一步实验测得:2.3g的 X与过量金属钠反应可放出560mLH2(已换算成标准状况下),且已知X分子只含一个官能团。查阅资料后,学生们又进行了性质探究实验:实验一:X在一定条件下可催化氧化最终生成有机物Y;实验二:X与Y在浓硫酸加热条件下生成有机物Z。则:①写出实验二中反应的化学方程式 。
② 除去Z中混有的Y所需的试剂和主要仪器是 、 。
(5)若已知室温下2.3g液态X在氧气中完全燃烧生成二氧化碳气体和液态水时可放出68.35kJ的热量,写出X在氧气中燃烧的热化学方程式 。
0.2mol某烃A在氧气中完全燃烧后,生成CO2和H2O各1.2mol。
(1)烃A的分子式为 ;
(2)若烃A不能使溴水褪色,但在一定条件下能与氯气发生取代反应,其一氯取代产物只有一种,则A 的结构简式为 ;
(3)若烃A能使溴水褪色,在催化剂作用下,与H2发生加成反应,其加成产物B经测定分子中含有4个甲基,且其核磁共振氢谱图中有两组峰,则A可能的结构简式为 ,B的名称为 。
(12分))某有机化合物A经李比希法测得其中含碳为72.0%、含氢为6.67%,其余为氧。现用下列方法测定该有机化合物的相对分子质量和分子结构。
方法一:用质谱法分析得知A的相对分子质量为150。
方法二:核磁共振仪测出A的核磁共振氢谱有5个峰,其面积之比为1∶2∶2∶2∶3,如图A所示。
方法三:利用红外光谱仪测得A分子的红外光谱如图B所示。


请填空:
(1)A的分子式为 。
(2)A的分子中含一个甲基的依据是 。
a.A的相对分子质量
b.A的分子式
c.A的核磁共振氢谱图
d.A分子的红外光谱图
(3)A的结构简式为 。
【原创】(10分)某烃类化合物A的质谱图表明其相对分子质量为84,红外光谱表明分子中含有碳碳双键,核磁共振氢谱表明分子中只有一种类型的氢。
(1)A的分子式为________。用系统命名法给化合物A命名为________。
(2)下列有关化合物A的说法正确的是________。
A.A中的碳原子处于同一平面上
B.可以做萃取剂萃取碘水中的碘
C.存在顺反异构体
D.一氯代物有2种
(3)已知A、B、C有如下转化关系:
则反应②的化学方程式为___________________________________________________________;
①的反应类型是________。
(1)某有机物A的质量为9.2克,完全燃烧后生成0.4mol二氧化碳和10.8克水,且此有机物的蒸气的相对密度是相同状况下氢气的23倍,求:
①此有机物的分子式为
②写出该有机物可能的结构简式
(2)某烃B的相对分子质量为84。回答下列问题:
①下列物质与B以任意比例混合,若总物质的量一定,充分燃烧消耗氧气的量不相等的是(填序号) 。
a.C7H12O2 b.C6H14 c.C6H14O d.C7H14O3
②若链烃B分子中所有的碳原子共平面,该分子的一氯取代物只有一种, 则B的结构简式为 。
③若烃B不能使溴水褪色,并且其一氯代物只有一种,则B的结构简式为 。
(3)C1(一碳化学)是以含一个碳原子的化合物如:甲烷(CH4)、合成气(CO和H2)、CO2、CH3OH、HCHO等为初始反应物,反应合成一系列重要的化工原料和燃料的化学。
①CO与H2按一定比例可合成乙二醇(C2H6O2),则n(CO)/n(H2)= 。
②汽油平均组成用CmHn表示,则合成汽油应控制n(CO)/n(H2)= 。(用m 、 n表示)
为测定某有机化合物A的结构,进行如下实验。
[分子式的确定]
(1)将有机物A置于氧气流中充分燃烧,实验测得:生成5.4 g H2O和8.8 g CO2,消耗氧气6.72 L(标准状况下),则该物质中各元素的原子个数比是_____________________。
(2)质谱仪测定该有机化合物的相对分子质量为46,则该物质的分子式是 。
(3)根据价键理论,预测A的可能结构并写出其结构简式 。
[结构式的确定]
(4)1H核磁共振谱能对有机物分子中不同位置的氢原子给出不同的峰值(信号),根据峰值(信号)可以确定分子中氢原子的种类和数目。例如:甲基氯甲基醚(Cl—CH2—O—CH3)有两种氢原子(如图1)。经测定,有机物A的1H核磁共振谱示意图如图2所示,则A的结构简式为 。
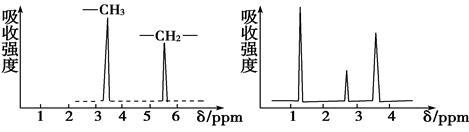
图1 图2
[性质实验]
(5)A在一定条件下脱水可生成B,B可合成塑料C,请写出B转化为C的化学方程式:_______________
(6)体育比赛中当运动员肌肉扭伤时,队医随即用氯乙烷(沸点为12.27 ℃)对受伤部位进行局部冷冻麻醉。请用B选择合适的方法制备氯乙烷,要求原子利用率为100%,请写出制备反应的化学方程式:_____________
A、B是相对分子质量不相等的两种烃,无论二者以何种比例混合,只要混合物的总质量不变,完全燃烧后所产生的CO2的质量就不变。
(1)试写出两组符合上述情况的烃的结构简式:
________________和________________;
________________和________________。(与第一组的物质类别不同)
(2)A、B应满足的条件是_____________________________________________。
Ⅰ.下图中A、B、C分别是三种有机物的结构模型:
请回答下列问题:
(1)A及其同系物的分子式中的碳原子数用n表示。当n=_______时,烷烃开始出现同分异构体。B模型是有机物的________模型。
(2)结构简式为 的有机物中,分子中最多有 个原子共面。
的有机物中,分子中最多有 个原子共面。
(3)等质量的A、B、C三种有机物完全燃烧生成H2O和CO2,消耗氧气的体积(相同状况下)最大的是________(填分子式)。
Ⅱ.在有机物分子中,不同氢原子的核磁共振氢谱中给出的峰值(信号)也不同,根据峰值(信号)可以确定有机物分子中氢原子的种类和数目。
(1)下列物质中,其核磁共振氢谱中给出的峰值(信号)只有一个的是________。
A.CH3COOH B.C(CH3)4 C.CH3COOCH3 D.CH3OH
(2)化合物A和B的分子式都是C2H4Br2,A的核磁共振氢谱图如下图所示,则A的结构简式为________。
(3)用核磁共振氢谱的方法来研究C2H6O的结构,简要说明根据核磁共振氢谱的结果来确定C2H6O分子结构的方法是_______________________ _ 。
(1)某有机物A的质量为9.2克,完全燃烧后生成0.4mol二氧化碳和10.8克水,且此有机物的蒸气的相对密度是相同状况下氢气的23倍,求:
①此有机物的分子式为
②写出该有机物可能的结构简式
(2)某烃B的相对分子质量为84。回答下列问题:
①下列物质与B以任意比例混合,若总物质的量一定,充分燃烧消耗氧气的量不相等的是(填序号) 。
a.C7H12O2 b.C6H14 c.C6H14O d.C7H14O3
②若链烃B分子中所有的碳原子共平面,该分子的一氯取代物只有一种, 则B的结构简式为 。
③若烃B不能使溴水褪色,并且其一氯代物只有一种,则B的结构简式为 。
(3)C1(一碳化学)是以含一个碳原子的化合物如:甲烷(CH4)、合成气(CO和H2)、CO2、CH3OH、HCHO等为初始反应物,反应合成一系列重要的化工原料和燃料的化学。
①CO与H2按一定比例可合成乙二醇(C2H6O2),则n(CO)/n(H2)= 。
②汽油平均组成用CmHn表示,则合成汽油应控制n(CO)/n(H2)= 。(用m 、 n表示)
有机物A可由葡萄糖发酵得到,也可从酸牛奶中提取.纯净的A为无色黏稠液体,易溶于水.为研究A的组成与结构,进行了如下实验:
实验步骤
称取A 9.0g,升温使其汽化,测其密度是相同条件下H2的45倍. 试通过计算填空:
(1)A的相对分子质量为: .
(2)将此9.0g A在足量纯O2中充分燃烧,并使其产物依次缓缓通过浓硫酸、碱石灰,发现两者分别增重5.4g和13.2g,则A的分子式为: .
(3)另取A 9.0g,跟足量的NaHCO3粉末反应,生成2.24L CO2(标准状况),若与足量金属钠反应则生成2.24L H2(标准状况) 则A中官能团的结构简式: 、 .
(4)A的核磁共振氢谱如图:

则A中含有 种氢原子
(5)综上所述,A的结构简式 .A与浓H2SO4混合,在一定条件下反应生成六元环状物B,B的结构简式 .
(1)(5分)由A、B两种气态烃组成的混合气体,对H2的相对密度为17。常温常压下,取这种混合气体10mL与80mL氧气(过量)混合,当完全燃烧后恢复到原状态时,测得气体的体积为70mL。试求:
①混合气体的平均组成为(用CxHy的形式表示)___________;
②若上述两种气体按体积1:1混合时,则两种气态烃的可能组成为______________。
(2)(5分)具有支链的化合物X的分子式为C4H8O,X既能使Br2的四氯化碳溶液褪色,又能与Na反应。
①X的结构简式是
②写出与X具有相同官能团的X的所有同分异构体的结构简式:_____________
对硝基甲苯是医药、染料等工业的一种重要有机中间体,它常以浓硝酸为硝化剂,浓硫酸为催化剂,通过甲苯的硝化反应制备。
一种新的制备对硝基甲苯的实验方法是:以发烟硝酸为硝化剂,固体NaHSO4为催化剂(可循环使用),在CCl4溶液中,加入乙酸酐(有脱水作用),45℃反应1h 。反应结束后,过滤,滤液分别用5% NaHCO3溶液、水洗至中性,再经分离提纯得到对硝基甲苯。
(1)上述实验中过滤的目的是 。
(2)滤液在分液漏斗中洗涤静置后,有机层处于 层(填“上”或'下”);放液时,若发现液体流不下来,其可能原因除分液漏斗活塞堵塞外,还有 。
(3)下列给出了催化剂种类及用量对甲苯硝化反应影响的实验结果。
| 催化剂 |
n(催化剂) n(甲苯) |
硝化产物中各种异构体质量分数(%) |
总产率(%) |
||
| 对硝基甲苯 |
邻硝基甲苯 |
间硝基甲苯 |
|||
| 浓H2SO4 |
1.0 |
35.6 |
60.2 |
4.2 |
98.0 |
| 1.2 |
36.5 |
59.5 |
4.0 |
99.8 |
|
| NaHSO4 |
0.15 |
44.6 |
55.1 |
0.3 |
98.9 |
| 0.25 |
46.3 |
52.8 |
0.9 |
99.9 |
|
| 0.32 |
47.9 |
51.8 |
0.3 |
99.9 |
|
| 0.36 |
45.2 |
54.2 |
0.6 |
99.9 |
①NaHSO4催化制备对硝基甲苯时,催化剂与甲苯的最佳物质的量之比为 。
②由甲苯硝化得到的各种产物的含量可知,甲苯硝化反应的特点是 。
③与浓硫酸催化甲苯硝化相比,NaHSO4催化甲苯硝化的优点有 。
等质量的甲、乙、丙、丁、戊、己6种只含C、H、O三种元素的有机物,分别充分燃烧时,消耗等量的O2,且生成的气体全部分别通过足量的无水硫酸铜后再分别通过足量的碱石灰,无水硫酸铜与碱石灰质量增重之比均为9∶22。已知:
① 6 M(甲)=3 M(乙)=3 M(丙)=3 M(丁)=2 M(戊)=M(己)=180;
② 乙、戊的水溶液可使甲基橙试液变红,相互之间在一定条件下能发生酯化反应;
③ 戊的核磁共振氢谱有4种峰,峰面积之比为3∶1∶1∶1;
④ 甲、丙、丁、己能发生银镜反应。丙不易溶于水但丁易溶于水。
请回答下列问题:
(1)甲的结构式为 ;己的一种可能的结构简式为 。
(2)乙、丙、丁三者之间的关系是 ;丁的结构简式为 。
(3)写出2分子戊生成1分子环状酯的化学方程式 。
有①甲烷,②乙烷,③丙烷,④丁烷4种烷烃,试回答下列问题:
(1)请写出烷烃(用通式表示)在足量的氧气中充分燃烧的化学方程式:
________________________________________________________________________。
(2)相同状况下,等体积的上述气态烃,消耗O2的量最多的是________ 。
(3)等质量的上述气态烃,在充分燃烧时,消耗O2的量最多的是________ 。
(4)存在同分异构体的是_______ _。
(5)在120 ℃,1.01×105Pa条件下,某气态烃与足量的O2完全反应后,测得反应前后气体的体积没有发生改变,则该烃为________ 。
(6)10 mL某气态烃,在50 mL O2中充分燃烧,得到液态水,以及体积为35 mL的混合气体(所有气体体积均在同温同压下测定)。该气态烃是________ 。