下列离子的检验方法正确的是
A.某溶液 有白色沉淀,说明原溶液中有Cl- 有白色沉淀,说明原溶液中有Cl- |
B.某溶液 有白色沉淀,说明原溶液中有SO42- 有白色沉淀,说明原溶液中有SO42- |
C.某溶液 无明显变化 无明显变化 溶液变红色,说明原溶液中有Fe2+ 溶液变红色,说明原溶液中有Fe2+ |
D.某溶液 生成无色无味气体,说明原溶液中有CO32- 生成无色无味气体,说明原溶液中有CO32- |
某同学在奥运五连环中填人了5种物质,相连环物质间能发生反应,不相连环物质间不能发生反应。你认为“五连环”中物质间发生的反应,没有涉及的基本反应类型有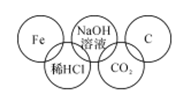
| A.复分解反应 |
| B.分解反应 |
| C.化合反应 |
| D.置换反应 |
某同学用中和滴定法去测定某烧碱的纯度,实验过程如下:
(1)配制待测液称取得 5.0g 固体烧碱样品(杂质不与酸反应)配制成 250 mL 溶液,
(2)用 0.2000 mol·L-1标准盐酸滴定待测烧碱溶液,实验操作如下
| A.用碱式滴定管取上述烧碱溶液10.00 mL,注入锥形瓶中,加入指示剂。 | B.用待测定 的溶液润洗碱式滴定管。 | C.用蒸馏水洗干净滴定管。 | D.取下酸式滴定管用标准的盐酸 溶液润洗后,将标准液注入酸式滴定管刻度“0”以上2~ 3 cm处,再把酸式滴定管固定好, 调节液面至刻度“0”或“0”刻度以下。E.检查滴定管是否漏水。F.另取锥形瓶,再重复 操作一次。G.把锥形瓶放在滴定管下面,边滴边摇动锥形瓶直至滴定终点,记下滴定管液面的刻度。 |
①滴定操作的正确顺序是(用序号填写):________________
②该滴定操作中应选用的指示剂是:________________
③在G操作中如何确定终点?________________
(3)数据处理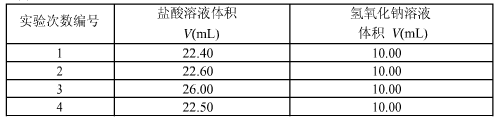
根据上述各数据,选取合适的三组,计算待测烧碱溶液的浓度为__________,烧碱的纯度为_________。
(4)下列操作,会导致实验结果偏低的是________(填序号)。
①碱式滴管用蒸馏水洗净后没有用待测液润洗 ②锥形瓶用蒸馏水洗净后没有用待测液润洗 ③终点读数时俯视(滴定前读数准确) ④酸式滴定管尖端气泡没有排除,滴定后消失 ⑤振荡时锥形瓶中液滴飞溅出来 ⑥酸式滴定管用蒸馏水洗净后没有用标准液润洗
液体燃料电池相比于气体燃料电池具有体积小等优点.一种以液态肼(N2H4)为燃料 的电池装置如图所示,该电池以空气中的氧气为氧化剂,以 KOH 溶液为电解质溶液.下列关于该电池的叙述错误的是( )
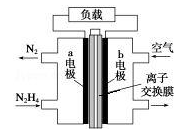
| A.b 极发生还原反应 | |
B.a 极的反应式为 N2H4﹣4e﹣═N2↑+4H+ |
C.放电时,电流从 b 极经过负载流向 a 极 |
| D.其中的离子交换膜需选用阴离子交换膜 |
如图所示,甲池的总反应式为 2CH3OH+3O2+4KOH═2K2CO3+6H2O.下列说法正确的是( )
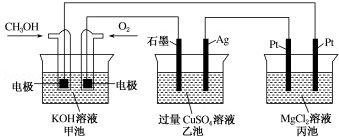
| A.若将乙池电解液换成 AgNO3 溶液,则可以实现在石墨棒上镀银 |
| B.甲池通入 CH3OH 的电极反应式为 CH3OH+6e﹣+2H2O═CO2-3+8H+ |
| C.反应一段时间后,向乙池中加入一定量 Cu(OH)2 固体,能使 CuSO4 溶液恢复到 原浓度 |
| D.甲池中消耗 224mL(标准状况下)O2,此时丙池中理论上产生 1.16g 固体 |
已知常温下,KSP(AgCl)=1.8×10-10 mol2·L-2,KSP(AgI)=8.3×10-17mol2·L-2,下列叙述中, 正确的是( )
| A.常温下,AgCl 在饱和 NaCl 溶液中的 KSP 比在纯水中的 KSP 小 |
| B.向 AgCl 的悬浊液中加入 KI 溶液,沉淀由白色转化为黄色 |
| C.将 0.001 mol·L-1的 AgNO3 溶液滴入 KCl 和 KI 的混合溶液中,一定先产生 AgI 沉淀 |
| D.向 AgCl 的饱和溶液中加入 NaCl 晶体,有 AgCl 析出且溶液中 c(Ag+)=c(Cl-) |
在一密闭容器中进行如下反应:3H2(气)+N2(气) 2NH3(气),已知反应过程中某一时 刻 H2、N2、NH3的浓度分别为 0.3mol/L、0.1mol/L、0.2mol/L,当反应达平衡时,可能存在的数据是( )
2NH3(气),已知反应过程中某一时 刻 H2、N2、NH3的浓度分别为 0.3mol/L、0.1mol/L、0.2mol/L,当反应达平衡时,可能存在的数据是( )
| A.H2为 0.6mol/L、N2为 0. 2mol/L | B.NH3为 0.25mol/L |
| C.N2、NH3均为 0.15mol/L | D.NH3为 0.4mol/L |
已知醋酸、醋酸根离子在溶液中存在下列平衡:
| CH3COOH+H2O |
C H3COO-+H3O+ |
K1=1.75×10-5 mol·L-1 |
| CH3COO-+H2O |
CH3COOH+OH- |
K2=5.71×10-10 mol·L-1 |


 现将 50 mL 0.2 mol·L-1醋酸与 50 mL 0.2 mol·L-1醋酸钠溶液混合制得溶液甲,下列叙述正确的是
现将 50 mL 0.2 mol·L-1醋酸与 50 mL 0.2 mol·L-1醋酸钠溶液混合制得溶液甲,下列叙述正确的是
A.溶液甲的pH>7
B.对溶液甲进行微热,K1、K2 同时增大
C.若在溶液甲中加入少量的 NaOH 溶液,溶液的 pH 明显增大
D.若在溶液甲中加入 5 mL 0.1 mol·L-1的盐酸,则溶液中醋酸的 K1 会变大
已知 298K 时,H+(aq)+ OH-(aq)= H2O(l) △H = -57.3 kJ/ mol ,推测含 1mol
CH3COOH 的稀溶液与含 1 mol NaOH 的稀溶液反应放出的热量( )
| A.大于 57.3 kJ | B.等于 57.3 kJ | C.小于 57.3 kJ | D.无法确定 |
下列四个装置图均与电化学有关,请根据图示回答相关问题:
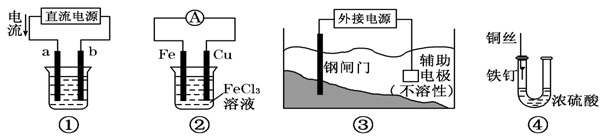
(1)这四个装置中,利用电解原理的是 (填装置序号);
(2)装置①若用来精炼铜,则a极的电极材料是 (填“粗铜”或“精铜”),电解质溶液为 ;
(3)装置②的总反应方程式是 ;
(4)装置③中钢闸门应与外接电源的 极相连(填“正”或“负”)
(5)装置④中的铁钉几乎没被腐蚀,其原因是 。
已知:Ksp(AgCl)=1.8×10-10,Ksp(AgI)=1.5×10-16 ,Ksp(AgBr)=7.7×10-13,则下列难溶盐的饱和溶液中,Ag+浓度大小顺序正确的是
| A.AgCl>AgI> AgBr | B.AgBr >AgI>AgCl |
| C.AgBr >AgCl>AgI | D.AgCl> AgBr>AgI |
已知:(1)Zn(s)+ 1/2O2(g)= ZnO(s),ΔH =" -350" kJ/mol,
(2)2Ag(s) + 1/2O2(g)= Ag2O(s),ΔH =" -25" kJ/mol,
则Zn(s)+ Ag2O(s) =" ZnO(s)+" 2Ag(s)的ΔH等于
| A.-375 kJ/mol | B.-325 kJ/mol |
| C.+375 kJ/mol | D.+325 kJ/mol |
欲用0.2000mol·L-1的标准NaOH溶液滴定未知浓度的盐酸,下列有关说法正确的是
| A.滴定管在装溶液前,先用蒸馏水洗涤干净后,再用待装溶液润洗 |
| B.锥形瓶在装待测溶液前,先用蒸馏水洗涤干净后,再用待装溶液润洗 |
| C.滴定过程中,两眼注视滴定管装液面的变化 |
| D.装标准液的滴定管中有气泡而滴定前未排出,则滴定结果将偏低 |