利用碳酸钠晶体(Na2CO3·10H2O)来配制1.0 mol·L-1 Na2CO3溶液500 mL,假如其他操作均准确无误,下列情况会引起所配溶液浓度偏高的是
| A.称取碳酸钠晶体53.0 g |
| B.移液时,对用于溶解碳酸钠晶体的烧杯没有进行冲洗 |
| C.定容时,俯视观察刻度线 |
| D.定容后,将容量瓶反复倒转、摇匀、静置时发现液面低于刻度线,于是又加入少量水至刻度线 |
下列溶液中Cl-的物质的量浓度与50 mL 1 mol/L AlCl3溶液中Cl-物质的量浓度相等的是
| A.75 mL 1.5 mol/L MgCl2溶液 | B.150 mL 2 mol/L KCl溶液 |
| C.100 mL 1 mol/L NaCl溶液 | D.25 mL 2 mol/L AlCl3溶液 |
已知下列几个反应的化学方程式:① 2KI+Cl2=2KCl+I2、② 2FeCl2+Cl2=2FeCl3、③ 2FeCl3+2HI=2FeCl2+I2+2HCl,下列有关物质的氧化性的强弱排列顺序中正确的是
| A.Cl2>Fe3+>I2 | B.Cl2>I2>Fe3+ |
| C.Fe3+>Cl2>I2 | D.Fe3+>I2>Cl2 |
水溶液中能大量共存的一组离子是
| A.NH4+、Ba2+、Br-、CO32- | B.Cl-、NO3-、Fe2+、H+ |
| C.K+、Na+、SO42-、MnO4- | D.Na+、H+、NO3-、HCO3- |
在下列化学方程式中,不能用离子方程式Ba2++SO42-=BaSO4↓表示的是
| A.Ba(NO3)2+H2SO4=BaSO4↓+2HNO3 |
| B.BaCl2+Na2SO4=BaSO4↓+2NaCl |
| C.BaCO3+H2SO4=BaSO4↓+H2O+CO2↑ |
| D.BaCl2+H2SO4=BaSO4↓+2HCl |
镁和铝分别与等浓度、等体积的过量稀硫酸反应,产生气体的体积(V)与时间(t)关系
如右图。反应中镁和铝的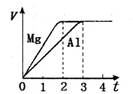
| A.物质的量之比为3:2 | B.质量之比为2:3 |
| C.摩尔质量之比为2:3 | D.反应速率之比为3:2 |
右图是向100mL的盐酸中逐滴加入NaOH溶液时,混合溶液的pH变化图像,根据图像得出的结论正确的是
| A.原盐酸溶液的浓度为0.1mol/L |
| B.加入的NaOH溶液的浓度为0.1mol/L |
| C.至滴定终点用去NaOH为0.01mo1 |
| D.pH=12时,共加入NaOH溶液100mL |
下列仪器中,不属于定量仪器的是
| A.容量瓶 | B.温度计 | C.烧杯 | D.秒表 |
下列微粒间的作用力中,不属于化学键的是
| A.分子间作用力 | B.金属键 | C.共价键 | D.离子键 |
从化学试剂商店购买的某些试剂瓶上常贴有危险化学品的标志。盛装浓硫酸的试剂瓶上所贴的危险化学品标志是
下列有关实验现象或结论的描述不正确的
| A.铅蓄电池充电时,阳极的反应为:PbSO4+2H2O+2e-=PbO2+SO42-+4H+ |
| B.FeCl2溶液与K3[Fe(CN)6]溶液混合后得到特征蓝色沉淀,利用此反应可检验Fe2+ |
| C.常温下将5mL0.1mol/LNa2S2O3溶液、5mL0.01mol/LNa2S2O3溶液分别与5mL0.1mol/LH2SO4溶液混合并搅拌,通过记录溶液中出现浑浊的时间,可确定浓度对化学反应速率的影响 |
| D.处理含有Hg2+离子的废水可加入硫化钠,使Hg2+离子转化为HgS沉淀 |
一定条件下,在密闭容器里进行如下可逆反应:S2Cl2(橙黄色液体)+Cl2(气) 2SCl2(鲜红色液体) ΔH=-61.16 kJ·mol-1。下列说法正确的是
2SCl2(鲜红色液体) ΔH=-61.16 kJ·mol-1。下列说法正确的是
| A.增大压强,平衡常数将增大 |
| B.达到平衡时,单位时间里消耗n mol S2Cl2的同时也生成n molCl2 |
| C.达到平衡时,若升高温度,氯气的百分含量减小 |
| D.加入氯气,平衡向正反应方向移动,氯气的转化率一定升高 |
某溶液可能含有Cl-、SO42-、CO32-、NH4+、Fe3+、Al3+和K+。取该溶液100 mL,加入过量NaOH溶液,加热,得到0.02 mol气体,同时产生红褐色沉淀;过滤,洗涤,灼烧,得到1.6 g固体;向上述滤液中加足量BaCl2溶液,得到4.66 g不溶于盐酸的沉淀。由此可知原溶液中
| A.至少存在5种离子 |
| B.CO32-、Al3+一定不存在,K+可能存在 |
| C.SO42-、NH4+一定存在,Cl-可能不存在 |
| D.Cl-一定存在,且c(Cl-)≥0.4 mol·L-1 |
下列说法正确的是
A.将标准状况下的2.24L CO2通入150mL 1mol·L-1 NaOH溶液中,所得溶液中c(CO32-)>c(HCO3-)
B.常温下0.1 mol·L-1的下列溶液①NH4Al(SO4)2 ②NH4Cl ③NH3·H2O ④CH3COONH4中,c(NH4+)由大到小的顺序是:②>①>④>③
C.0.1 mol·L-1 pH为9的NaHB溶液中:c(HB-)>c(B2-)>c(H2B)
D.室温下,将0.4mol/L HA溶液和0.2mol/LNaOH溶液等体积混合(忽略混合时溶液体积的变化)测得混合液pH=5,则c(A-)+c (OH-)>c (H+) + c(HA)