[化学-物质结构与性质]碳、氮、氧、铁、铜是常见的几种元素,请回答以下问题:
(1)已知碳、氧、氯三种元素可形成CCl4、ClO:等物质,则C,O、Cl的电负性从大到小的顺序为______。
(2)基态铜原子的核外电子排布式为___________________________。
(3)三氯化铁常温下为固体,熔点282~C,沸点315~C,易溶于水,也易溶于乙醚、丙酮等有机溶剂。据此判断三氯化铁的晶体类型为_________。
(4)lmolCH3COOH分子中含有ɑ键数目为___________。
(5)维生素B1可作为辅酶参与糖的代谢,并有保护神经系统的作用。该物质的结构式为
①维生素B1中碳原子的杂化轨道类型有__________________
②维生素B1晶体溶于水的过程中要克服的微粒间的作用力有________________。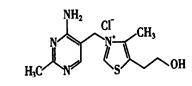
| A.离子键、共价键 | B.离子键、氢键、共价键 |
| C.氢键、范德华力 | D.离子键、氢键、范德华力 |
(6)通常酸式盐在水中的溶解度大于正盐,但NaHCO3,的溶解度却小于Na2C03,这是由于____________。
选考[化学一选修3:物质结构与性质]砷化稼为第三代半导体,以其为材料制造的灯泡寿命长,耗能少。己知砷化稼的晶胞结构如图所示。请回答下列问题:
(1)下列说法正确的是____(填序号)。
| A.砷化镓晶胞结构与NaCl相同 |
| B.第一电离能As>Ga |
| C.电负性As>Ga |
| D.原子半径As>Ga |
(2)砷化镓可由(CH3)3Ga和AsH3在700℃下反应制得,反应的方程式为_________________;
(3)AsH3空间形状为_______;已知(CH3)3Ga为非极性分子,则其中镓原子的杂化方式为____________;
Ⅱ.金属铜的导电性仅次于银,居金属中的第二位,大量用于电气工业。
(4)请解释金属铜能导电的原因___________,Cu2+的核外电子排布式为_________________
(5)在硫酸铜溶液中通入过量的氨气,小心蒸发,最终得到深蓝色的[Cu(NH3)4]SO4晶体,晶体中含有的化学键除普通共价键外,还有___________和____________。
[化学—选修3:物质结构与性质](15分)
Ⅰ.德国和美国科学家首先制出由20个碳原子组成的空心笼状分子C20,该笼状结构是由许多正五边形构成如图。
①C20分子中每个碳原子只跟相邻的3个碳原子形成化学键;
②多面体的顶点数、面数和棱边数的关系,遵循欧拉定理:顶点数+面数-棱边数=2,
请回答:C20分子共有 个正五边形,共有 条棱边。
Ⅱ.A、B、C是短周期非金属元素,核电荷数依次增大。A原子外围电子排布为ns2np2,C是地壳中含量最多的元素。D元素的核电荷数为29。请用对应的元素符号或化学式填空:
(1)A、B、C的第一电离能由小到大的顺序为 。
(2)分子(AB)2中键与键之间的夹角为180°,并有对称性,每个原子最外层电子数均满足八电子,其结构式为 ,1mol该分子中含有π键的数目为 。该分子中碳原子的杂化轨道类型是 ,该分子属于 分子(填“极性”或“非极性”)。
(3)基态D原子的电子排布式为 。
(12分)【选做题】本题包括A、B两小题,请选定其中一小题,并作答。若多做,则按A小题评分。
A.[物质结构与性质]原子序数小于36的X、Y、Z、W四种元素,X基态原子的最外层电子数是其内层电子数的2倍,Y基态原子的2p原子轨道上有3个未成对电子,Z是地壳中含量最多的元素,W的原子序数为22。
(1)W基态原子的核外电子排布式为________。元素X、Y、Z的电负性由大到小的顺序为________。
(2)与XYZ-互为等电子体的一种分子、一种离子分别为________、________(填化学式)。
(3)二元弱酸H2X2Z4中X原子轨道的杂化类型是_______,1 molH2X2Z4分子中含有σ键的数目为_______。
(4)YH3极易溶于水的主要原因是________________。元素W的氧化物WO2可与氢氟酸发生非氧化还原反应,生成配合物HnWF6,该反应的化学方程式为________。
(5)Z、W与Ca形成晶体的晶胞如图所示,该晶体的化学式为________。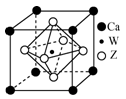
【选做题】本题包括A、B两小题,请选定其中一小题,并在相应的答题区域内作答。若多做,则按A小题评分。
A.[物质结构与性质]
高氯酸三碳酰肼合镍{[Ni(CHZ)3](ClO4)2 }是一种新型的起爆药。
(1)Ni2+基态核外电子排布式为 。
(2)ClO4-的空间构型是 ;与ClO4-互为等电子体的一种分子为 (填化学式)。
(3)化学式中CHZ为碳酰肼,组成为CO(N2H3)2,碳酰肼中碳原子的杂化轨道类型为 ;1molCO(N2H3)2分子中含有σ键数目为 。
(4)高氯酸三碳酰肼合镍可由NiO、高氯酸及碳酰肼化合而成。NiO的晶胞结构如图所示,晶胞中含有的Ni2+数目为a,Ni2+的配位数为b,NiO晶体中每个镍离子距离最近的镍离子数目为c,则a∶b∶c= 。
(12分)【选做题】本题包括A、B两小题,请选定其中一小题作答。若多做,则按A小题评分。
A.【物质结构与性质】
氧化锌(ZnO)、氮化镓(GaN)及新型多相催化剂组成的纳米材料能利用可见光分解水,生成氢气和氧气。
(1)Zn2+基态核外电子排布式为________。
(2)与水分子互为等电子体的一种阴离子是________(填化学式)。
(3)氮化镓(GaN)的晶体结构如图1所示,其中氮原子的杂化轨道类型是________;N、Ga原子之间存在配位键,该配位键中提供电子对的原子是________。
(4)ZnO是两性氧化物,能跟强碱溶液反应生成[Zn(OH)4]2-。 不考虑空间构型,[Zn(OH)4]2-的结构可用示意图表示为________。
(5)某种ZnO晶体的晶胞如图2所示,与O2-距离最近的Zn2+有________个。
铜单质及其化合物在很多领域有重要用途,如金属铜用来制造电线电缆,五水硫酸铜可用作杀菌剂。
(1)Cu位于元素周期表第四周期第ⅠB 族。Cu2+的核外电子排布式为 。
(2)如图1是铜的某种氧化物的晶胞结构示意图,可确定该晶胞中阴离子的个数为 。
(3)胆矾CuSO4·5H2O可写成[Cu(H2O)4]SO4·H2O,其结构示意图如图2:下列说法正确的是 (填字母)。
| A.在上述结构示意图中,所有氧原子都采用sp3杂化 |
| B.在上述结构示意图中,存在配位键、共价键和离子键 |
| C.胆矾是分子晶体,分子间存在氢键 |
| D.胆矾中的水在不同温度下会分步失去 |
(4)往硫酸铜溶液中加入过量氨水,可生成[Cu(NH3)4]2+配离子。已知NF3与NH3的空间构型都是三角锥形,但NF3不易与Cu2+形成配离子,其原因是: 。
(5)Cu2O的熔点比Cu2S的 (填“高”或“低”),请解释原因: 。
(6)S单质的常见形式为S8,其环状结构如图所示,S原子采用的轨道杂化方式是________
(7)原子的第一电离能是指气态电中性基态原子失去一个电子转化为气态基态正离子所需要的最低能量,O、S、Se原子的第一电离能由大到小的顺序为____________________;
【化学—选修3:物质结构与性质】(15分)A、B、C、D、E、F均属前四周期且原子序数依次增大的六种元素,其中A、B、C是同一周期相邻的三种元素,C的氢化物水溶液呈碱性;D的基态原子3p轨道上有3个未成对电子;E、F为副族元素,4s能级均只有一个电子。回答下列问题:
(1)A、B、C三种元素按电负性由小到大的顺序是_________(用元素符号表示)。
(2)B与氧原子能形成四原子阴离子,其中B的杂化方式为_____________;C的三氯化物分子的立体构型为____________________________________。
(3)任写一种与BC—离子互为等电子体的离子__________________(写出化学式)。
(4)F原子的外围电子排布式为_____________,F晶体中原子的堆积方式是下图中的_________(填写“甲”、“乙”或“丙”)。
(5)E的离子可以形成多种配合物,将ECl3溶液蒸发浓缩,析出深绿色晶体。该晶体中E3+、Cl—、H2O的物质的量之比为1∶3∶6,且E的配位数为6。向1.0mol该晶体的溶液中加入足量AgNO3溶液产生143.5g白色沉淀,则该配合物的化学式为__________________________。
(6)AD是一种耐磨材料,其结构与金刚石相似,下图为其晶体结构单元,它可由A的三溴化物和D的三溴化物于高温下在氢气的氛围中合成。
①写出合成AD的化学方程式:________________________。
②已知晶体中A与D原子的最近距离为a pm,则该晶体密度的表达式为_________g/cm3。(不需化简,阿伏加德罗常数为NA)
( 在5-氨基四唑(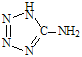 )中加入金属Ga,得到的盐是一种新型气体发生剂,常用于汽车安全气囊。
)中加入金属Ga,得到的盐是一种新型气体发生剂,常用于汽车安全气囊。
(1)基态Ga原子的电子排布式可表示为 ;
(2)5-氨基四唑中所含元素的电负性由大到小的顺序为 ;
在1mol 5-氨基四唑中含有的σ键的数目为 。
(3)叠氮酸钠(NaN3)是传统家用汽车安全气囊中使用的气体发生剂。
①叠氮酸钠(NaN3)中含有叠氮酸根离子(N3-),根据等电子体原理N3-的空间构型为 。②以四氯化钛、碳化钙、叠氮酸盐作原料,可以生成碳氮化钛化合物。其结构是用碳原子取代氮化钛晶胞(结构如图示)顶点的氮原子,这种碳氮化钛化合物的化学式为 。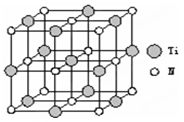
③与钛同周期的所有元素的基态原子中,未成对电子数与钛相同的元素有 。(填写元素符号)
④[Ti(OH)2(H2O)4]2+中的化学键有 。
| A.σ键 | B.π键 | C.离子键 | D.配位键 |
(10分)金属镍及其化合物在合金材料以及催化剂等方面应用广泛。
(1)基态镍原子的外围电子排布式为 。
(2)金属镍能与CO形成配合物Ni(CO)4,写出与CO互为等电子体的一种分子和一种离子的化学式 、 。
(3)很多不饱和有机物在Ni催化下可与H2发生加成反应。
如①CH2=CH2、②HC≡CH、③ 、④HCHO,其中碳原子采取sp2杂化的分子有
、④HCHO,其中碳原子采取sp2杂化的分子有
(填物质序号),HCHO分子的立体结构为 形。
(4)金属镍与镧(La)形成的合金是一种良好的储氢材料,其晶胞结构示意图如左下图所示。该合金的化学式为 。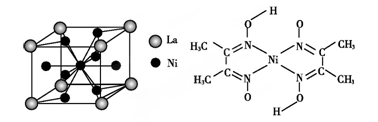
(5)丁二酮肟常用于检验Ni2+:在稀氨水中,丁二酮肟与Ni2+反应生成鲜红色沉淀,其结构如上右图所示。该结构中,除共价键外还存在配位键和氢键,请在图中用箭头和“…”表示出配位键和氢键。
准晶体亦称为准晶或拟晶,是一种介于晶体和非晶体之间的固体结构。
(1)有一种由铝、铜、铁三种元素构成的天然准晶体化合物,分析该准晶体组成的一种简单方法是先将该准晶体进行粉碎,然后按如下程序进行实验:
第1步:称取38.99 g 准晶体,让其与足量的NaOH溶液充分反应,在标准状况下,收集得到21.84 L 氢气。
第2步:将第1步反应后的浊液过滤出固体,用蒸馏水洗涤,逐滴滴入6mol/L盐酸,当加入的盐酸的体积为40mL时,固体不再溶解。
①铝、铁的第一电离能的大小关系为 (用元素符号表示)。
②根据以上实验可确定该准晶体的化学式为 。
(2)锰与一种短周期元素A形成的凝固态是一种准晶,已知A最外层电子数等于其电子层数,且其中含有成对和不成对电子。
①锰原子在基态时的核外电子排布式为 。
②锰与A在准晶体中的结合力为 。(离子键、共价键、金属键、分子间作用力)
③锰与A形成的准晶结构如图所示,则该准晶体的化学式为 。
④过渡金属配合物Mn2(CO)n的中心原子价电子数与配体提供电子总数之和为34,则n= 。
X、Y、Z、W、M五种元素位于周期表的前四周期,原子序数依次增大,其中X元素是宇宙中最丰富的元素,Y元素原子核外有三种不同的能级且各个能级所填充的电子数相同,W元素原子最外层电子数是内层电子数的3倍,M含有未成对电子数最多的元素。请回答下列问题。
(1)Y、Z、W的电负性由小到大的顺序为______________。(用元素符号表示)
(2)M原子的外围电子排布式为________。
(3)X2W2分子中W原子轨道的杂化类型为________。
(4)Z与W可形成的一种ZW3-阴离子,与其互为等电子体的阴离子为_______(任写一种,)。
(5)MCl3能与Z、W的氢化物形成配位数为6的配合物,且相应两种配体的物质的量之比为2∶1,氯离子全部位于外界。则该配合物的化学式为_______。
(本题15分)铜是重要金属,Cu的化合物在科学研究和工业生产中具有许多用途.请回答以下问题:
(1)Cu+基态核外电子排布式为
(2)与OH-互为等电子体的一种分子为 (填化学式)。
(3)氯和钾与不同价态的铜可生成两种化合物,其阴离子均为无限长链结构(如图),a位置上Cl原子的杂化轨道类型为__________。已知其中一种化合物的化学式为KCuCl3,另一种的化学式为___________;
(4)Cu2O的熔点比Cu2S的 (填“高”或“低”),请解释原因_________。
(5)一种铜金合金晶体具有面心立方最密堆积的结构,在晶胞中Cu原子处于面心,Au原子处于顶点位置,则该合金中Cu原子与Au原子数量之比为_______;该晶体中,原子之间的作用力是________;
(6)上述晶体具有储氢功能,氢原子可进入到由Cu原子与Au原子构成的四面体空隙中。若将Cu原子与Au原子等同看待,该晶体储氢后的晶胞结构为CaF2的结构相似,该晶体储氢后的化学式应为__________。
(7)将空气或氧气直接通入到铜粉与稀硫酸的混合物中,发现在常温下几乎不反应。向反应液中加少量FeSO4作催化剂,即发生反应,生成硫酸铜。其反应过程的第2步是:2Fe3++Cu===2Fe2++Cu2+,请写出其第l步反应的离子方程式__________________________________。
[化学一物质结构与性质](13分)钛被称为“国防金属’’和“生物金属”,是重要的结构材料。
(1)基态钛原子的核外电子排布式是_______________________________,钛所在的周期中第一电离能最小的元素是______________________________.
(2)金红石(TiO2)的熔点 ,用熔盐法直接电解金红石可获得金属钛,金红石所属的晶体类型是______________________________________晶体。
,用熔盐法直接电解金红石可获得金属钛,金红石所属的晶体类型是______________________________________晶体。
(3)TiCl4能与NH4CI反应生成配合物(NH4)2[TiCl6]。此配合物中,形成配位键时提供孤对电子的有_____________.(填元素符号),空间构型呈正四面体的微粒是___________。
(4)TiO2+与H2O2在稀酸中反应生成橘红色的[TiO(H2O2) ] 2+离子,可用于钛的定性检验。
[TiO(H2O2) ] 2+中不含有_____________________________.
A.极性键
B.非极性键
C. 键
键
D. 键
键
E.离子键
(5)H2O2分子可看成H2O分子中的一个H被OH所取代,下列关于H2O2的说法正确的是______
A.H2O2分子结构对称为非极性分子
B.I mol H2O2最多能形成2mol氢键
C.H2O2不稳定是因为氢键的键能较小
D.H2O2分子的空间构型为直线形
【物质结构与性质】
Fe、C、N、O、H可以组成多种物质。回答以下问题:
(1)基态铁原子中,未成对电子数有 个。
(2)铁单质在一定条件下可与CO反应生成配位化合物——羰基铁[Fe(CO)5],其结构如图。已知CO分子与N2分子结构相似,分子中C、O原子均能提供孤电子对形成配位键。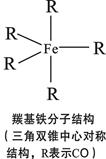
①CO分子中σ键与π键数目之比为 ;
②从电负性角度分析,Fe(CO)5中与Fe形成配位键的是 (填“碳”或“氧”)原子。
③与羰基铁分子的极性相似的分子是 。
A.SO2 B.CS2 C.BF3 D.PCl3
(3)CH4、H2O分子的键角分别为a、b。则a b(填>、=或<),原因是 。
(4)血红素分子结构如图所示。
①血红素分子间存在的作用力有 (填名称);
②与Fe通过配位键结合的氮原子的编号是 。