写出钢铁生锈的电极反应式(水膜呈中性):
负极___________________________
正极___________________________
下列叙述的原因不是由于原电池造成的是
| A.运输液氯的铁管被腐蚀 | B.金属在潮湿空气中更容易腐蚀 |
| C.铁与酸反应滴加硫酸铜后反应加快 | D.含杂质的锌比纯锌与酸反应快 |
以下现象与电化学腐蚀无关的是:
| A.黄铜(铜锌合金)制作的铜锣不易产生铜绿 |
| B.生铁比纯铁更易生锈 |
| C.铁质配件附有铜质配件,在接触处易生铁锈 |
| D.银质物品久置表面变暗 |
家用炒菜铁锅用水清洗放置后,出现红棕色的锈斑,在此变化过程中不发生的化学反应是
| A.4Fe(OH)2+2H2O+O2=4Fe(OH)3↓ | B.2Fe+2H2O+O2=2Fe(OH)2↓ |
| C.2H2O+O2+4e-=4OH- | D.Fe-3e-=Fe3+ |
24.(15分)本题为选做题,包括A、B两题。选学《化学与生活》模块的考生答A题,选学《有机化学基础》模块的考生答B题,每位考生只可选做1题。若两题都作答,则以A题计分。
A.《化学与生活》
(4分)性能各异的各种材料的广泛应用大大提高了人们的生活水平。回答问题:
(1)家庭中“钢精锅”是由铝合金做成的,在烧菜时能否放大量醋炖煮? 。(填能或否)
(2)下列关于铁制品保护措施的说法中不正确的有 (填序号)。
A.在自行车钢圈上镀上一层金属铬,摩擦部位加上机油或黄油
B.相同条件下,马口铁(表层镀锡)与白铁(表层镀锌)相比,马口铁更为耐用
C.在海轮的外壳上常焊有锌块,且定期更新
D.将不锈钢制成刀具和餐具,有的刀具还进行烤蓝处理
(3)在快中子反应堆中得以广泛应用的钠钾合金,这个事实说明合金的熔点比其成分金属的熔点 (填字母)。
a.高 b.低 c.可能高也可能低
(4)轨道交通建设需要大量金属材料。下列金属材料最容易发生腐蚀的是 (填字母)
a、铝合金 b、钢铁 c、纯度很高的铁
下列叙述与电化学腐蚀无关的是
| A.切过咸菜的菜刀不及时清洗易生锈 |
| B.线路连接时,有经验的电工从不把铝导线和铜导线接在一起 |
| C.银质奖章久置后表面逐渐变暗 |
| D.在轮船的尾部和船壳的水线以下,常装有一定数量的锌块 |
化学用语是学习化学的重要工具,下列化学用语中正确的是
A.Na2S的水解:S2-+ 2H2O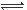 H2S + 2OH- H2S + 2OH- |
B.NaHCO3的电离:NaHCO3 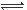 Na + + H+ + CO32- Na + + H+ + CO32- |
C.HSO3-的电离:HSO3- 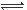 H+ + SO32- H+ + SO32- |
| D.钢铁的电化学腐蚀的负极反应式:Fe-3e-Fe3+ |
下列叙述,其中正确的是
①电解池是将化学能转变成电能的装置
②原电池是将电能转变成化学能的装置
③金属和石墨导电均为物理变化,电解质溶液导电是化学变化
④不能自发进行的氧化还原反应,通过电解的原理有可能实现
⑤电镀过程相当于金属的“迁移”,可视为物理变化
| A.①②③④ | B.③④ | C.③④⑤ | D.④ |
下列叙述错误的是
| A.生铁中含有碳,抗腐蚀能力比纯铁弱 |
| B.用锡焊接的铁质器件,焊接处易生锈 |
| C.在铁制品上镀铜时,镀件为阳极,铜盐为电镀液 |
| D.铁管上镶嵌锌块,铁管不易被腐蚀 |
(9分) 观察下列几个装置示意图,有关叙述正确的是
(1)在①图中,发生反应的化学方程式为: 。
(2)在②图中,待镀铁制品应与电源 极相连,电极反应式为: 。
(3)在③图中,外电路电子由 极流向 极,若电解液为KOH溶液,则b极的反应式为 。
有关下图的说法不正确的是
| A.构成原电池时Cu极反应为: Cu﹣2e-=Cu2+ |
| B.无论a和b是否连接,铁片均会溶解,溶液从蓝色逐渐变成浅绿色 |
| C.要使Fe极不被腐蚀,Cu片换Zn片或将a与直流电源的负极相连 |
| D.a和b分别连接直流电源正、负极,Fe片上有气体产生 |
下列叙述错误的是
| A.生铁中含有碳,抗腐蚀能力比纯铁弱 |
| B.铁在潮湿空气中发生腐蚀,其负极反应是2H++2e-=H2↑ |
| C.用锡焊接的铁质器件,焊接处易生锈 |
| D.铁管上镶嵌锌块,铁管不易被腐蚀 |
在面盆、痰盂等铁制品表面烧制搪瓷的目的是
| A.防止铁生锈且美观 | B.增大厚度防止磨损 |
| C.增大硬度防止撞坏 | D.美观及杀菌消毒作用 |