已知NH3难溶于CCl4,如下图所示,下列装置中,不宜用于氨气吸收的是( )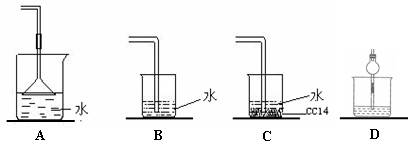
光卤石是化工生产中一种重要的中间产物,其化学成分是KCl·MgCl2·6H2O。当用光卤石为原料制取金属镁时,一共有下列几步:①过滤②溶解 ③加入适量Ca(OH)2④蒸发⑤用盐酸溶解⑥电解熔融MgCl2⑦在HCl气流中强热MgCl2·6H2O晶体,正确的顺序是( )
| A.⑤③①②④⑥⑦ | B.②③①⑤④⑦⑥ |
| C.②④①③⑦⑤⑥ | D.⑤③①④②⑦⑥ |
海水是巨大的资源宝库,在海水淡化及综合利用方面,天津市位居全国前列。从海水中提取食盐和溴的过程如下:


 (1)请列举海水淡化的两种方法、。
(1)请列举海水淡化的两种方法、。
 (2)将
(2)将溶液进行电解,在电解槽中可直接得到的产品有
、、、或
、。
 (3)步骤Ⅰ中已获得
(3)步骤Ⅰ中已获得,步骤Ⅱ中又将
还原为
,其目的为。
 (4)步骤Ⅱ用
(4)步骤Ⅱ用水溶液吸收
,吸收率可达95%,有关反应的离子方程式为,由此反应可知,除环境保护外,在工业生产中应解决的主要问题是。
 (5)某化学研究性学习小组为了解从工业溴中提纯溴的方法,查阅了有关资料,
(5)某化学研究性学习小组为了解从工业溴中提纯溴的方法,查阅了有关资料,的沸点为59℃。微溶于水,有毒性和强腐蚀性。他们参观生产过程后,了如下装置简图:


 请你参与分析讨论:
请你参与分析讨论:
 ①图中仪器
①图中仪器的名称:。
 ②整套实验装置中仪器连接均不能用橡胶塞和橡胶管,其原因是。
②整套实验装置中仪器连接均不能用橡胶塞和橡胶管,其原因是。
 ③实验装置气密性良好,要达到提纯溴的目的,操作中如何控制关键条件:。
③实验装置气密性良好,要达到提纯溴的目的,操作中如何控制关键条件:。
 ④
④中液体产生颜色为。为除去该产物中仍残留的少量
,可向其中加入
溶液,充分反应后,再进行的分离操作是。
二氧化氯()是一种在水处理等方面有广泛应用的高效安全消毒剂。与Cl2比,
不但具有更显著的杀菌能力,而且不会产生对人体有潜在危害的有机氯代物。
(1)在的制备方法中,有下列两种制备方法:
方法一:↑
↑
方法二↑
↑:
用方法二制备的更适合用于饮用水的消毒,其主要原因是。
(2)用处理过的饮用水(
为5.5~6.5)常含有一定量对人体不利的亚氯酸根离子(
)。2001年我国卫生部规定,饮用水中
的含量应不超过0.2
。饮用水中
、
的含量可用连续碘量法进行测定。
被
还原为
、
的转化率与溶液
的关系如图所示。

当≤2.0时,
也能被
还原成
。
反应生成的I2用标准溶液滴定:
①请写出≤2.0时,
与
反应的离子方程式。
②请完成相应的实验步骤:
步骤1:准确量取水样加入到锥形瓶中。
步骤2:调节水样的为7.0~8.0。
步骤3:加入足量的晶体。
步骤4:加入少量淀粉溶液,用溶液滴定至终点,消耗
溶液
。
步骤5:。
步骤6:再用溶液滴定至终点,消耗
溶液
。
③根据上述分析数据,测得该饮用水样中浓度为
用含字母的代数式表示)
④若饮用水中的含量超标,可向其中加入适量的
将
还原成
,该反应的氧化产物是(填化学式)。