已知反应X+Y= M+N为放热反应,对该反应的下列说法中正确的
| A.X的能量一定高于M |
| B.因该反应为放热反应,故不必加热就可发生 |
| C.Y的能量一定高于N |
| D.X和Y的总能量一定高于M和N的总能量 |
50 mL 1.0 mol·L-1盐酸跟50 mL 1.1 mol·L-1氢氧化钠溶液在下图装置中进行中和反应,并通过测定反应过程中所放出的热量来计算中和热。试回答下列问题:
⑴大小烧杯间填满碎泡沫塑料的作用___ 。
⑵ (填“能”或“不能”)将环形玻璃搅拌棒改为环形铜棒。其原因是 。
⑶大烧杯上如不盖硬纸板,对求得中和热数值的影响是 (填“偏高”或“偏低”或“无影响”)。
⑷如果改用60 mL 1.0 mol·L-1盐酸跟50 mL 1.1 mol·L-1氢氧化钠溶液进行反应,则与上述实验相比,所放热量 (“增加”、 “减少”或“不变”),理由是 ;所求中和热数值 (“增加”、 “减少”或“不变”),理由是 。
已知反应2CO(g)=2C(s)+O2(g)的△H为正值,△S为负值,设△H和△S不随温度改变,对于该反应下列说法正确的是( )
| A.低温下是自发变化 |
| B.高温下是自发变化 |
| C.任何温度下都是自发变化 |
| D.任何温度下都是非自发变化 |
氮化铝(AlN)具有耐高温、抗冲击、导热性好等优良性质,被广泛应用于电子工业、陶瓷工业等领域。在一定条件下,氮化铝可通过如下反应合成:
Al2O3 + N2 + 3C 2AlN + 3CO↑
2AlN + 3CO↑
下列叙述不正确的是
| A.在氮化铝的合成反应中,N2是还原剂 |
| B.在氮化铝的合成反应中,C是还原剂 |
| C.氮化铝中氮元素的化合价为-3 |
| D.上述反应中每生成1molAlN,转移3 mol e- |
20世纪30年代,Eyring和Pelzer在碰撞理论的基础上提出化学反应的过渡态理论:化学反应并不是通过简单的碰撞就能完成的,而是在反应物到生成物的过程中经过一个高能量过渡态。分析图中信息,回答下列问题: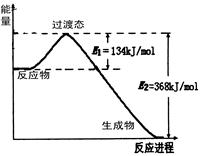
右图是NO2和CO反应生成CO2和NO过程中能量变化示意图,请写出NO2和CO反应的热化学方程式: 。
下列说法中正确的是
| A.能够使甲基橙呈现黄色的溶液一定是碱性溶液 |
| B.凡需加热的反应一定是吸热反应 |
| C.水解反应是放热反应 |
| D.绝对不溶解的物质是不存在的 |
下列说法中正确的是( )
| A.在化学反应过程中,发生物质变化的同时不一定发生能量变化 |
| B.生成物全部化学键形成时所释放的能量大于破坏反应物全部化学键所吸收的能量时, 反应为吸热反应 |
| C.为了提高煤的利用率,常将煤气化或直接液化后燃烧。煤气化或直接液化属于物理变化 |
| D.反应产物的总焓大于反应物的总焓时,反应吸热,ΔH>0 |
0.3mol气态高能燃料乙硼烷(B2H6)在氧气中燃烧,生成固态三氧化二硼和液态水,放出649.5kJ的热量。
(1)写出反应的热化学方程式。
(2)已知H2O(l)转化为H2O(g)的△H=44kJ·mol-1,试计算11.2L(标准状况)气态乙硼烷完全燃烧生成气态水时放出的热量。
已知:①H2(g)+ O2(g)=H2O(g) △H1=a kJ·mol-1
O2(g)=H2O(g) △H1=a kJ·mol-1
②2H2(g)+O2(g)=2H2O(g) △H2=b kJ·mol-1
③H2(g)+ O2(g)=H2O(l) △H3=c kJ·mol-1
O2(g)=H2O(l) △H3=c kJ·mol-1
④2H2(g)+O2(g)=2H2O(l) △H4=d kJ·mol-1
下列关系式中正确的是
| A.a<c<0 | B.b>d>0 | C.2a=b<0 | D.2c=d>0 |
下列变化不能说明发生了化学变化的是( )
| A.变化时有电子的得失或共用电子对的形成 |
| B.变化过程中有化学键的断裂和形成 |
| C.变化时释放或吸收能量 |
| D.变化前后原子的种类和数目没有改变,分子种类增加了 |
用50mL 0.55mol/L NaOH溶液和50mL 0.25mol/L H2SO4溶液来做中和热测定的实验,测得溶液在反应前后的温度变化为t1℃~t2℃(t2>t1),混合后溶液的比热容为c = 4.18J/(g·℃),溶液的密度都近似为1g/mL,中和热△H=____________________(填表达式,不用化简)若将H2SO4溶液换成相同物质的量浓度的CH3COOH溶液,测得的△H______填(“偏大”、“偏小”或“相同”)若将稀硫酸换成浓硫酸来做该实验,测得的△H___________(填“偏大”、“偏小”或“相同”)
实验室用4molSO2与2molO2在一定条件下进行下列反应:
2SO2(g)+O2(g) 2SO3(g);△H=-197kJ/mol,当放出315.2kJ热量时,SO2的转化率为
2SO3(g);△H=-197kJ/mol,当放出315.2kJ热量时,SO2的转化率为
| A.40% | B.50% | C.80% | D.90% |
已知1g氢气完全燃烧生成水蒸气时放出热量121kJ,且1mol O2的化学键完全断裂时吸收热量496kJ,水蒸气中1mol H-O键形成时放出热量463kJ,则氢气中1mol H-H键断裂时吸收热量为
| A.188kJ | B.436kJ | C.557kJ | D.920kJ |
已知氯气、溴蒸气分别跟氢气反应的热化学方程式如下(Q1、Q2均为正值):
H2(g)+Cl2(g) =" 2HCl(g)" △H= -Q1kJ/mol; H2(g)+Br2(g) =" 2HBr(g)" △H= -Q2kJ/mol
有关上述反应的叙述正确的是
| A.Q1>Q2 |
| B.1mol HBr(g)具有的能量大于1mol HBr(1)具有的能量 |
| C.生成1molHCl气体时放出Q1kJ热量 |
| D.生成物总能量均高于反应物总能量 |