物质之间的转化关系如下图,其中A、D、E、F、H为常见单质,其余为化合物,且单质E和单质F在点燃或加热的条件下生成淡黄色的固体,B常温下为液态化合物。 
试回答下列有关问题:
(1)A在元素周期表的位置 周期 族
(2)以上7个化学反应属于非氧化还原反应的是 (用编号①→⑦填写)
(3)写出反应①是 ;
(4)写出引发反应④的实验操作
写出该反应一种重要的工业用途
(5)反应⑤的化学方程式是 。
(5)写出用A与H作电极材料插入G溶液闭合电路后的正极反应式是
。
有X、Y、Z、W四种短周期元素原子序数依次增大,它们之间可以同时相互形成A2B2型、AB型、A2型、A22—型等具有相同电子数的微粒。
(1)当A2型微粒为空气的主要成分时:
①写出上述A22—型微粒电子式 _______________。
②写出四种元素原子按5:1:1:3形成的离子化合物与足量NaOH反应的离子方程式_______________。
(2)当A2型微粒为最活泼的单质时:
①1mol A2B2型化合物分解转移电子的物质的量为_______。
②任写出一种具有相同电子的其他非极性分子的有机物化学式__________
③比较Z与W两种元素的氢化物的沸点与水溶液的酸性。沸点________________酸性______________。
现有E、F、H、I、G、K六种原子序数依次增大的前四周期主族元素,且分属四个不同周期,E、G同主族,F、H、I为同周期相邻的三种元素,其中F元素形成的化合物种类是所有元素中最多的,I、G简单离子具有相同的电子层结构,K与F形成的离子化合物Q与E和I形成的常见共价化合物R之间的反应是实验室常见的可燃气体制备原理。(题中的字母只代表元素代号,与实际元素符号无关),请回答下列问题:
(1)E~K六种元素原子,原子半径第三大的是 (填对应的元素符号,下同)。
(2)E与H两种元素组成一种阳离子,该离子的结构式为 。
(3)I、G两种元素组成含有两种化学键的化合物,该化合物的电子式为
。
(4)下图为常温下向25mL 0.1 mol·L-1由E、I、G组成的化合物W溶液中逐滴滴加0.2 mol·L-1E、F、I组成相对分子质量为60的一元酸Z溶液过程中溶液pH的变化曲线。 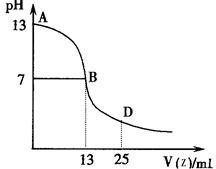
①上图能确定Z为 (“强”或“弱”)酸,理由是
②B点溶液呈中性,有人据此认为,在B点时W与Z恰好完全反应,这种看法是否正确? (选填“是”或“否”)。若不正确,则二者恰好完全反应的点是在AB区间还是BD区间内? 区间(若正确,此问不答)。
(5)写出Q与R之间的化学反应方程式 。
(11分)有A、B、C三种元素,A元素是所有元素中原子半径最小的元素,B、C两元素的核外电子层数相同,C元素的单质为深棕红色液体,B元素的最高价阳离子0.5 mol被还原成中性原子时,需得到1 mol电子,当它同盐酸反应时,放出0.02 g H2,用去B元素0.4 g,则
(1)A元素为______________,B元素为______________,C元素为_______________。
(2)用电子式表示A与C,B与C形成化合物的过程:______________、______________,化学键分别是_________________、_________________。
有A、B、C、D四种短周期元素,它们的原子序数由A到D依次增大,已知A和B原子有相同的电子层数,且A的最外层电子数是次外层电子数的两倍;C的单质燃烧时呈现黄色火焰,C的单质在加热条件下与B的单质反应,可以得到与D单质颜色相同的固态化合物甲;D的最高价与最低价代数和为其最低价绝对值的两倍。据此,回答下列问题:
(1)写出A与B两元素所形成化合物AB2的电子式__________,该化合物分子属于
分子(极性或非极性)。
(2)用电子式表示形成C2D的形成过程: 。
(3)C、D两元素还可以形成化合物C2D2,该化合物性质类似于C2B2,试写出C2D2与稀盐酸反应的化学方程式 。
已知A、E、I、L是常见的非金属单质,其中A为淡黄色固体,Z是常见的金属单质,B的相对分子质量比A大32,C的相对分子质量比B大16,Y是一种常见的液体,J俗称磁性氧化铁,D、H、K均是重要的工业产品,X分子的球棍模型如图所示,图中部分反应条件已略去。

试回答下列问题:
(1)写出化学式:D____________、X____________。
(2)E的电子式为________________________。
(3)写出化学方程式:①______________________________________;
②____________________________________________________________。
下图中A—J分别代表相关反应中的一种物质,已知A受热分解得到相同物质的量的B、C、D(图中有部分生成物未写出)。
请填写以下空白:
(1)B的电子式为____________,D分子的空间构型为____________。
(2)写出反应①②的化学方程式:
①___________________________________________;
②___________________________________________。
(3)反应③的离子方程式为:_______________________________。
A、B、C、D为常见气态单质。已知:
①A和B可以在放电条件下发生化合反应,其产物还可与B化合生成红棕色气体;
②C分别与A、B反应生成的两种化合物分子中都含有10个电子;
③C和D反应生成的化合物易溶于水,在其溶液中滴加AgNO3溶液,生成白色沉淀。
请完成下列问题:
(1)C和D反应生成的化合物的电子式是_______________________。
(2)上述②中化合物的热稳定性_______________强于_______________。(填写化学式)
(3)将D通入B、C生成的化合物中,发生反应的化学方程式是________________________。
(4)A、C、D所含元素可组成一种离子化合物,该化合物发生水解反应的离子方程式是____________________________________。
A、B、C、D、E为中学常见的五种物质,均含元素Y,有的还可能含有元素X、Z,元素X、Y、Z的原子序数依次递增。
①元素Y在A、B、C、D、E中所呈现的化合价依次递增,其中只有B为单质;
②常温下将气体D通入水中发生反应,生成C和E;
③工业上以A、空气和水为原料,通过催化氧化法制取E。
请完成以下问题:
(1)B的电子式为___________,A的结构式为___________,A分子的空间构型是__________;
(2)写出②中涉及反应的化学方程式____________________________________;
(3)由B反应生成1 mol A放出的热量为46.2 kJ,写出该反应的热化学方程式,并注明反应条件________________________;
(4)工业上,若输送Cl2的管道漏气,用A进行检验时可观察到大量白烟,同时有B生成,写出有关反应的化学方程式________________________。
(1)A、B、C的元素名称A______;B_______;C________
(2)A、B的最高价氧化物的水化物的化学式为(按酸性由强到弱顺序排列)__________
(3)A、B、C的氢化物的化学式为(按稳定性由强到弱顺序排列)_________________
(4)B的氧化物与A的单质反应的化学方程式为:_________________________
已知甲、乙、丙为常见单质,A、B、C、D、X、Y、Z为常见的化合物,Y的摩尔质量数值比Z的小16,乙、丙的摩尔质量相同,B的摩尔质量比D的小2,B、X的摩尔质量相同,各物质转化关系如下:
 |
1、写出下列有关物质化学式:丙_________;B _________。
2、写出Y→Z反应化学方程式__________________________。