名师原创题大全
以下是某学生利用集气瓶、导管、稀硫酸、四氯化碳一起设计的一套能“防止倒吸”,并能吸收氨气的装置。下列说法错误的是( )
| A.a为稀硫酸 |
| B.b为四氯化碳 |
| C.若吸收后的溶液中溶质为单一物质时,则不一定显酸性。 |
| D.该吸收过程,表现了硫酸的酸性 |
单斜硫和正交硫转化为二氧化硫的能量变化图如右,下列说法正确的是 
| A.S(s,单斜) = S(s,正交)△H = +0.33kJ·mol -1 |
| B.正交硫比单斜硫稳定 |
| C.相同物质的量的正交硫比单斜硫所含有的能量高 |
| D.①式表示断裂lmol O2中的共价键所吸收的能量比形成1mol SO2中的共价键所放出的能量少297.16kJ |
某有机化合物A的相对分子质量大于100,小于l30。经分析得知,其中碳和氢的质量分数之和为46.66%,其余为氧,则该化合物分子中最多含碳氧双键的个数为( )
A.1 B.2 C.3 D.4
现有E、F、H、I、G、K六种原子序数依次增大的前四周期主族元素,且分属四个不同周期,E、G同主族,F、H、I为同周期相邻的三种元素,其中F元素形成的化合物种类是所有元素中最多的,I、G简单离子具有相同的电子层结构,K与F形成的离子化合物Q与E和I形成的常见共价化合物R之间的反应是实验室常见的可燃气体制备原理。(题中的字母只代表元素代号,与实际元素符号无关),请回答下列问题:
(1)E~K六种元素原子,原子半径第三大的是 (填对应的元素符号,下同)。
(2)E与H两种元素组成一种阳离子,该离子的结构式为 。
(3)I、G两种元素组成含有两种化学键的化合物,该化合物的电子式为
。
(4)下图为常温下向25mL 0.1 mol·L-1由E、I、G组成的化合物W溶液中逐滴滴加0.2 mol·L-1E、F、I组成相对分子质量为60的一元酸Z溶液过程中溶液pH的变化曲线。 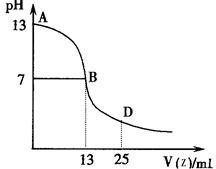
①上图能确定Z为 (“强”或“弱”)酸,理由是
②B点溶液呈中性,有人据此认为,在B点时W与Z恰好完全反应,这种看法是否正确? (选填“是”或“否”)。若不正确,则二者恰好完全反应的点是在AB区间还是BD区间内? 区间(若正确,此问不答)。
(5)写出Q与R之间的化学反应方程式 。
有X、Y、Z、W四种短周期元素原子序数依次增大,它们之间可以同时相互形成A2B2型、AB型、A2型、A22—型等具有相同电子数的微粒。
(1)当A2型微粒为空气的主要成分时:
①写出上述A22—型微粒电子式 _______________。
②写出四种元素原子按5:1:1:3形成的离子化合物与足量NaOH反应的离子方程式_______________。
(2)当A2型微粒为最活泼的单质时:
①1mol A2B2型化合物分解转移电子的物质的量为_______。
②任写出一种具有相同电子的其他非极性分子的有机物化学式__________
③比较Z与W两种元素的氢化物的沸点与水溶液的酸性。沸点________________酸性______________。
物质之间的转化关系如下图,其中A、D、E、F、H为常见单质,其余为化合物,且单质E和单质F在点燃或加热的条件下生成淡黄色的固体,B常温下为液态化合物。 
试回答下列有关问题:
(1)A在元素周期表的位置 周期 族
(2)以上7个化学反应属于非氧化还原反应的是 (用编号①→⑦填写)
(3)写出反应①是 ;
(4)写出引发反应④的实验操作
写出该反应一种重要的工业用途
(5)反应⑤的化学方程式是 。
(5)写出用A与H作电极材料插入G溶液闭合电路后的正极反应式是
。
(14分)已知A是一种含两种元素组成的液态有机溶剂,N带有磁性,B、F、L、O、P是中学化学常见单质, B、D、F、J都含有一种相同的元素且它们的相对分子质量关系是M(D)=2M(B)=2M(F),A和B反应前后气体体积(常温常压)保持不变,I是一种常用的氮肥,反应①②③均是化工生产中的重要反应。
⑴A的化学式___________。
⑵写出反应①的化学方程式_______________________________。
在工业上叫______________
⑶高温下反应⑤⑥互为可逆反应,写出反应⑥的化学方程式___________________
(4)写出在加热条件下单质F与单质L的化学反应方程式___________________________。
(5)请设计一个实验方案,完成反应④,并在答题卡指定位置绘出实验装置图。
某研究性学习小组用下图所示装置制取氯气并探究氯气的性质。请回答下列问题:
请填写下列空白:
(1)制取氯气时,在烧瓶里加入一定量的MnO2和NaCl,通过 (填写仪器名称)向烧瓶中加入适量的浓硫酸。
(2)某同学查阅资料后发现浓硫酸与二氧化锰反应产生氧气。先需要你帮该同学设计一个实验,既要完成(3)、(4)的实验,又要探究有氧气产生的实验。仪器连接顺序为a→( )→( )→d→e→( )→( )→( )→( )→l,证明有氧气的操作是 ,写出浓硫酸与二氧化锰反应产生氧气的化学方程式
(3) 实验中可观察到③的锥形瓶里溶液的颜色变化
(4)取出④中的集气瓶进行氯气与铜的反应实验,应该进行的操作是 后立刻放入充满氯气的集气瓶中。实验中有同学提出应该在集气瓶底先放少量的水或细沙,你认为是否一定要放 ;理由是 。
某学校探究性学习小组对消毒液次氯酸钠(NaClO)的制备与性质等进行了探究。
甲同学:为制备消毒液,探究并制作了一种家用环保型消毒液(NaClO溶液)发生器,设计了如图所示的装置,用石墨作电极电解饱和氯化钠溶液。
请完成下列问题:若通电时,为使生成的Cl2被完全吸收,制得有较强杀菌能力的消毒液,则电源的a电极名称为 极(填“正”、“负”、“阴”或“阳”);装置溶液中反应生成NaClO的离子方程式为: 。
乙同学:从某超市中查询到某品牌消毒液包装说明的部分内容,摘录如下:
主要有效成份为次氯酸钠,有效氯含量8000-10000mg/L。可用于各类家居用品、餐具、棉织衣物等的消毒,对彩色织物可能有褪色作用。切勿用于丝绸、毛、尼龙、皮革、油漆表面,勿用于铝、铜、碳钢制品。本品须密封,置阴凉暗处保存。
请完成以下实验探究过程:
I.阅读材料,根据学过的知识判断问题
(1)室温条件下,该消毒液(NaClO)的不显中性的原因是(用离子方程式表示)
_____________________。
(2)该消毒液还具有的化学性质是_________(填序号)。
A.强氧化性 B.强还原性 C.不稳定性 D.漂白性 E.弱酸性
(3)从该消毒液的保存要求分析,导致其失效的主要原因是(用化学方程式表示)
_ 。
II.确定要研究的问题
该消毒液对碳钢制品的腐蚀原理。
III.设计方案,实施探究
(1)用烧杯取少量样品,将一颗光亮的普通碳钢钉放入烧杯,浸泡一段时间。
预期的实验现象是_________________________________。
(2)为了进一步探究铁钉在该漂白剂(NaClO)溶液中的腐蚀原理,丁同学设计了如下图实验装置,写出碳(C)极上发生的电极反应式: 。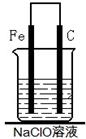
已知:G是一种常用的药用有机物,合成路线如图所示:
①有机物A和C都能与FeCl3发生显色反应,且取代基处于邻位
②有机物G只含碳、氢、氧元素且式量小于200,氧元素的质量分数为35.56%。
请回答:
(1)写出A、C、K的结构简式A________C________K__________
(2)反应①~⑨中,属于取代反应的有______________(填序号)
(3)写出F的常见同分异构体与F在浓硫酸条件下的反应_____________________
(4)写出G在加热条件下与NaOH溶液反应的化学方程式_______________________
(5)写出反应⑥的方程式____________________。
已知有机物A~I之间的转化关系如图所示:
①A与D、B与E、I与F互为同分异构体
②加热条件下新制Cu(OH)2悬浊液分别加入到有机物I、F中,I中无明显现象,F中变砖红色。
③C的最简式与乙炔相同,且相对分子质量为104
④B的一种同分异构体与FeCl3发生显色反应。
根据以上信息,回答下列问题:
(1)C中含有的官能团名称为
(2)H的结构简式为
(3)反应①~⑨中属于取代反应的是
(4)写出反应⑥的化学方程式
(5)写出 F与新制Cu(OH)2悬浊液反应的化学方程式
(6)苯环上含有两个取代基且能与NaOH溶液反应,但不与FeCl3发生显色反应的G的同分异构体有
种.
已知有机物A分子中含有苯环且只有一个侧链。有机物A的相对分子质量M不超过200,其中氧元素的质量分数为26.7%,完全燃烧只生成水和二氧化碳。与之有关的有机物转化关系如下:(注意:部分反应产物省略)
(1)有机物A中含有官能团的名称分别为________________,A的分子式为____________。
(2)有机物C的结构简式为________
(3)有机物A~F中互为同分异构体的有____________和______________(填写序号)
(4)有机物A~F中不能使溴的四氯化碳溶液褪色的有_________________(填写序号)
(5)16.2g有机物BCD组成的混合物完全燃烧,得到的CO2通入3mol/LNaOH溶液中得到的产物为________________。
(6)写出A+D生成E的化学方程式_____________________________。
 2C(g),根据下表中的数据判断下列图像错误的( )
2C(g),根据下表中的数据判断下列图像错误的( )
 粤公网安备 44130202000953号
粤公网安备 44130202000953号