和空气接触可发生非氧化还原反应的物质组合是
①Na ②Na2SiO3溶液 ③Na2O2 ④烧碱溶液 ⑤石灰水 ⑥Fe(OH)2
| A.①③④ | B.②④⑤ | C.②③⑥ | D.①④⑤ |
下列推断正确的是
| A.SiO2是酸性氧化物,能与NaOH溶液反应 |
| B.Na2O、Na2O2组成元素相同,与CO2反应产物也相同 |
| C.CO、CO2都是大气污染气体,在空气中都能稳定存在 |
| D.新制氯水显酸性,向其中滴加少量紫色石蕊试液,充分震荡后溶液显红色 |
随着人们生活节奏的加快,方便的小包装食品已被广泛接受。为了延长食品的保持期,防止食品受潮变质,在包装袋中可以放入的化学物质是
| A.硅胶 | B.硫酸亚铁 | C.食盐 | D.石灰石 |
根据实验操作和现象所得出的结论正确的是( )
| 选项 |
实验操作 |
实验现象 |
结 论 |
| A |
将盐酸滴入Na2CO3溶液中 |
有气泡产生 |
氯非金属性比碳强 |
| B |
向2mL 0.1mol/L MgCl2溶液中加入2 mL 1mol/L 的NaOH。观察到白色沉淀后加入2滴FeCl3,静置 |
出现红褐色沉淀 |
同温下 Ksp[Mg(OH )2] >Ksp[Fe(OH)3] |
| C |
向某溶液中滴加KSCN溶液 |
溶液显红色 |
证明原溶液中有Fe3+,无Fe2+ |
| D |
分别将乙烯与二氧化硫通入到酸性高锰酸钾溶液中 |
高锰酸钾溶液均褪色 |
两种气体使酸性高锰酸钾褪色原理相同 |
某溶液中可能含有下列6种离子中的某几种:Cl—、SO42—、CO32—、NH4+、Na+、K+。为确认溶液组成进行如下实验:(1)200mL上述溶液,加入足量BaCl2溶液,反应后将沉淀过滤、洗涤、干燥,得沉淀4.30g,向沉淀中加入过量的盐酸,有2.33g沉淀不溶。(2)向(1)的滤液中加入足量的NaOH溶液,加热,产生能促使湿润红色石蕊试纸变蓝的气体1.12L(已换算成标准状况,假定产生的气体全部逸出)。由此可以得出关于原溶液组成的正确结论是
| A.一定存在SO42—、CO32—、NH4+,可能存在Cl—、Na+、K+ |
| B.一定存在Cl—、SO42—、CO32—、NH4+,一定不存在Na+、K+ |
| C.c(CO32—)=0.01mol·L-1,NH4+>SO42— |
| D.如果上述6种离子都存在,则c(Cl—)>c(SO42—) |
有关物质间转化关系如下图,试回答:
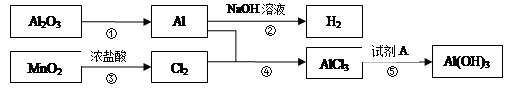
据此判断:
(1)转化①的反应条件为 。
(2)转化②的化学方程式为 。
(3)若转化⑤用于实验室制Al(OH)3,则试剂A宜选择 填名称)。
(4)转化⑤的离子方程式为 。
除去下列溶液中的杂质(括号内是杂质)所用试剂正确的是
| A.Cl2(HCl):饱和食盐水 | B.FeCl2溶液(FeCl3):Cu |
| C.NaHCO3溶液(Na2CO3):NaOH | D.CO2(HCl ):Na2CO3溶液 |
下列鉴别物质的方法能达到目的的是
| A.用加热、称重的方法鉴别Na2CO3固体和NaHCO3固体 |
| B.用焰色反应鉴别NaCl固体和NaOH固体 |
| C.用KSCN溶液鉴别FeCl3溶液和Fe2(SO4)3溶液 |
| D.用丁达尔效应鉴别NaCl溶液和KCl溶液 |
只用一种试剂即可区别NaCl、MgCl2、FeCl2、Al2 (SO4) 3四种溶液,这种试剂是
| A.AgNO3 | B.HCl | C.BaCl2 | D.NaOH |
在化学学习中常可根据已知的实验事实,对某些物质的化学性质作出推测,请判断下列推测合理的是
| A.从红热的铜丝能在氯气中燃烧,推测红热的铁丝也能在氯气中燃烧 |
| B.从碘单质使淀粉试液变蓝,推测 I-也能使淀粉试液变蓝 |
| C.从Fe能从CuSO4 溶液中置换出Cu,推测Na也能从CuSO4 溶液中置换出Cu |
| D.从二氧化碳通入Ca(OH)2 溶液能产生白色沉淀的事实,推测二氧化碳通入CaCl2 溶液也能产生白色沉淀 |