俄罗斯科学家最近合成了核电荷数为139元素的原子,经测定该原子质量为4.89946×10-25kg(已知碳原子质量为1.993×10-26kg)计算:
(1)则该原子的相对原子质量是多少?
(2)该原子中子数为多少?
(3)中子数与电子数之差是多少?
取10g金属锌样品(假设其中杂质和硫酸不反应,也不溶于水),加入到试管中,和足量的稀硫酸充分反应后,得到0.2g氢气。请回答下列问题。
(1)写出发生反应的化学方程式 ;
(2)求解参加反应的硫酸质量(X)的比例式为 ;
(3)生成硫酸锌的质量为 ;
(4)原金属锌样品的纯度(锌的质量分数)为 ;
有碳酸镁与氧化镁的混合物共重12.4克,把该混合物加入到192克稀盐酸中恰好完全反应,称得反应后溶液的质量为200克.试计算反应后所得溶液中溶质的质量分数.(写出具体计算过程)
某品牌洁厕灵的成分是硫酸与盐酸的混合溶液.某课外活动小组想测定20g该
品牌洁厕灵溶液中H2SO4和HCl的质量.取20g该品牌的洁厕灵溶液于烧杯中,不断滴加溶质质量分数为17.1%的氢氧化钡溶液,反应过程中烧杯中产生沉淀质量和烧杯中溶液pH变化的部分数据如下所示:
滴加氢氧化钡溶液的质量/g5 10 25
烧杯中产生沉淀的质量/g1.165 2.33 4.66
(已知BaCl2溶液的pH=7;Ba的相对原子质量137)
求:20g该品牌洁厕灵溶液中H2SO4的质量和HCl的质量.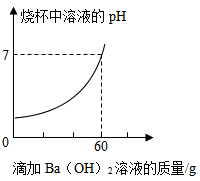
小希同学欲测定某氢氧化钠溶液中溶质的质量分数.取10g该氢氧化钠溶液,向其中滴加溶质的质量分数为7.3%的稀盐酸至恰好完全反应,得到20g不饱和溶液.求:
(1)稀盐酸的质量.
(2)该氢氧化钠溶液中溶质的质量分数.
实验室欲配制84g质量分数为10%的碳酸氢钠溶液用于实验,请计算:
(1)需要碳酸氢钠的质量为 g.
(2)已知碳酸氢钠与稀盐酸发生如下反应:NaHCO3+HCl═NaCl+CO3↑.向84g 10%的碳酸氢钠溶液 中加入一定量的稀盐酸,恰好完全反应,反应后剩余溶液质量为117g(假设生产的气体全部逸出).求:
①生成氯化钠的质量;
②所得溶液中溶质质量分数.
某同学测定一瓶标签残缺的硫酸镁溶液的溶质质量分数,取30g该溶液,向其中逐滴加入溶质质量分数为10%的氢氧化钠溶液.生成沉淀的质量与所用氢氧化钠溶液的质量关系如图所示.反应方程式为:MgSO4+2NaOH=Na2SO4+Mg(OH)2↓

(1)配制100g溶质质量分数为10%的NaOH溶液,需NaOH的质量为 g.
(2)计算MgSO4溶液中溶质的质量分数(列式计算).
某实验小组为探究酸的化学性质,由甲、乙同学设计并完成了如图所示的实验.
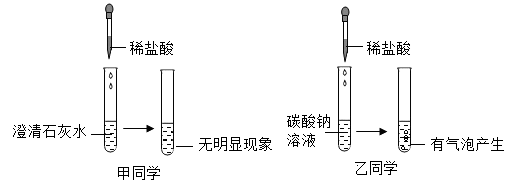
(1)甲同学实验中所发生的化学方程式为 .
【查阅资料】CaCl2、NaCl的溶液呈中性,Na2CO3溶液呈 (填“酸”或“碱”)性.
【实验探究一】确定甲、乙同学上述实验后所得溶液中的溶质.
(2)取甲所得溶液少许,加入石蕊试液,溶液显红色,甲所得溶液中一定含有的溶质是 (写化学式)
(3)取乙所得溶液少许,加入酚酞试液,溶液显红色,乙所得溶液中一定含有的溶质是 (写化学式)
【实验探究二】
(4)甲、乙同学把上述实验所得溶液倒入同一废液缸中,观察到废液缸中产生少量气泡,最终有白色沉淀生成,该白色沉淀是 (写化学式).
【讨论交流】丙同学提出:若将上述废缸中物质取出,过滤,所得滤液中含有哪些物质呢?经过讨论大家一致认为:一定含有NaCl,可能含有CaCl2、盐酸和Na2CO3中的部分物质.
【实验探究三】取少量滤液于试管中,滴加过量的稀硝酸,可观察到有大量气泡产生.
【归纳总结】该滤液中含有的溶质是氯化钠和 (写化学式).
【探索与拓展】有一份由Na2SO4、NaCl两种物质组成的固体样品.为确定其组成,上述小组同学将样品全部溶于蒸馏水中制成119.3g溶液,再往其中加入104gBaCl2溶液,两者恰好完全反应.过滤,得到23.3g白色沉淀和一定质量的滤液.经测定,该滤液中溶质质量分数为9%.试计算:(均需计算过程)
(5)所用B2Cl2的溶液中溶质的质量分数.
(6)所用样品的质量.
硅钢是制变压器、充电器的核心材料,其主要成分是Fe和Si.某同学用硅钢样品进行如下实验:取6.60g硅钢样品,将60.00g稀硫酸分6次加入样品中(其中稀硫酸与硅及其它杂质不反应).实验测得相关数据如表:

(1)根据表中数据判断,稀硫酸加入到第 次,铁恰好反应完全.
(2)表中W= g
(3)计算该稀硫酸溶质的质量分数(写出过程)
我市盛产石灰石,主要成分是
。某同学为了测定石灰石中碳酸钙的质量分数进行了如下实验。取一定量的石灰石样品研碎和
溶质质量分数为10%的稀盐酸放入烧杯中。在化学反应过程中对烧杯及其中的剩余物进行了五次称量,记录数据如下表:(假设反应匀速进行;杂质不溶于水,也不与稀盐酸反应,烧杯的质量为
。)
| 反应时间/s |
20 |
40 |
60 |
80 |
100 |
| 烧杯和药品质量/g |
137.8 |
135.6 |
m |
134.5 |
134.5 |
请计算:
(1)表中的"
"为
;
(2)该石灰石样品中碳酸钙的质量分数。(计算结果精确至0.1 % )
测定铁制品中铁的质量分数
铁是常用的金属材料,兴趣小组的同学对某铁制品中的质量分数进行测定.称取3
铁屑,缓慢加入一定溶质质量分数的硫酸溶液,直到过量(假设除铁以外的物质都不与硫酸反应),实验数据如图所示.

请计算:
(1)该铁制品中的铁的质量分数.(最终结果保留到0.1%)
(2)所用硫酸溶液的溶质质量分数.(要求有计算的过程)
某合作学习小组的同学们.欲测定一定量的某种石灰石样品中碳酸钙的质量,进行了如下实验:

(1)配制溶质质量分数为7.3%的稀盐酸.
①配制100
溶质质量分数为7.3%的稀盐酸,需图1所示盐酸的质量
。
②量取盐酸与水时,视线要与量筒内液体凹液面的保持水平.再读出液体的体积;将两种液体都倒入中(填仪器名称),用玻璃棒搅拌,使溶液混合均匀。
(2)将(1)中配制好的稀盐酸加人盛有石灰石样品的烧杯中,产生气体的质量与加入稀盐酸的质量关系如图2所示(假设石灰石样品中的杂质不与稀盐酸反应)。
计算:该石灰石样品中碳酸钙的质量。
现将10g铜锌(Cu﹣Zn)合金放入到一定质量的稀硫酸中恰好完全反应,过滤得到100g溶质质量分数为16.1%的溶液.据此请完成下列问题:
(1)生产氢气 g;
(2)稀硫酸中H2SO4的质量是 g;
(3)合金中铜的质量分数是多少?
永州市某中学的初三化学课堂上,刘老师布置了一道计算题,题目如下:取100g溶质质量分数为8%的氢氧化钠溶液于烧杯中,向其中加入100g19.6%的稀硫酸,充分反应后,求所得溶液中硫酸钠的质量分数.
检查作业发现,班上出现了下表所示的两种情形:
| 结果编号 |
① |
② |
| 计算结果 |
14.2% |
7.1% |
请你分析并回答:
(1)你赞同的计算结果是 (填结果编号)。
(2)请写出该题正确计算的详细过程。
将6g生铁样品加入到盛有100g过量硫酸的烧杯中(样品中杂质不溶于水,也不与稀硫酸反应),充分反应后,称得烧杯内剩余物质的总质量为105.8g,试行算:
(1)
的相对分子质量为;
(2)生成
的质量为;
(3)该生铁样品中铁的质量分数(要写出计算步骤,结果保留一位小数)