家庭厨房或卫生间的管道常被厨余垃圾或脱落的头发堵塞而令人烦恼.市面上有固态、液态两种管道疏通剂,研究小组购买了这两种管道疏通剂进行探究.
【查阅资料】
①固态管道疏通剂主要成分为NaOH、NaNO 3和铝粉.
②铝粉能与NaOH溶液反应并能放出热量,其化学方程式为:2Al+2NaOH+2H 2O=2NaAlO 2+3H 2↑.
③BaSO 4、BaCO 3都不溶于水,BaSO 4也不溶于酸.
探究一:
【提出问题】固态管道疏通剂能够疏通管道的原理是什么?
【实验验证】
| 操作 |
现象 |
解释与结论 |
| 将菜叶、头发、米饭等垃圾放入烧杯中,然后加入少量固态管道疏通剂,再加入 . |
烧杯中产生大量气泡,烧杯壁发热,垃圾翻动,一段时间后菜叶、米饭部分溶解并分散成小颗粒,头发变成碎屑. |
反应中产生的 使垃圾翻动. NaOH使垃圾分散成小颗粒,头发变成碎屑. |
【反思评价】经过大家讨论,认为固态管道疏通剂虽然能疏通管道,但使用过程中不安全,理由是 ;
目前超市出售更多的是液态管道疏通剂.液态管道疏通剂的成分主要是NaOH和一种钠盐.
探究二:
【提出问题】液态管道疏通剂中除NaOH以外,另一种钠盐是什么呢?
【猜想假设】这种钠盐是NaCl、Na 2SO 4、Na 2CO 3、NaNO 3中的一种.
【实验验证】(不考虑疏通剂中其它成分对实验的影响)
| 操作 |
现象 |
结论 |
| 取少量液态疏通剂加入试管中,滴加 溶液. |
产生白色沉淀 |
该钠盐是Na 2SO 4,写出该反应的化学方程式: . |
【提出质疑】同学们认为该实验不能证明这种钠盐一定是Na 2SO 4,理由是 ,
请你补充一个实验证明该钠盐是Na 2SO 4: ;
【拓展延伸】NaOH有强烈的腐蚀性,能腐蚀皮肤和衣物等,但管道疏通剂正是利用了它的腐蚀性,将"弊"变"利".请你再举出一个利用物质的"弊"为生活服务的例子: .
某兴趣小组的同学从超市购买一袋食盐,欲检测其是否为加碘食盐(加碘食盐中的碘元素以碘酸钾的形式存在,碘酸钾的化学式为KIO 3).他们査阅资料得知,加碘食盐中的KIO 3在酸性条件下能与KI溶液发生反应,生成碘(I 2),淀粉遇I 2变蓝色.
现提供下列试剂和生活中常见的物质:
①KI溶液②纯碱③米汤④白糖⑤白酒⑥白醋,该小组同学进行实验必须选用的试剂和物质是 .
A.①③④B.①③⑥C.②④⑥D.①④⑤
该小组经过实验确定这袋食盐是加碘食盐,同学们探究的兴趣高涨,他们仔细阅读加碘食盐包装袋上的说明后,提出问题并与其他同学讨论,继续进行实验探究.
问题一:食盐是比较稳定的,而说明中强调"防热",是否因为受热会造成碘的损失?
【实验一】探究温度对碘损失率的影响.
老师指导他们将一定浓度的碘酸钾溶液分成5等份,在不同温度下加热十分钟后,用硫代硫酸钠标准溶液测定碘酸钾溶液的浓度,计算碘损失率并记录如表:
| 温度 |
30℃水浴 |
50℃水浴 |
80℃水浴 |
100℃水浴 |
煮沸 |
| 碘损失率(%) |
0 |
0.3 |
0.67 |
1 |
5.56 |
分析上表可得出的结论是 .
问题二:炒菜时加醋对碘的损失率是否也有影响?
【实验二】探究酸碱度对碘损失率的影响.
(1)此组对照实验,要控制在碘酸钾溶液的浓度和质量、加热的 均相同,溶液的酸碱度不同的条件下进行.
(2)实验需要调节溶液的酸碱性,下列物质不能选用的是 (填字母)
A.氢氧化钠 B.纯碱粉末 C.食盐晶体 D.食醋.
叠氮化钠(NaN 3)被广泛应用于汽车安全气囊,某化学小组同学对其进行下列研究。
【査阅资料】
①NaN 3受撞击会生成Na、N 2
②NaN 3遇盐酸、H 2SO 4溶液无气体生成
③碱石灰是CaO和NaOH的混合物
④NaN 3的制备方法是:将金属钠与液态氨反应制得NaNH 2,再将NaNH 2与N 2O反应可生成NaN 3、NaOH和NH 3
【问题探究】
(1)汽车受撞击后,30毫秒内引发NaN 3迅速分解,该反应的化学方程式为 ;
(2)工业级NaN 3中常含有少量的Na 2CO 3,其原因是 (用化学方程式表示);
(3)为测定某工业级NaN 3样品中Na 2CO 3的质量分数,小组同学设计了如图实验装罝:
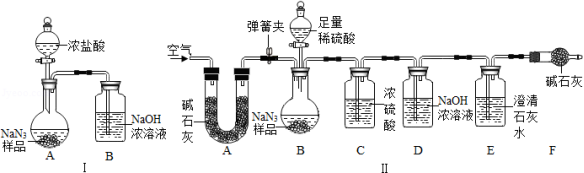
①小明同学认为通过测定装置I中反应前后B的质量差,再通过相应计算,就可测定Na 2CO 3的质量分数,小组同学通过讨论认为不可行,其理由可能是 (答出一种即可)
②小明同学在大家讨论的基础上,又设计了装罝Ⅱ,请分析:装置Ⅱ中A的作用是 。若无装置C,对测定结果造成的影响是 (填"偏大"、"偏小"或"无影响")。装置E的作用是 。
③根据装置Ⅱ,小组同学设计的实验步骤有:
a.称量装置D
b.称量样品,检査装置气密性
c.打开弹簧夹,鼓入空气
d.关闭弹簧夹,打开分液漏斗的活塞和玻璃塞,注入足量的稀琉酸,关闭活塞和玻璃塞。
其正确的顺序为 (填字母序号,可重复)
④计算碳酸钠的质量分数时,至少需要测定 个数据。(填数字)
某同学用微型实验装置(如图)制取二氧化碳并检验其性质,回答问题。

(1)试管中发生反应的化学方程式是 。
(2)b处出现的现象是 。
(3)根据烧杯中的变化现象,得出二氧化碳的化学性质是 。
(4)另一同学操作时,误将浓盐酸当稀盐酸使用,结果 处没有明显现象。
(5)你认为微型实验的优点是 (写一条即可)
小明在学习金属活动性顺序时,对课本上"活动性较强的金属一般可以将位于其后面的金属从它们的盐溶液中置换出来"这句话产生了好奇,为什么用"一般"这个词呢?难道还有例外吗?
【查阅资料】金属Na性质活泼,常温下与氧气反应,也可以与水反应放出氢气.
【实验与分析】
①在实验室中,金属钠保存在煤油中;
②用镊子从煤油中取出金属钠,用滤纸吸干其表面的煤油,用小刀切下一小块,投入蒸馏水中,发现钠块立刻熔化成银白色小球,在水面上到处游动,滴入酚酞试液后水变成红色;
③往硫酸铜溶液中投入一小块钠,又出现蓝色沉淀,但没有红色物质析出.
(1)金属钠保存在煤油中的原因是 .
(2)从②中,你能得到哪些信息?(任写两条) , .
(3)写出钠与硫酸铜溶液反应的化学方程式 ; .
【结论】在金属活动性顺序中,活动性较强的金属不一定能将位于其后面的金属从它们的盐溶液中置换出来.
小丽家里的下水道被毛发、食物残渣等杂物堵塞了,她爸爸买了一瓶管道通回来,经过短时间的浸泡使用,堵塞的下水道很快就疏通了,管道通是怎样使堵塞的下水道变得重新疏通呢?小丽产生了强烈的好奇,决定与化学兴趣小组的同学对管道通的成分及性质进行研究.
【查阅资料】
1.管道疏通剂的说明书:疏通剂的主要成分是NaOH固体和Al粉
2.NaOH溶液会与Al发生反应生成NaAlO 2
【实验模拟】在实验室里,小丽取出了一些NaOH固体和Al粉混合后,放入盛有水的试管中,观察到反应剧烈,有大量气泡产生,且试管壁发烫.
对于试管壁发烫的原因,学习小组的同学认为可能是 的原因,也可能是 的原因.
【猜想与假设】产生的气泡可能是什么气味?
同学们纷纷提出了自己的猜想:
1.小李认为该气体是氧气,小张认为是氢气.
2.你认为该气体可能是氧气和氢气的混合气体外,还可能是 .
【验证假设】
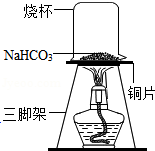
小丽设计了如图所示装置进行实验,该气体的收集方法叫 .小丽在用该方法收集气体时,等大量气泡生成一段时间后再进行收集,其目的是 .
小李拿一根带火星的木条伸到集满气体的B试管中,如果他的假设是正确的,将看到 现象.而现在发现B试管中的气体能被点燃,产生淡蓝色的火焰,该实验现象证明了小张的猜想是正确的.
经试验确定A试管中反应后只有NaAlO 2一种溶质,写出A试管中反应的化学方程式: .
【原理分析】
对于Al为什么能与氢氧化钠溶液反应生成氢气的原因,大家进一步提出自己的猜想,小李认为,Al的金属活动性排在H之前,所以置换出NaOH"分子"中的"H".但他的观点遭到了大家的反对,因为 .
小丽猜想是Al的性质比较特殊的原因,经过网络查找,大家终于明白了疏通反应的原理.
【交流反思】根据上述实验及NaOH的性质,请你提出一条保管或安全使用管道疏通剂的建议: .
糕点疏松的主要成分中含有碳酸氢钠,某化学兴趣小组对碳酸氢钠的化学性质进行探究。
【探究实验一】 碳酸氢钠溶液的酸碱性:用玻璃棒蘸取碳酸氢钠溶液在pH试纸测上并与 对比,读出其pH值约为10,由此得出结论是:碳酸氢钠溶液呈碱性。
【探究实验二】碳酸氢钠能否与酸反应:取少量固体放入试管中,滴加足量的稀盐酸,现象为 。结论:碳酸氢钠能与酸反应。
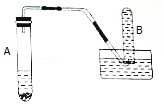
【探究实验三】碳酸氢钠的热稳定性:取一定量的碳酸氢钠放在铜片上加热,如图所示。
(1)加热一段时间后,观察到烧杯内壁有水珠。
(2)充分加热后,将烧杯迅速倒转过来,加入适量的澄清石灰水,振荡,观察到石灰水变浑浊。
(3)通过进一步实验来确定充分加热后的固体产物的成分。限选试剂及仪器:稀盐酸、氯化钙溶液、澄清石灰水、酚酞溶液、蒸馏水、试管、胶头滴管
| 序号 |
实验操作 |
预期现象 |
结论 |
| ① |
取少量加热后的固体产物放入试管A中,加入适量蒸馏水,充分振荡溶解,滴加足量 氯化钙溶液,振荡,静置 |
产生白色沉淀 |
产物含 |
| ② |
取操作①后的上层清液于试管B中,滴加
|
|
产物不含NaOH |
请分析上述操作①中不能用澄清石灰水替代氯化钙溶液的理由 。
(4)根据上述实验结论,写出碳酸氢钠受热分解的化学方程式 。
氢化钠与水反应的化学方程式为:NaH+H 2O═NaOH+H 2↑.在实验室里,小强先取一定量的硫酸铜溶液于烧杯中,再将少量氢化钠加入硫酸铜溶液中,充分反应后过滤得到滤液和蓝色滤渣。并对滤液的成分进行探究。
【提出问题】滤液中溶质的成分是什么?
【查阅资料】Na 2SO 4溶液呈中性
【猜想与假设】猜想一:Na 2SO 4
猜想二:
猜想三:Na 2SO 4和CuSO 4
猜想四:Na 2SO 4、CuSO 4和NaOH
【讨论与交流】:小玲认为猜想 不合理,理由是 (用化学方程式表示)。
【实验与结论】
| 实验 |
实验操作 |
实验现象 |
实验结论 |
| 实验一 |
取少量滤液于试管中,仔细观察现象 |
溶液为无色 |
猜想 不成立 |
| 实验二 |
向实验一所取滤液中滴入酚酞溶液 |
|
猜想二成立 |
| 实验三 |
常温下,再取少量滤液,测溶液酸碱度 |
pH>7 |
猜想 不成立 |
如图是实验室常用的部分实验装置。请按要求回答问题。
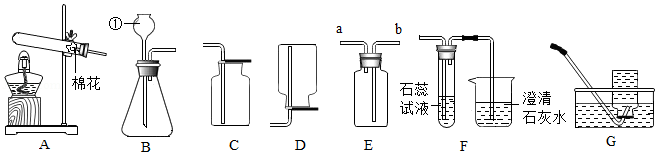
(1)写出标有编号的仪器名称① 。
(2)写出A中发生反应的化学方程式 ,用E装置检验氧气收集满的方法是 。
(3)将装置B、E、F相连接用于制取纯净的二氧化碳气体并验证其化学性质,则E装置中装有的试剂是 ;F装置中可观察到试管中的现象 。写出烧杯中发生反应的化学方程式 。
(4)实验室用加热氯化铵和熟石灰的固体混合物制取氨气。已知氨气极易溶于水且密度小于空气,所选的发生装置和收集装置是 。
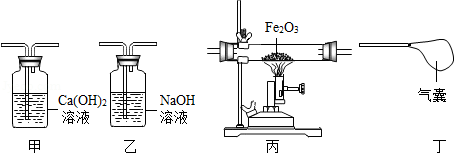
(5)某同学利用少量混有少量CO 2的CO还原Fe 2O 3,并验证反应后的气体产物。现有如图所示实验装置(可重复使用),按气体流向从左到右,装置的正确连接顺序是乙→ →丁。
兴趣小组获得两包制作"跳跳糖"的添加剂,一包是柠檬酸晶体,另一包是标注为钠盐的白色粉末。将少量柠檬酸和这种白色粉末溶于水,混合后产产生了使澄清石灰水变浑浊的气体。于是对白色粉末的化学成分进行了以下探究:
【提出猜想】猜想1.碳酸钠;猜想2.碳酸氢钠;猜想3.碳酸钠和碳酸氢钠
【查阅资料】①碳酸钠溶液、碳酸氢钠溶液均呈碱性;
②碳酸氢钠受热分解生成碳酸钠、水和二氧化碳;碳酸钠受热不分解
【实验探究】小月、小妮分别对有关猜想设计方案并进行实验:
| |
实验操作 |
实验现象 |
实验结论 |
| 小月 |
将白色粉末溶于水后用pH试纸测定其酸碱度 |
pH 7(填">"、"<"或"=") |
溶液呈碱性,猜想1成立 |
| 小妮 |
用如图所示的装置进行实验 |
试管A中有水珠产生,试管B中液体变浑浊 |
猜想2成立,试管B中反应的化学方程式为 。 |
【交流反思】大家一致认为小月和小妮的结论不准确:
(1)小月实验结论不准确的原因是 ;
(2)小妮的实验方案不能排除白色粉末是否含有 。
【继续探究】小戚称取mg白色粉末与足量稀盐酸反应,充分反应后生成二氧化碳的质量为n g,通过计算并分析实验数据确定猜想3正确,则n的取值范围为 (用含m 的代数式表示)。
【结论分析】探究后他们核查到添加剂的成分是柠檬酸和碳酸氧钠,分析后认为白色粉末中的碳酸钠是由碳酸氢钠分解产生的。
【拓展应用】下列物质常温下放置一段时间也会分解的是 (填序号)。
A.浓硫酸 B.氢氧化钠 C.碳酸氢铵 D.氯化钠。

为了解甲酸的分解产物,实验小组进行了以下探究:
【查阅资料】甲酸(HCOOH)的熔点为8.6℃,能分解生成两种物质。
【提出猜想】实验小组对甲酸的分解产物提出了猜想:
猜想1.H 2和CO 2;猜想2.CO和H 2O。
【设计实验】20℃时,甲酸的状态为 ;从图一装置中选择合适的装置 (填序号)对甲酸进行加热。为了加快分解速率,实验小组加入了催化剂,反应后将分解产物通入图二装置进行实验。
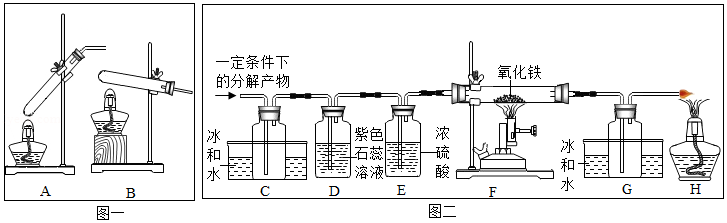
【实验预测】若猜想l成立,则D中的实验现象应为 。
【进行实验】实验中观察到C处瓶内出现大量水珠,F处玻璃管中出现的现象为 ,甲酸分解的化学方程式为 。
【交流拓展】资料表明,不同条件下,甲酸的分解产物不同,猜想1和猜想2均能成立。据此小新对甲酸的分解产物又提出新猜想:猜想3.H 2O和CO 2;猜想4.CO和H 2.经讨论认为无需进行实验就能确定猜想3和猜想4都错误,理由是 。