小文研学旅行时,对“自热米饭”发热包的发热现象感到好奇。返校后,利用化学实验室中已有的生石灰、活性炭、铁粉、碳酸钠、氯化钠、硫酸钠中的若干种物质自制了一个发热包。发现使用自制发热包时,可迅速升温,还可保温较长时间。
小静同学对小文同学自制发热包的成分进行探究。
【实验探究】
小静取适量自制发热包中的固体放入盛有水的烧杯中,迅速放出大量的热,她认为是固体样品中的生石灰与水发生反应产生了热量。为了进一步确认发热包中物质的成分,小静把烧杯中的物质过滤,得到滤液A和滤渣B。
|
实验步骤 |
实验操作 |
实验现象 |
分析与结论 |
|
① |
取适量滤渣B放入烧杯中 |
观察到滤渣B慢慢出现红棕色固体,触摸烧杯外壁感到微热并持续了较长时间 |
红棕色固体是 |
|
② |
取适量滤液A放入试管中,加入过量的氯化钡溶液 |
有白色沉淀生成 |
发热包中除含有生石灰外,一定还含有的物质是 |
|
③ |
取②中的白色沉淀放入试管中,加入足量的稀硝酸 |
白色沉淀全部溶解,有气泡产生 |
|
|
④ |
取②反应后的上层清液放入试管中,先加入足量稀硝酸,再滴入适量 溶液 |
有白色沉淀生成 |
|
|
⑤ |
取适量滤渣B放入试管中,加入足量的稀盐酸 |
固体部分溶解,溶液呈浅绿色,有气泡产生 |
【反思与交流】
(1)步骤②反应后的上层清液中含有的离子共有 种。
(2)步骤④中生成白色沉淀的化学方程式是 。(任写一个)
(3)发热包中的物质使用前必须 保存,使用后注意合理回收。
实验活动课上,老师为大家演示兴趣实验,振荡留有小孔的盒子,将里面的黑色粉末均匀地洒在酒精灯火焰的上方,观察到火星四射的灿烂烟花。老师揭秘黑色粉末是食品包装袋中的脱氧剂。为此兴趣小组展开了对该脱氧剂成分及原理的探究。
实验活动一:探究脱氧剂中黑色粉末的成分。
【作出猜想】黑色粉末含有铁粉和碳粉中的一种或两种。
【实验探究】小组同学设计实验方案并完成如下实验:
|
实验步骤 |
实验现象 |
实验结论 |
|
①取黑色粉末放入烧杯中,加入稀盐酸。 |
,溶液变为浅绿色,有黑色不溶物。 |
黑色粉末中含有铁粉,反应的化学方程式为 。 |
|
②将①中黑色不溶物滤出,洗涤、干燥后,放在石棉网上灼烧,上方放一蘸有澄清石灰水的玻璃片。 |
。 |
黑色粉末中含有碳粉。 |
【查阅资料】实验所用脱氧剂中还含有氯化钠
实验活动二:探究脱氧剂中氯化钠的作用。
【实验探究】小组同学用控制变量法按如图装置进行实验:
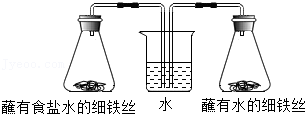
一段时间后观察到烧杯内左侧导管液面 右侧导管液面(填“高于”或“低于”)。
【表达交流】脱氧剂利用铁生锈的原理延长食品保质期。其中碳粉具有 性,可以促进反应的发生,氯化钠可以加快铁生锈的反应速率。
实验活动三:探究溶液中溶质的成分。
【实验探究】小组同学用老师提供的完全变质的同种脱氧剂设计并完成如下实验:
|
实验步骤 |
实验现象 |
实验结论 |
|
①取适量完全变质的脱氧剂放入烧杯中,加入稀盐酸。 |
溶液由无色变为黄色,有黑色不溶物。 |
反应的化学方程式为 。 |
|
②取①中过滤后的滤液,向其中滴加少量氢氧化钠溶液。 |
无明显现象。 |
滤液中溶质的成分为 。 |
【反思评价】脱氧剂包装上应注明的注意事项是 (请写出一条)。
二氧化碳是人类生存不可缺少的物质,某兴趣小组利用如图装置对二氧化碳的性质进行以下探究。(夹持装置已省略)

(1)探究一:检查装置的气密性,打开 ,关闭 、 ,往B中加入药品。一段时间后观察到③处纸花先变红,①处纸花后变红,②处纸花不变色,说明二氧化碳能与水反应,该反应的化学方程式为 ,也能证明二氧化碳具有的物理性质是 。
(2)探究二:打开 ,关闭 、 ,C中出现浑浊,说明二氧化碳与氢氧化钙反应生成了碳酸钙。有同学质疑:白色固体可能是二氧化碳与水反应导致溶液中水减少而析出的氢氧化钙,小组同学向C中加入足量的水验证,白色固体不溶解,该方法利用了氢氧化钙和碳酸钙 (填具体性质)。
(3)探究三:打开 ,关闭 、 ,一段时间后,D中无明显现象。小组同学通过探究二的结论推理,二氧化碳能与氢氧化钠反应生成碳酸钠。为验证推理是否正确,进行了如下实验。
|
操作 |
现象 |
结论 |
|
向D反应后的溶液中加入足量的氯化钡溶液,振荡,观察现象 |
|
二氧化碳能与氢氧化钠反应生成碳酸钠 |
(4)废液处理:小组同学在对D试管的废液过滤后分类处理时,测得滤液显碱性,故向滤液中加入稀盐酸调节酸碱度,发现滴入盐酸时产生气泡,经检验该气体为二氧化碳,得出新的结论,探究三中二氧化碳与氢氧化钠反应除生成碳酸钠和水外,还生成 。
(5)依据二氧化碳的性质写出二氧化碳与氢氧化钾溶液反应的一个化学方程式: 。
小苏打在日常生活中常用于浸泡蔬菜以杀死虫卵,清除农药等。小苏打不稳定,受热易分解而变质( )。小明对厨房里的小苏打取样探究。
【做出猜想】猜想1:该样品是 ;猜想2:该样品是 ;
猜想3:该样品是 、 的混合物。
【查阅资料】① 受热不分解;②溶液中 与 不反应。
【定量探究】取该样品 g在一试管中充分加热至质量不再变化,冷却至初始温度称量,试管中物质质量为 g。
【讨论交流】测得 ,可以确定猜想 (填“1”“2”或“3”)不成立。
【定性探究】i.另取一定量该样品于烧杯中,加入足量 溶液,产生白色沉淀;
ii.待上述物质充分反应后过滤,向滤液中加入稀盐酸,产生气泡。
【反思与评价】
(1)实验i证明该样品中一定有 ,所发生反应的基本类型为 。
(2)根据实验i、ii,可以断定最初猜想 (填“1”“2”或“3”)正确,实验ii有关反应的化学方程式为 。
(3)实验中涉及过滤操作,下列有关说法正确的是 (填选项字母)。
a.使漏斗下段管口正对烧杯中央
b.玻璃棒末端斜靠在三层滤纸的一边
c.漏斗中滤纸边缘高于漏斗边缘
d.过滤器中的液面始终低于滤纸边缘
实验室贮存的镁条表面有一层灰黑色的物质,用砂纸打磨后发现镁是一种银白色的金属。镁在空气中燃烧发出耀眼的白光,生成白色的氧化镁固体。某化学实验小组对镁条表面的灰黑色物质产生了兴趣,并对其成分进行如下探究。
【提出问题】镁条表面的灰黑色物质是什么?
【猜想与假设】同学们根据空气的成分对镁条表面的灰黑色物质提出以下猜想:
猜想一:是MgO
猜想二:是
猜想三:是
猜想四:是
实验小组的小军同学认为灰黑色物质是氧化镁,但是遭到了其他同学的一致反对,
【设计实验】
|
实验序号 |
实验操作 |
实验现象 |
分析与结论 |
|
实验Ⅰ |
取一定量的灰黑色物质于试管中,滴加稀盐酸,将生成的气体通入澄清石灰水 |
试管中固体溶解,有气泡产生。生成的气体使澄清石灰水变浑浊 |
生成的气体是
|
|
实验Ⅱ |
另取一定量干燥的灰黑色物质于试管中,加热,将生成的气体依次通过无水硫酸铜和澄清石灰水 |
一段时间后,试管中的灰黑色物质变为白色,无水硫酸铜变为蓝色,澄清石灰水变浑浊 |
无水硫酸铜变为蓝色,说明产物中一定有 |
【结论与反思】
(1)写出实验Ⅰ中澄清石灰水变浑浊的化学方程式 。
(2)根据实验Ⅰ、Ⅱ的现象和结论,猜想 是正确的。
(3)写出实验Ⅱ中灰黑色物质受热分解的化学方程式 。
【拓展与提升】
镁条表面的灰黑色物质是镁与空气中的氧气、 共同作用,发生一系列化学反应形成的。为了防止镁条表面形成灰黑色物质,工业上往往将镁和铝制成合金。现有一块21g的镁铝合金与足量的稀硫酸充分反应,生成2g氢气,则这块镁铝合金中镁的质量是 g。
化学是一门以实验为基础的学科。请结合下列实验仪器图回答问题:
(1)写出仪器的名称:① ,② 。
(2)实验室用氯酸钾和二氧化锰加热制取氧气,反应的化学方程式为 ;该实验可选用 (填序号)和E组装成制取氧气的装置。现用该装置收集到一瓶气体,检验这瓶气体是氧气的方法: 。
(3) 是一种有臭鸡蛋气味的剧毒气体,密度比空气大,可溶于水,溶于水后的溶液叫氢硫酸。实验室常用 和稀 在常温下反应来制取 ,请写出该反应的化学方程式 。 必须要进行尾气处理,请写出 气体的发生、收集、尾气处理等装置的管口连接顺序 → → →h(填管口字母)。在容器G中将8g的 完全溶于水配成溶液来吸收 气体(可能发生的反应: , ),尾气吸收完全后得到的溶液中溶质质量是7.9g,则溶质可能是 。
某化学兴趣小组将镁条用砂纸打磨后按图Ⅰ所示方案进行实验。A中缓慢产生气泡,B、C中快速产生较多气泡,且C中有白色不溶物产生。
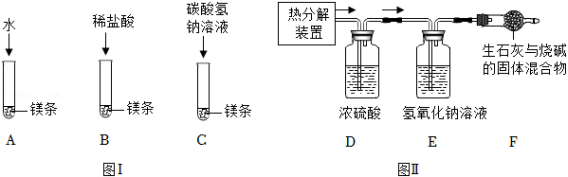
(1)图Ⅰ实验中取用镁条的仪器是_____(填“药匙”或“镊子”)。
(2)同学们经过讨论获知:水能解离出少量 ,且镁与稀盐酸反应的化学方程式为: ,则A中反应的化学方程式为_____。
同学们接着对C中产生的白色不溶物的成分进行了以下探究。
【提出问题】
C中产生的白色不溶物是什么呢?
【查阅资料】
① 和 均为白色不溶物。
② 和 均可与盐酸发生复分解反应。
③ 和 加热均易分解,分别生成两种氧化物。
④ 可溶于水,且不稳定,易分解为 。
⑤白色的无水硫酸铜遇水会变成蓝色。
【提出猜想】
(3)猜想一:白色不溶物是纯净的 。
猜想二:白色不溶物是纯净的_____。
猜想三:白色不溶物是 的混合物。
【实验验证】
(4)取该白色不溶物加足量的稀盐酸,发现不溶物全部溶解,并有气体产生,则猜想 不成立。再取干燥的该白色不溶物加热分解,并将所产生的气体通过无水硫酸铜,发现无水硫酸铜变蓝,由这两个小实验得出猜想_____成立。
【拓展探究】
(5)如图Ⅱ,称取干燥的该白色不溶物 克于热分解装置中,充分加热至不再产生气体,使分解产生的气体依次通过装置D、E,并使分解产生的气体全部被装置D、E吸收,实验后测得装置D增重 克,装置E增重 克,若该白色不溶物的组成用 表示,则 _____。
(6)装置F的作用是_____。
化学精灵提供的实验仪器和药品还有很多。某同学在做“稀盐酸中和氢氧化钠溶液”的实验时,发现向烧杯中滴加稀盐酸前忘了加入指示剂,导致无法判断该中和反应进行的程度,他赶紧补滴酚酞溶液,发现溶液仍然为无色。于是他和同学们一起对烧杯内溶液的溶质成分进行探究。
【提出问题】该烧杯内溶液的溶质除酚酞外还有什么?
【提出猜想】猜想一:只有 ;
猜想二:有_____(填化学式);
猜想三:有 和 。
【分析与思考】根据已有的实验现象,小爱认为其中猜想_____肯定不正确。
【进行实验】为进一步确认溶液的溶质成分,小荷进行了如下实验:取样,加入适量的碳酸钠溶液,观察到_____。
【得出结论】上述现象说明猜想二正确。
【反思与交流】小平认为,另选与小荷实验中不同类别的物质,如__________(填一种物质名称即可),也能得到上述相同的结论。
一种“贴身暖宝宝”的使用说明书如下,某化学兴趣小组围绕袋内物质展开探究。
品名:XX牌贴身暖宝宝 成分:袋内物质:铁粉、水、活性炭、食盐等 内袋材料:微孔透气无纺布 外袋材料:不透气塑料 用法:临使用前,打开外袋取出内袋,直接贴在衣服上,打开外袋后保持温暖12小时 |
【提出问题】袋内是否含有铁粉?
【进行实验】①取出袋内粉末于滤纸上,与磁铁充分接触。②将少量磁铁吸出的粉末加入足量稀硫酸中。
【收集证据】磁铁吸出的粉末与稀硫酸剧烈反应得到浅绿色溶液、同时_____。
【得出结论】袋内含有铁粉。
【做出猜想】被磁铁吸出的铁粉能在空气中燃烧。
【获取事实】将少许铁粉撒在酒精灯火焰上,铁粉立即剧烈燃烧、火星四射。
【反思交流】铁粉燃烧反应的化学方程式为__________。铁丝不能而铁粉能在空气中燃烧的原因是__________。
【拓展探究】用不同燃料测定空气里氧气的含量:分别在图甲所示装置的燃烧匙内放置铁粉、红磷(均足量),电加热引燃。氧气含量随时间变化情况如图乙、图丙:

(1)温度传感器显示,实验过程中瓶内温度均_____(填“升高”或“降低”)。
(2)待铁粉熄灭并恢复至室温后,打开弹簧夹,进入瓶内的水约占原水面上方空间体积的_____。
(3)分析图乙、图丙可知,实验中消耗氧气更彻底的是_____(填“铁粉”或“红磷”,下同),消耗氧气速率更快的是_____。
竹麻通过生石灰、草木灰(主要成分是 )浸泡以及打浆、抄纸等步骤可制得纸张。某兴趣小组模拟古代造纸技术,他们将一定量的生石灰、 足量的水溶解后,过滤得到澄清溶液。澄清溶液中溶质是什么,请你参与他们的探究。
【猜想假设】
猜想一:只含有
猜想二:含有 、_____
猜想三:含有 、
【设计实验】
实验步骤 |
实验现象 |
实验结论 |
1.取溶液少许于试管中,滴加过量稀盐酸 |
_____ |
猜想二不正确 |
2.取溶液少许于试管中,滴加少许_____溶液 |
_____ |
猜想三正确 |
【交流反思】
1.步骤2中发生反应的化学方程式为 _______________。
2.含有 、 的废水直接排放会造成水体污染。某小组同学对废水做如下处理(见如图)。C烧杯中出现__________现象时,说明废水中已无 、 。

海洋封存是实现“碳中和”的途径之一,其原理是利用 在水等溶剂中的溶解性来吸收 。某小组开展如下探究。
【活动一】探究 在水和食盐水(模拟海水)中的溶解情况
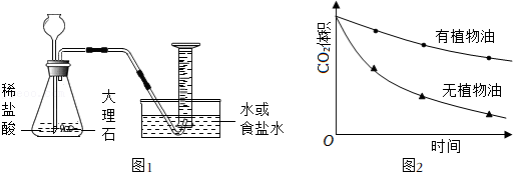
相同条件下,该小组分别用排水法、排食盐水法收集 (如图1),待收集 后,移出导管。每隔一段时间观察并记录量筒内 体积。重复实验,所测数据平均值如下表。
时间/ |
|
|
|
|
|
|
排水法时 体积/ |
|
|
|
|
|
|
排食盐水法时 体积/ |
|
|
|
|
|
|
(1)图1发生装置中反应的化学方程式为_____,反应类型是_____。
(2)由上表数据分析:
①能用排水法收集 的理由是_____。
②相同条件下,等体积水和食盐水吸收 更多的是_____(填“水”或“食盐水”)。
(3)海洋封存 可能带来的危害是_____(写出1点即可)。
【活动二】探究植物油隔离对 在水中溶解情况的影响
(4)小芳设计并完成以下对照实验:用两个量筒分别收集 倒置于水槽中,向其中一个量筒内注入少量植物油,使 与水被植物油隔开( 与植物油不反应)。测得量筒内 体积随时间变化曲线如图2。分析该图可得出的结论是_____。
【活动三】深度探究【活动二】中 的溶解情况
(5)①小松用图3表示无植物油隔离时,量筒内气体中存在的
分子的微观示意图。请参照图3的表示方式,在图4方框中画出有植物油隔离时,量筒内植物油和水中存在的分子的微观示意图(植物油分子用 表示)。
表示)。

②为检验有植物油隔离时 是否会进入水中,请设计实验方案:_________。
某小组用高锰酸钾制取氧气。如图是实验室中常见仪器,回答下列问题。
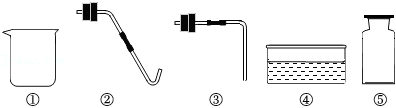
(1)仪器①的名称是_____。
(2)高锰酸钾制氧气的化学方程式为_____。组装氧气的收集装置,可选用_____(填序号)。
(3)某同学用排水法收集氧气时,发现水槽中的水变红了,可能是未使用_____(填实验用品名称)。若该同学收集的氧气不纯,原因可能是_____(写出1点即可)。
竹麻通过生石灰、草木灰(主要成分是 )浸泡以及打浆、抄纸等步骤可制得纸张。某兴趣小组模拟古代造纸技术,他们将一定量的生石灰、 用足量的水溶解后,过滤得到澄清溶液。澄清溶液中溶质是什么,请你参与他们的探究。
【猜想假设】
猜想一:只含有
猜想二:含有 、____
猜想三:含有 、
【设计实验】
实验步骤 |
实验现象 |
实验结论 |
1.取溶液少许于试管中,滴加过量稀盐酸 |
________ |
猜想二不正确 |
________ |
猜想三正确 |
【交流反思】
1.步骤2中发生反应的化学方程式为____________________。
2.含有 、 的废水直接排放会造成水体污染。某小组同学对废水做如下处理(见如图)。C烧杯中出现 ____________现象时,说明废水中已无 、 。

絮凝剂常用于水的净化,实验小组探究用絮凝剂净水时影响净化效果的因素。
【查阅资料】絮凝剂溶于水后能够吸附水中悬浮物并发生沉降,从而达到净水目的。硫酸铁是一种常见的絮凝剂。
【进行实验】
Ⅰ.配制水样和絮凝剂溶液
配制水样:向 水中加入 高岭土,搅拌、静置,取上层液作为水样。
配制絮凝剂溶液:用 水和 硫酸铁进行配制。
Ⅱ.探究影响水样净化效果的因素
取水样,向其中加入絮凝剂溶液,搅拌,测定静置不同时间水样的浊度,并计算浊度去除率(浊度去除率越高代表净化效果越好)。实验记录如下:
实验序号 |
水样的体积/ |
加入絮凝剂溶液的体积/ |
静置时间/ |
浊度去除率/ |
① |
|
|
|
|
② |
|
|
|
|
③ |
|
|
|
|
④ |
|
|
|
|
⑤ |
|
|
|
|
⑥ |
|
|
|
|
⑦ |
|
|
|
|
⑧ |
|
|
|
|
⑨ |
|
|
|
|
【解释与结论】
(1)配制絮凝剂溶液的操作如图所示。
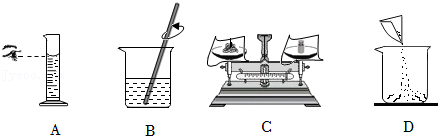
正确的操作顺序是_______(填序号), 中用玻璃棒搅拌的目的是_______。
(2)②中浊度去除率比①高的原因是_______。
(3)依据④~⑦得出的结论是______________。
(4)探究等量水样中加入絮凝剂溶液的体积对净化效果影响的实验是______________(填序号)。
【反思与评价】
(5)依据实验数据,不能得出“静置时间相同时,等量水样中加入絮凝剂溶液的体积越大,净化效果越好”的结论,其证据是_____________________。