实验室欲用 溶液制备氧气,并进行铁丝在氧气里燃烧的实验。回答下列问题:

(1)若用溶质质量分数为 的 溶液和 制备氧气,反应速率太快。为获得平稳的气流,下列发生装置(如图1)最合适的是_____(填标号);发生反应的化学方程式为_______________。
(2)已知:用 制取氧气时,也可用铂丝代替 作催化剂。如图2中甲装置可通过铂丝的上下移动控制反应的发生与停止,若制备过程中体系内压强过大,则安全管中的现象是__________,此时应将铂丝抽离过氧化氢溶液,使反应停止。
(3)用图2中乙装置进行铁丝在氧气里燃烧的实验,可观察到的现象是____________________;反应的化学方程式为_______________。
某校初三化学兴趣小组的同学为验证氢氧化钠的化学性质做了如下实验探究。请你根据实验回答有关问题。

(1)实验1的试管中可观察到的实验现象是 。
(2)甲同学观察到实验2无明显现象,他得出结论:氢氧化钠与盐酸不发生反应。乙同学认为甲同学的结论不正确,他改进了该实验方案:先向氢氧化钠溶液中滴入几滴
并振荡,再逐滴滴入稀盐酸,观察到溶液由红色变无色,由此可知氢氧化钠与稀盐酸 (填“发生”或“不发生”)化学反应。
(3)小亮同学由实验2联想到在氢氧化钠溶液中通入二氧化碳也没有明显现象,那么二氧化碳与氢氧化钠是否发生了化学反应呢?(本实验中忽略 溶于水)
Ⅰ.王敏同学从实验3得到的溶液中取出少量,加入试管中,滴入 溶液,观察到有白色沉淀生成,其反应的化学方程式为 ,证明二氧化碳与氢氧化钠发生了化学反应。
Ⅱ.为了验证 和 溶液发生了化学反应,晓霞同学设计了实验4图示实验方案,当观察到 现象时,证明二氧化碳与氢氧化钠溶液发生了化学反应。
Ⅲ.通过对氢氧化钠化学性质的探究,同学们得出保存氢氧化钠固体的方法是 。
某同学利用下列装置进行气体的制取和收集实验。请回答下列问题。
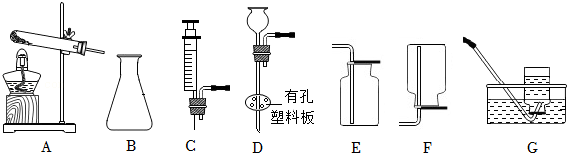
(1)写出仪器B的名称: 。
(2)实验室用加热高锰酸钾固体制取并收集氧气,应选用的装置是 (填字母序号,下同);所选装置中还需要改进的方法是 。
(3)实验室常用 (填药品名称)制取二氧化碳,发生装置要能达到“随开随起,随关随停”,需要选用的仪器有B和 。
(4)某同学选用B和C装置组合制取氧气,该组合的优点是 ,反应的化学方程式为 。
根据如图所示实验操作回答有关问题。
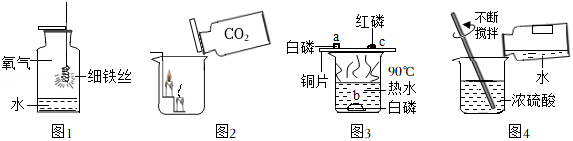
(1)图1实验中水的作用是 。
(2)图2实验,观察到的现象是 。
(3)图3是物质燃烧条件的探究实验,可观察到 (选填“a”“b”“c”)处的磷先燃烧。
(4)指出图4实验操作可能造成的后果 。
有一包从海水中获得的粗盐,已经经过初步提纯。课外活动小组对它的成分进行探究,并将粗盐进一步提纯。
一些物质的溶解性
OH﹣ |
Cl﹣ |
SO42﹣ |
CO32﹣ |
|
H+ |
溶、挥 |
溶 |
溶、挥 |
|
Na+ |
溶 |
溶 |
溶 |
溶 |
Ca2+ |
微 |
溶 |
微 |
不 |
Ba2+ |
溶 |
溶 |
不 |
不 |
Mg2+ |
不 |
溶 |
溶 |
微 |
探究过程:
Ⅰ.探究一:这包粗盐中可能有的杂质是CaCl2和MgCl2。
现用实验验证这种假设:取样品并溶解,加入数滴NaOH溶液,无明显现象,说明粗盐中无 ;另取样品并溶解,加入数滴碳酸钠溶液,有白色沉淀生成。
实验证明:这包粗盐中含有的杂质是 。
Ⅱ.探究二:这包粗盐中NaCl的质量分数。按下面步骤进行实验:
①称取ag的样品;
②将样品加水溶解,制成粗盐溶液;
③向粗盐溶液中加入过量的某种试剂,过滤,得到沉淀和滤液;
④将③中所得沉淀洗涤后小心烘干,称量得到bg纯净固体M;
⑤向③中所得滤液逐滴滴入稀盐酸,直到不再产生气泡为止后,移入蒸发皿蒸发,称量得到cg纯净固体N。
(1)②③⑤的步骤中,都使用到同一仪器是 ;它在步骤②和⑤中的操作方法相同,但目的不同,在步骤②中的目的是 。
(2)步骤③中加入的试剂是 ;目的是 。
(3)根据以上实验可知粗盐中NaCl的质量分数为 (用含字母的代数式表达)。
“珍爱生命,远离毒品”,冰毒是一种危害性很大的毒品,其主要成分是甲基苯丙胺(化学式为C10H15N)。某化学学习小组模拟对毒品的销毁,利用所制得的氧气燃烧冰毒,并检验所生成的二氧化碳气体,设计了如图实验。

本次实验只提供了如下化学试剂:5%的过氧化氢溶液,二氧化锰固体,浓硫酸,NaOH溶液,Ca(OH)2溶液,冰毒。请回答下列问题:
(1)仪器a的名称是 。
(2)为了完成此实验,除了选择装置B以外,还应选择的装置组合是 (填装置序号字母)。
(3)连接好装置,在加入药品前还必须进行的操作是 。
(4)检验二氧化碳时所发生反应的化学方程式为 。
我国“十四五”规划已经明确“2030年前实现碳达峰”的目标。碳达峰是指二氧化碳的排放达到峰值,不再增长。如图为自然界中CO2的循环图,图中箭头指向表示产生(排放)或消耗CO2的途径。回答下列问题:
(1)途径①需要消耗空气中的 。
(2)途径②中,枯枝败叶中的纤维素[化学式为(C6H10O5)n]在微生物作用下彻底转化为CO2和H2O,该转化中消耗O2与产生的CO2分子个数比为 。
(3)途径④通过光合作用吸收CO2的量白天 夜晚(填“大于”或“小于”)。

(4)途径⑤消耗的化石燃料是 (填“可”或“不可”)再生资源。
(5)降碳的一种途径是在合适的催化剂条件下,将二氧化碳与氢气反应使碳全部转化为乙烯(C2H4)、同时生成另一种化合物。请写出反应的化学方程式 。
(6)某年通过不同途径产生或消耗碳量的相对值如下表所示:
途径 |
① |
② |
③ |
④ |
⑤ |
⑥ |
⑦ |
相对值 |
0.6 |
60 |
60 |
121.8 |
5.5 |
92 |
90 |
据表可知,这一年大气中碳量增加了 (用表中相对值计算)。为达成“2030年前实现碳达峰”的目标,下列措施不可行的是 。
A.开发新能源
B.植树造林
C.禁止使用化石燃料
进一步分析上表回答:人口增多是否是大气中碳量增加的主要因素,并说明理由 。
某实验小组验证“Fe+Ag2SO4═FeSO4+2Ag”反应并进行了如下探究。已知银粉为黑色,22℃时Ag2SO4的溶解度为0.8g。
①22℃时,向盛有硫酸银饱和溶液的烧杯中加入过量铁粉,搅拌静置,观察到溶液变为黄色并逐渐加深。
②静置3小时后观察,烧杯底部仍有黑色粉末,溶液黄色几乎消失。
③用pH试纸检测Ag2SO4、FeSO4溶液,测得pH均小于7。
回答下列问题:
(1)22℃时,硫酸银饱和溶液显 性(填“酸”“碱”或“中”),其溶质质量分数为 。(列出计算式即可)
(2)取步骤①上层的黄色溶液少许滴加盐酸,观察到白色沉淀,该沉淀的化学式为 。
(3)某同学由步骤②中“仍有黑色粉末”得出Fe比Ag活泼的结论。小组同学讨论后认为思维不严密,因为黑色粉末不一定含Ag,还可能是 ,需要进一步实验才能得出结论,该实验方案是:取黑色粉末少许, 。(补充完实验方案)
(4)溶液呈黄色是因为含有Fe3+离子。小组对Fe3+产生的原因作出如下假设:
a.可能是铁粉表面有氧化物,可产生Fe3+;
b.空气中的O2能与Fe2+反应,可产生Fe3+;
c.溶液中存在 离子能与Fe2+反应,可产生Fe3+。
请设计实验证明假设a、b不是产生Fe3+的主要原因。实验方案是:向同样的铁粉中加入FeSO4溶液,振荡静置,观察到 时即可证明。
钨(W)是一种重要的战略金属。实验室需用干燥的H2还原WO3制备金属W,所用装置如图所示。已知Zn粒中往往含有ZnS杂质,焦性没食子酸溶液可用于吸收氧气。回答下列问题:
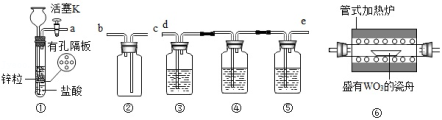
(1)装置①中用到的仪器有长颈漏斗、带导管的橡胶塞和 ,其反应的化学方程式有: 、ZnS+2HCl═ZnCl2+H2S↑。
(2)装置②的作用是安全瓶防倒吸,则a连接 (选填b、c、d或e)。
(3)装置③中盛装NaOH溶液,其作用是 。
(4)装置④⑤中盛装的溶液依次是 、 。
(5)装置①是启普发生器的简易装置,关闭活塞K后装置①中反应很快停止,其原因是 。
请同学们用如图装置完成相应气体的制取。

【资料】已知氨气是一种密度比空气小、极易溶于水且有刺激性气味的气体。以下两个反应均可产生氨气:
①碳酸氢铵受热分解:NH4HCO3 H2O+CO2↑+NH3↑
H2O+CO2↑+NH3↑
②熟石灰与氯化铵固体共热:Ca(OH)2+2NH4Cl CaCl2+2H2O+2NH3↑
CaCl2+2H2O+2NH3↑
【解决问题】
(1)实验室若用加热熟石灰与氯化铵固体混合物的方法制氨气,其发生装置可选用上述装置中的 (填字母代号),在用D装置收集氨气时可在a端放置一团蘸有酚酞试液的湿棉花,以便 。在选择制取氨气的反应原理时,选用反应②而不选用反应①的理由是 。
(2)上述装置中X仪器的名称为 ,请写出一个用A装置制氧气的反应的化学方程式 。
氨气(NH3)是一种重要化工原料,有刺激性气味,密度比空气小。某兴趣小组用加热NH4Cl和Ca(OH)2固体的方法制备、收集干燥的NH3,实验装置如图所示:
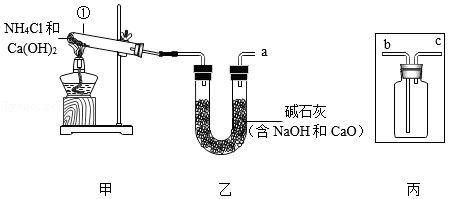
已知:2NH4Cl+Ca(OH)2 CaCl2+2NH3↑+2H2O,回答下列问题:
CaCl2+2NH3↑+2H2O,回答下列问题:
(1)图中仪器①的名称为 ,甲装置也可以用于实验室制备 (选填“H2”、“O2”或“CO2”)。
(2)乙装置的作用是 。
(3)丙装置用于收集NH3,则乙中导管口a应与丙中导管 端相连。
(4)从保护环境角度,该实验在丙装置后还应接一个 装置。
实验室制取X气体,该气体为氢气、氧气、氯气(Cl2)中的一种。根据如图回答问题:
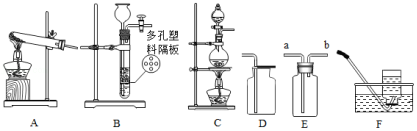
(1)用高锰酸钾制取并收集氧气:
①该反应的化学方程式为 ;
②用D装置收集氧气,检验收集满的方法 ;
③改用E装置(如图放置)收集氧气,气体应从 端(填“a”或“b”)通入;
(2)①实验室制取并收集氢气,可选用发生装置 (填字母)和收集装置F的组合;
②实验室常用二氧化锰粉末和浓盐酸在加热条件下制取氯气,可选用的发生装置为
(填字母)。
回答下列问题。
(1)某兴趣小组参观火力发电厂,了解到废气中的SO2、NO2、CO、CO2会影响环境,设计如图流程处理废气。
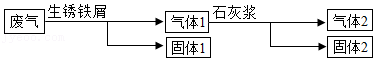
①用生锈铁屑处理废气中的CO,体现CO 性。
②用石灰浆不用石灰水的原因是 。
③固体2中有 (写两种物质)。
(2)A~D为初中化学常见物质,转化关系如图。A是由两种元素组成的钙盐,C是火力发电厂排放的温室气体。
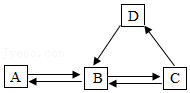
①B转化为A的化学方程式为 。
②若D广泛用于玻璃、洗涤剂的生产,则D转化为B的基本反应类型是 ;检验D中阴离子的方法是 。
③将足量C通入石蕊溶液中,现象是 ;测得该溶液pH=4,加热至90s时C完全排出,画出加热过程pH变化图像。
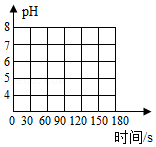
实验室用氯酸钾和二氧化锰制氧气,并回收产物。
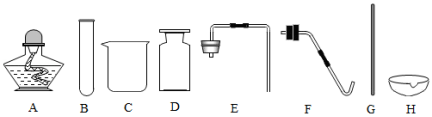
(1)氯酸钾制氧气的化学方程式为 ,制取装置需铁架台、水槽和
(填序号)。
(2)收集气体时,待集气瓶里的水排完后, (填操作),把集气瓶移出水槽,正放在桌上。
(3)将完全反应后的固体溶解、过滤、洗涤、蒸发,以上操作都用到的仪器名称是 。蒸发时需铁架台和 (填序号),当 时停止加热。
(4)产物KCl可作化肥,对植物的主要作用是 (填序号)。
a.促进叶色浓绿
b.增强抗寒抗旱能力
c.增强抗倒伏能力
早在春秋战国时期,我国就开始生产和使用铁器。某实验小组利用焦炭和Fe 2O 3模拟早期炼铁并检验可能的产物,实验装置如图:
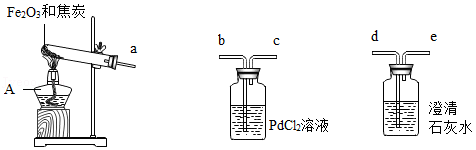
【查阅资料】①铁粉为黑色;常温下,Fe、Fe 3O 4可被磁铁吸引;
②PbCl 2溶液可用于检验CO,原理是:PdCl 2+CO+H 2O═Pd↓+CO 2+2HCl;
③Fe 3O 4与硫酸反应:Fe 3O 4+4H 2SO 4═FeSO 4+Fe 2(SO 4) 3+4H 2O。
【实验现象】澄清石灰水变浑浊,PdCl 2溶液中产生黑色沉淀,玻璃管内粉末全部变成黑色。冷却后,用磁铁靠近黑色固体,黑色固体被部分吸引。
(1)仪器A的名称是 。
(2)为了检验气体产物,装置从左到右的接口连接顺序为a→ → →
→ 。
(3)澄清石灰水变浑浊的化学方程式为 。
【实验结论】反应生成CO和CO 2,磁铁上的黑色固体可能是Fe、Fe 3O 4。
【提出猜想】磁铁上的黑色固体是什么?
猜想一:Fe
猜想二:Fe 3O 4
猜想三:Fe和Fe 3O 4
【设计实验】
| 设计思路 |
操作 |
现象 |
结论 |
| 定性实验 |
取少量黑色固体于试管中,加入足量稀硫酸,充分反应 |
固体完全溶解,产生气泡 |
猜想 成立 |
| 定量实验 |
取一定质量的稀硫酸(足量)放入烧杯中,加入5.6g黑色固体,充分反应后称量溶液的质量 |
固体完全溶解,产生气泡,溶液增加的质量为 g。 |
猜想一成立 |
【归纳总结】根据实验结论和探究结果C与Fe 2O 3反应的化学方程式为 。