新型洗涤剂过氧碳酸钠(Na 2CO 4)固体,能瞬间清除衣服上的汗渍、果汁渍等顽固污渍。它与水反应生成碳酸钠和其他化合物,某学习小组对产生的其他化合物进行探究。
实验1:溶解样品。取适量洗涤剂样品于烧杯中,加入适量蒸馏水,使之完全溶解,有气泡产生并形成无色溶液a。产生的气体能使带火星的木条复燃。
[提出问题]过氧碳酸钠与水反应生成的其他化合物是什么?
[猜想与假设]猜想一:H 2O 2
猜想二:NaOH
猜想三:H 2O 2、NaOH
猜想一、二、三除了遵循质量守恒定律外,猜想H 2O 2的其他理由是 。
实验2:验证
| 实验步骤 |
实验现象 |
分析与结论 |
| ①取适量溶液a于小烧杯中,加入稍过量的氯化钙溶液,过滤,得到清液b |
产生白色沉淀 |
加入稍过量氯化钙的目的是 。 |
| ②取适量清液b于试管中,加入过量二氧化锰,振荡 |
|
证明过氧碳酸钠与水反应有H 2O 2生成 |
| ③将步骤②所得混合物静置,取少量清液于试管中,滴加氯化铁溶液 |
无明显现象 |
|
[实验结论]猜想 正确。写出过氧碳酸钠与水反应的化学方程式: 。
[反思与评价]该洗涤剂保存时应密封、防潮。
如图是实验室制取气体的常用装置,请回答下列问题:

(1)写出仪器M的名称: 。
(2)实验室常用石灰石和稀盐酸制取二氧化碳,其反应的化学方程式为 ,应选用的发生装置和收集装置的组合为 (从A~E中选择)。
(3)若用装置A、F制取氧气,按气体流向,导管口连接顺序为 ,F装置还可用于干燥氧气,则需盛装的干燥剂为 (填名称)。
(4)某气体只能用E装置收集,则该气体可能具有的性质为 (填序号)。
①能与空气中的某物质反应
②密度与空气的密度接近
③能与水反应
请根据如图回答相关问题:

(1)实验A滤液仍然浑浊,可能的原因是 (答一点即可)。
(2)实验B观察到烧杯②中溶液变红,说明分子具有的性质是 。
(3)实验C中,将大小相同的白磷分别放入冷水和热水中,通入空气,观察现象。此实验说明燃烧的条件之一是 。
(4)配制溶液时,按图D所示量取溶剂,其他操作均正确,最终导致配制的溶液溶质质量分数 (填"偏大"或"偏小")。
硝酸是一种重要的酸,可用于生产化肥、染料和炸药。工业上利用氮的氧化物、氧气与水反应制备硝酸。
(1)某常见氮的氧化物中N、O两种元素的质量比为7:16,则该化合物的化学式为 。
(2)将该氮的氧化物23.0g与足量的氧气缓慢通入一定量水中(NO x+O 2+H 2O→HNO 3),得到60.0g硝酸溶液溶液的溶质质量分数为多少?(写出计算过程)
某校化学兴趣小组的同学发现长期露置在空气中的金属M表面会被锈蚀,于是他们一起探究金属M锈蚀的原因。经检测,锈蚀物中除含有M元素外,还含有C、H、O三种元素。
(1)甲同学依据锈蚀物中的组成元素,推测空气中 肯定参加了反应,但不能确定空气中的氧气是否参与反应。为了确认空气中的氧气是否参加反应,设计如图系列实验,你认为其中必须要做的对照实验是 (填字号)。
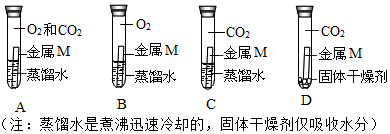
若观察到 (填现象),证明氧气参加了反应。
(2)若金属M是铜,铜器具长期露置在空气中会生成绿色铜锈,它的主要成分是碱式碳酸铜(Cu2(OH)2CO3)。小组同学欲探究Cu2(OH)2CO3的性质。
查阅资料:①Cu2(OH)2CO3的化学性质与Cu(OH)2和CuCO3混合物的性质相同
②Cu(OH)2受热分解生成CuO和H2O,CuCO3的化学性质和CaCO3相似
③白色CuSO4粉末遇水变蓝色
结合以上信息分析Cu2(OH)2CO3加热分解产物为 。
[实验探究]
为进一步验证Cu2(OH)2CO3受热分解产物,从如图中选择部分装置进行实验。装置的连接顺序为 ;实验中可观察到的现象是 。

[实验结论]碱式碳酸铜受热易分解。
如图是实验室常用的实验装置,请回答下列问题。
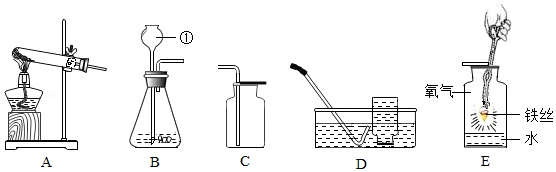
(1)仪器①的名称 。
(2)用A装置制取氧气的化学方程式 。C和D都可以收集O 2,选择D装置的优点 。
(3)E装置中水的作用 。
某兴趣小组取CaCO 3和CaCl 2的固体混合物7.5g,加入到盛有一定质量某浓度稀盐酸的烧杯中,恰好完全反应,气体全部逸出后,所得不饱和溶液的质量为41.8g。
烧杯及烧杯内物质质量随反应时间变化如表。
| 反应时间 |
0 |
t 1 |
t 2 |
t 3 |
| 烧杯及烧杯内物质质量 |
64 |
62.9 |
61.8 |
61.8 |
计算:
(1)生成CO 2的质量为 g。
(2)烧杯中原有稀盐酸的溶质质量分数是多少?
实验室有一瓶常用无色液体的标签模糊了(如图)。为确定该瓶溶液的溶质是什么,同学们进行了如下探究:
[提出问题]这瓶溶液的溶质是什么?
[作出猜想]猜想1:NaOH 猜想2:Na 2CO 3猜想3:NaHCO 3猜想4:NaCl
[查阅资料]NaHCO 3溶液显碱性,NaHCO 3溶液不与CaCl 2溶液反应。
[实验探究]
| 实验步骤 |
实验现象 |
实验结论 |
| 小亮取2mL该无色溶液于试管中,滴加2滴无色酚酞溶液 |
溶液变红 |
猜想1、3成立、猜想2、4不成立 |
| 小丽取2mL该无色溶液于试管中,加入3mL稀盐酸 |
立即产生气泡 |
猜想 不成立 |
[交流讨论]
(1)同学们一致认为小亮的实验结论不正确,理由是 。
(2)为了确定该无色溶液到底是什么,小强继续进行如下实验:
①取2mL该无色溶液于试管中,滴加CaCl 2溶液,边加边振荡,观察到产生白色沉淀。由此得出猜想 成立,反应的化学方程式为 。
②另取2mL该无色溶液于试管中,逐滴加入稀盐酸,一段时间后才观察到有气泡产生。
[拓展思考]小丽和小强都向无色溶液中加入稀盐酸,为什么现象不同?
[延伸探究]同学们查阅资料发现:向Na 2CO 3溶液中逐滴加入稀盐酸时,反应分两步进行:Na 2CO 3+HCl═NaHCO 3+NaCl;NaHCO 3+HCl═NaCl+CO 2↑+H 2O.故出现小强的实验现象。
[应用提升]现有两瓶失去标签的无色溶液,已知它们分别是碳酸钠溶液和稀盐酸中的一种,若不另加任何试剂要将二者鉴别开,你的鉴别方案是 (写出操作方法、现象和结论)。
走进化学实验室会给你带来无限乐趣。现有如图装置,结合装置图回答问题:
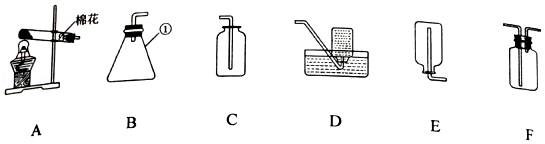
(1)写出图中带标号①的仪器名称 。
(2)连接装置A和D,可制取一种熟悉的气体,反应的化学方程式是 。要干燥制得的气体,可将气体通入F装置,F装置中应该装入的试剂名称是 。
(3)实验室制取气体发生装置的选择依据是 。选择装置B制取二氧化碳时,虽然操作简单,但无法控制反应速率。将该装置进行简单改进后就可达到控制反应速率的目的,改进措施是 。
化学兴趣小组要测定制作叶脉书签所用氢氧化钠溶液的浓度。取40g该氢氧化钠溶液于锥形瓶中,加入数滴酚酞溶液后再滴加质量分数为10%的稀硫酸,当锥形瓶中液体由红色恰好变成无色时,消耗稀硫酸的质量为49g。试计算该氢氧化钠溶液中溶质的质量分数。
经过一年的学习,同学们的化学探究能力得到了明显提升。兴趣小组想深入探究人体呼出气体的成分,进行如下活动:
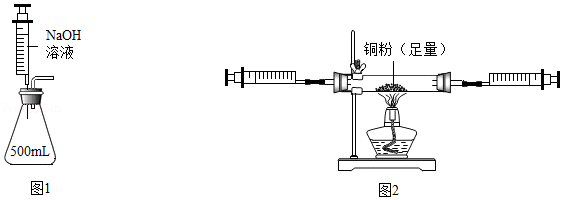
[活动一]探究人体呼出气体中是否含有CO 2
向装有呼出气体的集气瓶中滴加少量澄清石灰水,振荡后观察到 ,结论:人体呼出气体中含有CO 2。
[活动二]探究人体呼出气体中CO 2的体积分数
兴趣小组同学用图1所示装置进行实验。(锥形瓶内充满人体呼出的气体)实验前注射器内液体体积为50mL,向锥形瓶内注入少量液体后,注射器内的液体开始被自动吸入锥形瓶,充分反应后,注射器内NaOH溶液的体积为30mL。
小亮同学提出疑问:锥形瓶内CO 2是否反应完?
同学们展开了激烈的讨论,设计实验并证明锥形瓶内无色溶液中确实含有NaOH,得出锥形瓶内CO 2已反应完。
| 实验步骤 |
实验现象 |
实验结论 |
| ①取少量锥形瓶内无色溶液于试管中,加入 ②过滤,向滤液中滴加几滴酚酞溶液 |
③ , ④ 。 |
无色溶液中含有NaOH |
结论:人体呼出气体中CO 2的体积分数为 。
[活动三]探究人体呼出气体中O 2的体积分数
兴趣小组同学用图2所示装置进行实验。(注射器及玻璃管内充满人体呼出的气体)
①实验中需反复推拉注射器的目的是 ;
②在操作中如何判断装置中的O 2是否反应完? 。
结论:人体呼出气体中O 2的体积分数为16%。
[实验反思] 活动三所用方法与教科书上"测定空气里O 2的含量"的方法相比,其优点是: (答一点即可)。
如图是实验室制取气体常用的装置,请完成下列问题。

(1)写出标号①仪器的名称 ,实验室制取CO 2选择的药品是 (填字母);
A.块状大理石
B.块状碳酸钠
C.碳酸钙粉末
D.稀盐酸
E.稀硫酸
(2)写出实验室用A装置制取O 2的化学方程式 ,若要在相同时间内收集到纯度较高的O 2,则接口a应与接口 (填导管接口字母)相连,若此时收集到的O 2仍然不纯,则可能的原因是 (答一点即可)。
日常生活中的红糖、白糖和冰糖主要成分都是蔗糖。蔗糖的溶解度随温度的升高而急剧升高。同学们想除去红糖中的色素和少量可溶性盐得到冰糖,操作步骤如下:
①取一定质量的红糖加足量水溶解,制成红糖水;②对红糖水进行脱色处理;③分离无色糖水和固体残渣;④将无色糖水蒸发浓缩制得浓糖水;⑤经过操作得到冰糖。
请根据以上信息完成下列问题:
(1)步骤①中,玻璃棒不断搅拌的目的是 ;
(2)步骤②中应加入 ;
(3)步骤③进行的操作是 ;
(4)步骤⑤进行的操作是 。