随着手机、电脑等移动设备的普及,人们对充电设备的要求越来越高。最近,某品牌氮化镓充电设备以体积小、功率大深受消费者喜爱。
(1)氮化镓(GaN)是充电设备中的核心材料。查阅资料得知:氮化镓中氮元素的化合价与氨气(NH3)中氮元素的化合价相同。由此可知,氮化镓中镓元素的化合价为 。
(2)氮化镓的制取可通过镓与氨气在高温下发生置换反应来实现,其反应的化学方程式为 。
除H2、CO能还原氧化铜外,CH4及其它一些具有还原性的气体也能与氧化铜发生反应。如:加热时,CH4能与CuO反应生成Cu、CO2和H2O.某拓展小组同学设计了如图所示实验装置(夹持装置省略),分别对有关气体问题进行探究。请按要求回答相关问题。
【探究Ⅰ】对已知气体性质的探究。
(1)将CH4气体按如图所示装置进行规范实验,可观察到的实验现象有 (填序号);
①A装置中的黑色粉末变成光亮的红色物质
②B装置中的固体由白色变蓝色
③C装置中溶液变浑浊
【探究Ⅱ】对气体组成的探究。
(2)气体X可能由H2、CH4中的一种或两种组成,同学们按如图所示实验装置对其组成进行探究。
①C装置中溶液变浑浊,可证明气体X中含有 ;
②根据B装置中的固体由白色变蓝色的现象,得出气体X中含有H2的结论,请对此结论作出评价,并说明理由 ;
【探究Ⅲ】对未知气体的探究。
(3)将某火箭燃料X通过如图所示装置,观察到A装置中的黑色粉末变成光亮的红色物质;B装置中的固体由白色变蓝色,C装置中溶液不变浑浊。C中导出的气体是空气中含量最多的物质。已知燃料X是由2种元素组成的纯净物,其相对分子质量为32.根据现象及信息推断并写出:A装置中发生反应的化学方程式为 。
随着手机、电脑等移动设备的普及,人们对充电设备的要求越来越高。最近,某品牌氮化镓充电设备以体积小、功率大深受消费者喜爱。
(1)氮化镓(GaN)是充电设备中的核心材料。查阅资料得知:氮化镓中氮元素的化合价与氨气(NH3)中氮元素的化合价相同。由此可知,氮化镓中镓元素的化合价为 。
(2)氮化镓的制取可通过镓与氨气在高温下发生置换反应来实现,其反应的化学方程式为 。
某兴趣小组对“稀盐酸与石灰石是否恰好完全反应”展开了系列实验(稀盐酸与石灰石中杂质不反应)。
【实验操作】取一块状石灰石于试管中,往试管中加入5毫升稀盐酸。
【实验现象】①开始时固体表面有大量气泡;②反应停止后,试管底部有块状固体残留、固体表面无气泡;③试管内溶液无色。
【初步分析】(1)反应停止后,某同学根据上述实验现象进行初步判断,得出了石灰石没有反应完的结论。支持该同学得出这一结论的依据是 (填上述实验现象的序号)。
【小组讨论】大家讨论后认为,要判断是否恰好完全反应,可以从液体和固体两条途径进行探究:一是探究残留液体中是否还有盐酸;二是探究残留块状固体中是否还有碳酸钙。
【继续探究】(2)对原残留液体是否还有盐酸的探究,有同学取原残留液体,滴加AgNO3溶液、产生白色沉淀,再滴加稀硝酸沉淀不溶解。于是根据这一现象,得出了原残留液体中存在盐酸的结论。但小金认为根据这一现象是不能得出原残留液中存在盐酸的结论,小金的理由是 。
(3)探究原残留液体中是否还有盐酸,真正需要检验的离子是 。
(4)探究残留块状固体中是否还有碳酸钙。小丽取原残留块状固体用水洗净后加入稀盐酸,将产生的气体通入澄清石灰水,出现了 的现象,于是得出残留块状固体中还存在碳酸钙。
【实验结论】在原反应结束时,稀盐酸与石灰石没有恰好完全反应,石灰石中碳酸钙有剩余。

小明利用稀硫酸与生锈的铁屑反应制取硫酸亚铁,实验流程如图:
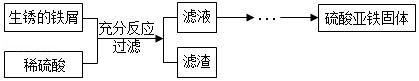
资料:①Fe2(SO4)3+Fe═3FeSO4;②硫酸亚铁容易被氧化为硫酸铁等物质。
(1)配制50克溶质质量分数为19.6%的稀硫酸,需溶质质量分数为98%的浓硫酸 克。
(2)写出该实验中的一条化学方程式(除资料①中的反应外) 。
(3)稀硫酸与生锈的铁屑充分反应后,要确保铁有少量剩余,其目的是 。
将12.9克NaCl和Na2CO3固体混合物完全溶于水中形成溶液,再将75克CaCl2溶液分5次加入到该溶液中,充分反应,测得的实验数据如下表。
实验序号 |
1 |
2 |
3 |
4 |
5 |
加入CaCl2溶液质量/克 |
15 |
15 |
15 |
15 |
15 |
生成沉淀的总质量/克 |
3 |
m |
9 |
10 |
10 |
求:(1)表格中m的数值是 。
(2)溶液中Na2CO3完全反应是在第 次实验。
(3)固体混合物中Na2CO3的质量分数。(精确到0.1%)
(4)请画出上述过程溶液中NaCl质量的变化图。
复方碳酸氢钠片是一种常用的抗酸剂药物,口服后能迅速中和或缓冲胃酸,减少疼痛等症状。复方碳酸氢钠片的主要成分是碳酸氢钠(与盐酸反应的化学方程式为:NaHCO3+HCl═NaCl+H2O+CO2↑)。
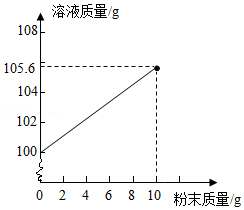
某科学兴趣小组为了测定药片中碳酸氢钠的含量做了以下实验:先将复方碳酸氢钠片制成粉末,取10克分多次放入盛有100克稀盐酸的烧杯中充分反应。测出加入的粉末质量和反应后的溶液质量,两者质量关系如图所示。
(1)实验后,兴趣小组又往烧杯中加入少量粉末,观察到 ,说明上述实验结束时稀盐酸过量。
(2)计算复方碳酸氢钠片中碳酸氢钠的含量。
(3)计算10克粉末与稀盐酸反应后所得氯化钠溶液的溶质质量分数。(计算结果精确到0.1%)
某化学兴趣小组同学做了实验后在整理实验室时,得到白色固体药品,查阅药品记录单可知,可能是碳酸钠、碳酸氢钠和硫酸钠中的两种物质的混合物。为探究其成分,进行如下探究活动:
[猜想与假设]针对其组成:
猜想一:含有Na2CO3和Na2SO4;
猜想二:含有Na2SO4和NaHCO3;
猜想三:含有 。
[实检探究]
实验Ⅰ:取白色固体于试管中加热,将产生的无色无味气体通入澄清石灰水,澄清石灰水变浑浊。
实验Ⅱ:取加热后的白色固体于试管中加足量的盐酸后,再滴加氯化钡溶液,立即产生白色沉淀。
[实验分析及结论]
(1)实验Ⅰ中,产生无色无味气体反应的化学方程式为 。实验Ⅱ中,滴加氯化钡溶液产生白色沉淀反应的化学方程式为 。
(2)实验Ⅰ中可判断猜想 不成立。
综合实验Ⅰ、Ⅱ,可判断猜想 不成立。
[拓展延伸]
若Na2SO4溶液中混有少量的NaHCO3,提纯Na2SO4溶液的实验方案是 。
日常生活中的红糖、白糖和冰糖主要成分都是蔗糖。蔗糖的溶解度随温度的升高而急剧升高。同学们想除去红糖中的色素和少量可溶性盐得到冰糖,操作步骤如下:
①取一定质量的红糖加足量水溶解,制成红糖水;②对红糖水进行脱色处理;③分离无色糖水和固体残渣;④将无色糖水蒸发浓缩制得浓糖水;⑤经过操作得到冰糖。
请根据以上信息完成下列问题:
(1)步骤①中,玻璃棒不断搅拌的目的是 ;
(2)步骤②中应加入 ;
(3)步骤③进行的操作是 ;
(4)步骤⑤进行的操作是 。
如图是实验室制取气体常用的装置,请完成下列问题。

(1)写出标号①仪器的名称 ,实验室制取CO 2选择的药品是 (填字母);
A.块状大理石
B.块状碳酸钠
C.碳酸钙粉末
D.稀盐酸
E.稀硫酸
(2)写出实验室用A装置制取O 2的化学方程式 ,若要在相同时间内收集到纯度较高的O 2,则接口a应与接口 (填导管接口字母)相连,若此时收集到的O 2仍然不纯,则可能的原因是 (答一点即可)。
一水硫酸四氨合铜的化学式为[Cu(NH3)4]SO4•H2O,是一种高效、安全的杀菌剂。它在乙醇﹣﹣水混合溶剂中的溶解度随乙醇体积分数的变化曲线如图甲所示。小明在实验室以氧化铜为主要原料合成该物质,他设计的合成路线如图乙所示:

(1)溶液A中一定存在的溶质为 。
(2)溶液B中含硫酸四氨合铜,“一系列操作”是指向溶液B中加入适量 、过滤、洗涤、干燥等。
开春以来,为提高水稻产量,某农场积极做好科学施肥、精准防治病虫害等工作。
(1)水稻不同生长期需要不同的肥料。如在水稻抽穗、开花时期,为促进穗数增多、籽粒饱满,需要多施磷肥。下列属于磷肥的是 。
| A. |
碳酸钾( ) |
| B. |
尿素[ ] |
| C. |
磷酸二氢钙[ ] |
(2)氮肥能促进水稻幼苗生长。一百亩水稻需要施碳酸氢铵3950千克,用氨气、水和二氧化碳反应来制取,化学方程式为 ,需要氨气多少千克?
(3)井冈霉素是防治水稻纹枯病的常用药。要为一百亩水稻喷洒一次这种农药,需要配制溶质质量分数为0.01%的药液7500千克,应购买5%的井冈霉素药液 千克。
2022年我国将有6名航天员生活在空间站。氧气、水、食物等是维持航天员驻留空间站的必要物质。为提高物质的利用率,目前空间站通过以下途径实现物质循环利用:
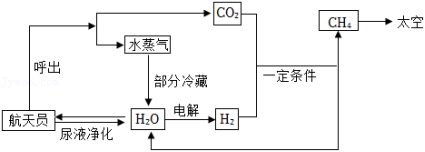
(1)由图可知,目前空间站通过物质循环获得水的途径共有 条,其中尿液净化时必须除去尿液中的 等代谢废物。
(2)为实现氧的循环,目前空间站内利用氢气和航天员呼出的二氧化碳,在一定条件下转化为甲烷和水,化学方程式为 。据测算,正常情况下一位航天员一天呼出的二氧化碳质量约1.1千克,若这些二氧化碳全部与氢气反应,则可生成水多少千克?
海洋是人类宝贵的自然资源,海水“晒盐”和海水“制碱”体现了人类利用和改造自然的智慧,请根据粗盐“制碱”的流程图(如图)回答问题:
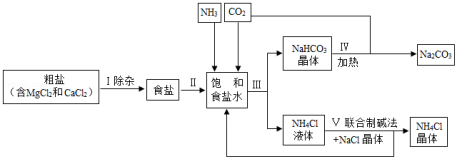
(1)步骤Ⅰ除杂中,常见的方法有两种:一是物理方法,即用NaCl溶液浸洗粗盐,溶解除去其中的可溶性杂质,则浸洗溶液应选用NaCl的 (填“饱和”或“不饱和”)溶液;二是化学方法,操作步骤依次为:加水溶解→加过量试剂①→加过量试剂②→过滤→加适量盐酸,以下试剂①②组合选用合理的是 。
A.①Ca(OH)2②Na2CO3
B.①Na2CO3②Ca(OH)2
C.①KOH②Na2CO3
D.①NaOH②Na2CO3
(2)步骤Ⅲ先向饱和食盐水中通入氨气,再通入二氧化碳,这样做的目的是 ,写出步骤Ⅲ反应的化学方程式 。
(3)步骤Ⅳ发生的反应属于 反应(填基本反应类型)。
(4)我国化学家侯德榜创立的联合制碱法的优点有 。
A.无“索尔维氨碱法”中的废弃物CaCl2生成,有利于保护环境
B.大大提高了食盐的利用率,节约了成本
C.将“制碱”与制氨生产联合起来,同时析出的NH4Cl晶体可用作复合肥
如图是某化工企业利用“侯氏制碱法”生产纯碱的部分工艺流程示意图:
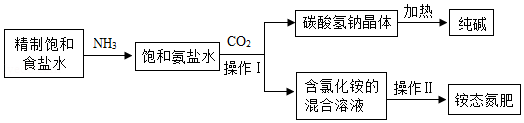
查阅资料知:①NH4Cl NH3↑+HCl↑;②氨气极易溶于水,氨水呈碱性。
(1)检验食盐水是否饱和的方法是 。
(2)操作Ⅰ的名称是 。实验室进行此操作时,玻璃棒的作用是 。
(3)“侯氏制碱法”中,向饱和氨盐水中通入足量的CO2,使氨气、水、NaCl和CO2反应生成NaHCO3等,该反应的化学方程式为 ;先通氨气形成饱和氨盐水,后加压通入二氧化碳,这样操作的目的是 。
(4)处理含氯化铵混合溶液时,不直接加热蒸干得到氯化铵固体的原因是 。